20##-2015武警部队院校招生统一考试物理模拟题
一、选择题
1、调查发现,某些新装修的居室中空气污染物浓度过高,对人体健康产生一定影响.这些污染物最常见的是( )

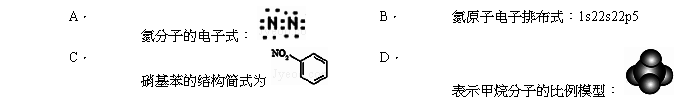
2、下列有关化学用语正确的是( )
3、下列依据热化学方程式得出的结论正确的是
A.已知2SO2(g)+O2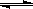 2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)==C(金刚石,s) △H>0,则金刚石比石墨稳定
C.已知H+(aq)+OH-(aq)=H2O(1) △H=-57.3kJ·mol-1,则任何酸碱中和的反应热均为57.3 kJ
D.已知2C(s)+2O2(g)==2 CO2(g) △H1,2C(s)+O2(g)==2CO(g) △H2;则△H1<△H2
4、下列各组离子在溶液中能大量共存,加入OH-有沉淀生成,加入H+有气体
生成的一组离子是 ( )
A.K+、Mg2+、Cl-、HCO B.K+、Cu2+、SO
B.K+、Cu2+、SO 、Na+
、Na+
C.NH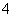 、CO
、CO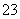 、NO
、NO 、Na+ D.NH
、Na+ D.NH 、Cl-、HCO
、Cl-、HCO 、K+
、K+
5、在某无色透明的酸性溶液中,能大量存在的离子组是 ( )
A.Na+ 、K+、SO42-、HCO3- B.Cu2+、K+、SO42-、NO3-
C.Na+、 K+、Cl-、 NO3- D.Fe3+、K+、SO42-、Cl-
6、 下列物质在水溶液中的电离方程式不正确的是
A.NaHSO4 ===Na++H++SO42-
B.AgCl ===Ag++ Cl-
C.Ba (OH)2 ===Ba2+ + 2OH-
D. CH3COONH4 NH4++ CH3COO-
NH4++ CH3COO-
7、下列说法不正确的是
A.金属单质与盐溶液的反应都是置换反应
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3属于化合反应
C.SO2+Cl2+2H2O=2HCl+H2SO4属于氧化还原反应
D.AgNO3+HCl=AgCl↓+ HNO3该反应不能说明盐酸酸性比硝酸强
8、 下列有机物的名称正确的是
A.2,2-二甲基-3-戊烯 B.4,5-二甲基-3-乙基己烷
C.2,3,3-三甲基丁烷 D.2,3-二甲基-4-乙基已烷
9、下列各组物质中,互称为同位素的是
A.甲烷和乙烷 B.氧气和臭氧 C.126C和146C D.正丁烷和异丁烷
10、下列各组液体混合物中,能用分液漏斗分离的是 ( ).
A.淀粉溶液和食盐溶液 B.CCl4和水
C.乙烷和乙烯 D.乙酸和乙醇
二、填空题
11、 (1)硫酸氢钾电离:
(2)氢氧化钡与稀硫酸反应的离子方程式:
(3)用双线桥或者单线桥法标明该反应的电子转移,并填空。
3Cl2 + 6 NaOH===5NaCl + NaClO3 + 3H2O
氧化剂与还原剂的质量比__________, 还原产物与氧化产物的物质的量之比___________
12、写出下列反应的化学方程式
1、制取漂白粉的化学方程式
2、过氧化钠与二氧化碳反应
3、钠与水反应
4、钠与硫酸铜溶液反应
5、氯气与水反应
13、今有下列气体:H2、Cl2、CH4、HCl、NH3、NO、H2S、SO2,用 如 图装置进行实验,填写下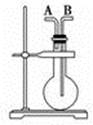 列空白:
列空白:
(1)当烧瓶干燥时,从A口进气可收集的气体是 ________________,从B口进气可收集的气体是________。
(2)当烧瓶中充满水时,可用来测量________等气体的体积。
(3)当烧瓶中装入某种溶液,用于洗气时,气体应从____ ____口进入烧瓶。
____口进入烧瓶。
14、对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、渗析、加热分解等。下列各组混和物的分离或提纯,应采用什么方法或加何种试剂:
(1)除去乙醇中溶解的食盐,方法是________________。
(2)除去Ca(OH)2溶液中悬浮的CaCO3颗粒用________操作。
(3)除去KCl溶液中的SO ,依次加入的溶液为(填化学式):________、________、________。
,依次加入的溶液为(填化学式):________、________、________。
(4)用食用酒精浸泡中草药提取其中的有效成分,其过程称________;从碘水中提取碘采用________操作。
15、 只用试管和胶头滴管就可以鉴别的下列各组溶液是 (填序号)
①AlCl3溶液和NaOH溶液 ②Ca(HCO3)2溶液和NaOH溶液 ③NaAlO2溶液和盐酸 ④Al2(SO4)3溶液和氨水 ⑤AgNO3溶液和氨水
16、按要求填空:
(1)分子中有18个氢原子的链烷烃的分子式: ▲
(2)2,3—二甲基—1—丁烯的结构简式: ▲
(3)用系统法命名:
▲
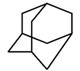 分子结构中有 ▲ 手性碳原子。
分子结构中有 ▲ 手性碳原子。
(4)CH2=CH—C≡CH结构中碳原子轨道的杂化方式是 ▲
(5)有机物的结构可用“键线式”简化表示。如CH3—CH=CH-CH3可简写为: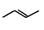 。
。
 的分子式为 ▲ ,1mol该烃完全燃烧,需要标准状况下氧气
的分子式为 ▲ ,1mol该烃完全燃烧,需要标准状况下氧气
▲ 升;该烃的一溴取代物有 ▲ 种。
17、同学们已经学习了同位素、同系物、同素异形体、同分异构体,你能区别这些概念吗?下面列出了几组物质,请将物质的合适组号填写在下表中。
①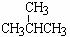 和
和 ; ②
; ②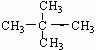 和
和 ;
;
③CH4和CH3CH2CH3; ④金刚石与石墨; ⑤氕、氘与氚; ⑥16O、17O和18O
⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3); ⑧氧气(O2)与臭氧(O3)。

18、 (1)有化合物A、B、C、D、E、F、G、H和单质甲,其中C是盐类化合物,H为酸性氧化物,它们在一定条件下有如下的转化关系:
G + A → 甲 + H D + A→ C + B C + E → F↓(红褐色) + NaCl
则A、B、G的化学式:A B G
(2)有化合物A、B、C、D、E、F、G,其中A为金属氧化物,它们之间有下列转化关系:
①A +B→ C + E ②C + NaOH →D蓝色↓ + F ③F + Ba(NO3)2 → G白↓ + NaNO3
写出下面各物质的名称:E F
19、有A、B、C、D、E、F六种化合物,它们之间的反应关系如下所示:
① A+B→C+E ② C+NaOH→蓝色沉淀D+F ③ D A+E ④ F+Ba(NO3)2→白色沉淀+NaNO3
A+E ④ F+Ba(NO3)2→白色沉淀+NaNO3
回答下列问题(1) 写出它们的化学式:
A B C D E F 。
(2)写出①②③④反应的化学方程式,属于离子反应的只写离子方程式
① ②
③ ④
三、计算题
20、某1 mol链烃A在一定条件下完全裂化成1 mol烷烃B和1 mol烯烃C,生成的混合气体对H2的相对密度为14.5。试通过计算回答下列问题:
(1)写出链烃A分子式。
(2)烷烃B和烯烃C可能各是什么物质?
(3)如果要求1 mol B完全燃烧时需要O2的物质的量是整数,那么C只能是什么烯烃?
21、将标准状况下的HCl气体8.96L溶于水形成100mL溶液,然后与足量的铁屑充分反应。计算:(要有计算过程,只有结果计零分)
(1)所得盐酸溶液的物质的量浓度。
(2)参加反应的铁的质量;生成H2的体积(标况)
(3)将生成的FeCl2配成400ml溶液,此溶液中FeCl2的物质的量浓度是多少?
22、取100mLNa2CO3和Na2SO4的混合液,加入过量BaCl2溶液后得到10.21g白色沉淀,用过量稀硝酸处理后沉淀质量减少到2.33g,并有气体放出。试计算:
①原混合物中Na2CO3和Na2SO4的物质的量浓度。
②产生的气体在标准状况下的体积。
参考答案
一、选择题
1、选D.
2、分析:
A.氮气分子中存在氮氮三键,即两个氮原子之间存在3对共用电子对;
B.氮原子的核电荷数为7,最外层含有5个电子,2p轨道应为3个电子;
C.硝基书写错误,硝基写在苯环左边,应该表示为:O2N﹣;
D.甲烷为正四面体结构,分子中存在1个C、4个H原子,且碳原子半径大于氢原子.
解答:
解:A.氮气中存在3对氮氮共用电子对,氮气分子正确的电子式为: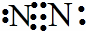 ,故A错误;
,故A错误;
B.氮原子的结构示意图为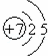 ,最外层为5个电子,含有两个电子层,则其原子正确的电子排布式为:1s22s22p3,故B错误;
,最外层为5个电子,含有两个电子层,则其原子正确的电子排布式为:1s22s22p3,故B错误;
C.硝基写在苯环左边,应该表示为:O2N﹣,硝基苯正确的结构简式为: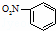 ,故C错误;
,故C错误;
D.甲烷中含有1个C、4个H原子,C原子半径大于氢原子,为正四面体结构,甲烷分子的比例模型为: ,故D正确;
,故D正确;
故选D.
3、D 4、A 5、C6、D 7、A 8、D9、C10、B
二、填空题
11、(1)KHSO4==== K+ + H+ + SO42-
(2)Ba2+ + 2OH- + 2H+ + SO42- ====BaSO4  + 2H2O
+ 2H2O
(3) 5e-
 3 Cl2+6NaOH===5NaCl+NaClO3+3H2O 5:1 5:1
3 Cl2+6NaOH===5NaCl+NaClO3+3H2O 5:1 5:1
12、 (1)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
(2) 2Na2O2+2CO2=2Na2CO3+O2↑ (3) 2Na+2H2O===2NaOH+H2
(4)2Na+2H2O+CUSO4=CU(OH)2+H2+Na2S04 (5) Cl2+H2O=HCl+HClO
13、解析 解答本题时注意以下两点:
(1)排气法收集气体要比较气体与空气的密度大小,该气体是否与空气中的成分反应;
(2)排水法收集气体时短进长出。
答案 (1)H2、CH4、NH3
Cl2、HCl、H2S、SO2
(2)H2、CH4、NO (3)B
14、 (1)蒸馏(2) 过滤(3)BaCl2 K2CO3 HCl (4) 萃取 萃取(或萃取分液)
15、①③⑤
16、(1)C8H18
(2)CH2=C(CH3)CH(CH3)CH3
(3)3,3,4—三甲基已烷 1
(4)sp2 sp
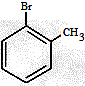 (5)C10H16 313.6 2 (每空2分)
(5)C10H16 313.6 2 (每空2分)
17、类别
同位素
同系物
同素异形体
同分异构体
组号
⑤⑥
①③
④⑧
②⑦
18、 (1) Fe2O3;H2O;CO (2)水;硫酸钠
19、 (1) CuO H2SO4 CuSO4 Cu(OH)2 H2O Na2SO4
(2)CuO + 2H+ ==== Cu2+ + H2O Cu2+ + 2OH- ==== Cu(OH)2
Cu(OH)2 ==== CuO + H2O SO42- + Ba2+====BaSO4 
三、计算题
20、(每小题2分,共6分)(1)C4H10(2)B:CH4 C:CH2==CHCH3或B:C2H6 C:CH2==CH2
(3)CH2==CHCH3
21、【答案】(1) 4mol/L (2) 11.2g;2.24L (3) 0.5mol/L
22、c(Na2SO4)=0.1mol/L c(Na2CO3)=0.4mol/L
气体体积为0.896L
第二篇:20xx武警部队院校招生统一考试综合模拟试题三
20##武警部队院校招生统一考试综合模拟试题三
化学部分(共60分,45min)
相对分子量H-1,C-12 ,O-16,N-14
一. 单项选择题(本题共6题,每题3分,共18分)
1. 下列两种物质均为纯净物的是
A 重水 王水 B 汽油 煤油
C 干冰 冰醋酸 D 水玻璃 硫酸铝钾
2. 碳的同素异形体所共有的性质是
A 硬度高 B 能导电
C 有金属光泽 D 能与氧气化合生成二氧化碳
3. 下列离子方程式书写错误的是
A 铜片放入FeCl3溶液中 Fe3+ + Cu = Cu2+ + Fe2+
B 硫化亚铁放入稀硫酸中 FeS + 2H+ = H2S + Fe2+
C 在FeCl3溶液中加入足量氨水 Fe3+ + 3OH- = Fe(OH)3¯
D 钠与水反应 2Na + 2H2O = 2Na+ + 2OH- + H2
4. 常温常压下,1g甲烷在氧气中完全燃烧生成液态水和二氧化碳气体时,放出56KJ热量,则下列热化学方程式中正确的是
A CH4(气) + 2O2(气) = 2H2O(液) + CO2(气) - 896KJ
B 1/2CH4(气) + O2(气) = H2O(液) + 1/2CO2(气) + 448KJ
C 1/2CH4(气) + O2(气) = H2O(气) + 1/2CO2(气) + 448KJ
D CH4(气) + 2O2(气) = 2H2O(液) + CO2(气) + 896KJ
5. 在高温下用一氧化碳还原mg氧化铁得ng铁,氧的原子量为16,则铁的原子量为
A 2(m-n)/3n B n/24(m-n)
C (m-n)/8n D 24n/(m-n)
6. 下列除去杂质的实验方法正确的是
A.除去CO中少量O2:通过灼热的Cu网后收集气体
B.除去K2CO3固体中少量NaHCO3:置于坩埚中加热
C.除去苯中溶有的少量苯酚:加入适量浓溴水反应后过滤
D.除去FeCl3酸性溶液中少量的FeCl2:加入稍过量双氧水后放置
二.填空题(共5题,共 31 分)
7.在一定条件下,反应 2A B + C 达到平衡。
B + C 达到平衡。
(1)若升高温度,平衡向正反应方向移动,则逆反应是 。
(2)若增加或减少B时,平衡不移动,则B是 态。
(3)若A、B、C均为气态,在温度和容积一定的条件下增大B的浓度,则A与C的物质的量之比 (填“增大”、“减小”或“不变”)
8.有A、B、C、D四种化合物,常温下固体A与B 溶液反应后有无色的气体C放出.若过量C通入烧碱溶液又生成A,C与氧气化合后的产物D通入水中又生成B.则A是 ,B是 ,C是 D是 .
.
9. 为得到39%的硝酸,应向300g 47%的硝酸中加入23%的硝酸的质量为
10.分子式为C4H10的一氯取代有_______种;化学式为C8H18的烷烃中,含有3 个甲基的同分异构体的数目是_______。
11.现有以下几项操作:① 加适量盐酸 ② 加适量水溶解 ③ 过滤 ④ 高温或加热灼烧 ⑤ 蒸发,请选择合适的操作,以除去下列各物质中含有的少量杂质,并将其标号按操作的先后顺序填在横线上。
A. 除去氯化钾晶体中的碳酸钾,应先 再 。
B. 除去生石灰中的碳酸钙,应 。
C. 除去铜粉中的氧化铜,应先 再 。
D. 除去碳酸钙中的碳酸钠,应先 再
三.计算题(11分)
12.某烃和乙烯组成的混合气体共0.1mol,完全燃烧后,在标准状况下得到3.36L二氧化碳和3.6g水.通过计算写出该烃的结构简式,并计算出该烃在混合气体中占的体积分数.
