人教版高一化学第一次月考(必修1)20##、9
本试卷分选择题和非选择题两部分,共100分。考试时间90分钟。
可能用到的相对原子质量 :H—1 C—12 O—16 N-14 Na---23 S—32 Mg---24
第 I 卷(选择题 共40分)
将1~20题答案填入下表中
一、选择题(每小题只有1个选项符合题意,每小题2分,共40分)
1、下列事故处理方法正确的是( )
A. 汽油失火时,立即用水灭火
B. 蒸发溶液时有液滴飞溅,应立即加水冷却
C. 浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液
D. 浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤
2.下列对于“摩尔”的理解正确的是 ( )
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔是物质的量的单位,简称摩,符号为mol
C.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
3.下列说法正确的是 ( )
A.摩尔质量就等于物质的式量 B.摩尔质量就是物质式量的6.02×1023倍 C.HNO3的摩尔质量是63g D.硫酸和磷酸的摩尔质量相等
4.现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ⑧氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是 ( )
A . 分液、蒸馏、萃取、 B. 萃取、蒸馏、分液
C . 分液、蒸馏、分液 D. 蒸馏、萃取、分液
5.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是 ( )
A . 化学不做实验,就什么都不知道 B . 化学不再需要实验
C. 化学不再是纯实验科学 D . 未来化学的方向是经验化
6.下列实验仪器不宜直接用来加热的是 ( )
A.试管 B.坩埚 C.蒸发皿 D.烧杯
7、0.25mol A的质量是16g,则A的相对分子质量(或相对分子质量)是
A.32g/mol B.64×10-3kg/mol C.32 D.64
8、为了除去粗盐中的Ca2+,Mg2+,SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序
①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液
A. ④②⑤ B.④①②⑤③
C. ②⑤④①③ D.①④②⑤③
9、下列实验操作中: ①过滤 ②蒸发 ③溶解 ④取液体试剂 ⑤取固体试剂.一定要用到玻璃棒的是
A.①②③ B.④⑤ C.①④ D.①③⑤
10、用NA表示阿伏加德罗常数,下列叙述正确的是
A. 64g SO2含有氧原子数为1NA
B. 物质的量浓度为0.5mol/L Mg Cl2溶液,含有Cl-离子数为1NA
C. 标准状况下,22.4L H2O的分子数为1NA
D. 常温常压下,14g N2含有分子数为0.5NA
11、在盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的( )

12、欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是
① 将14.2 g Na2SO4 溶于100ml水中
② 将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
③ 将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
A.①② B.②③ C.①③ D.①②③
13、将4g NaOH溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度是……………………………………………………………………………….( )
A.1mol/L B.0.1mol/L C.0.01mol/L D.10mol/L
14、配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是………( )
A.容量瓶中原有少量的蒸馏水 B.移液时,不慎将液体流到瓶外
C.容量瓶盛过KOH溶液,使用前未洗涤 D.定容时俯视刻度线和液面
15、今有0.1mol/LNa2SO4溶液300 mL,0.1mol/LMgSO4溶液200 mL和0.1mol/L Al2(SO4)3溶液100 mL,这三种溶液中硫酸根离子浓度之比是 ( )
(A)1∶1∶1 (B)3∶2∶2 (C) 3∶2∶3 (D) 1∶1∶3
16、某同学在实验报告中记录下列数据,其中正确的是( )
A.用25mL量筒量取12.36mL盐酸
B.用托盘天平称量8.75g食盐
C.用500mL的容量瓶配制450mL溶液
D.用广泛pH试纸测得某溶液的pH为3.5
17、下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
A.2.4 g金属镁变为镁离子时失去的电子数为0.1NA
B.1 mol HCl气体中的粒子数与0.5 mol/L盐酸中溶质粒子数相等
C.在标准状况下,22.4 L CH4与18 g H2O所含有电子数均为10NA
D.CO和N2为等电子体,22.4 L的CO气体与1 mol N2所含的电子数相等
18、已知Q与R的摩尔质量之比为9∶22,在反应X+2Y===2Q+R中,当1.6g X与Y完全反应后,生成4.4g R,则参与反应的Y和生成物Q的质量之比为( )
A.46∶9 B.32∶9
C.23∶9 D.16∶9
19、某非金属单质A和氧气发生化合反应生成B。B为气体,其体积是反应掉氧气体积的两倍(同温、同压)。以下对B的分子组成的推测一定正确的是( )
A.有1个氧原子 B.有2个氧原子
C.有1个A原子 D.有2个A原子
20、下列实验操作正确的是( )
A.制取蒸馏水时,为了防止瓶内产生暴沸现象,应先向烧瓶内加入几片碎瓷片
B.稀释浓硫酸时,常把水加入到盛浓硫酸的烧杯中
C.做CO还原Fe2O3实验时,为防止CO污染环境,实验完毕,常先停止通CO,再停止加热
D.在用水吸收HCl气体时可把导管直接插入液面下
第II卷(非选择题 共60分)
二、填空题(本题包括3小题,共29分)
21、(12分)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为________个。
(3)该气体在标准状况下的体积为________L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为________。设溶液的密度为ρg/cm3,则该溶液的物质的量浓度为__________mol·L-1。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为________mol·L-1。
22、(12分)(1)在标准状况下,4g H2,11.2L O2,1mol H2O中,所含分子数最多的是______,含原子数最多的是________,质量最大的是________,体积最小的是________。
(2)0.3 mol的氧气和0.2 mol的臭氧(O3),它们的质量________等,它们所含的分子数________等,原子数________等,它们的体积比(同温、同压)是________。
23、(5分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液法 B加热分解法 C结晶法 D分液法 E蒸馏法 F过滤法
(1)______分离饱和食盐水和沙子的混合物。
(2)______从硝酸钾和氯化钠的混合物中获得硝酸钾。
(3)______分离水和汽油的混合物。
(4)______分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
(5)______从碘的水溶液里提取碘。
三、实验题(本题包括2小题,共25分)
24、(14分)实验室欲配制0.5mol/L的NaOH溶液500ml有以下仪器:
①烧杯 ②100ml量筒 ③100ml容量瓶 ④500ml容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码)
(1)配制时,必须使用的仪器有___________(填代号),还缺少的仪器是_____ _____。该试验中两次用到玻璃棒,其作用分别是_______ ________,_________________。
(2)使用容量瓶前必须进行的一步操作是_____________________。
(3)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解④转移⑤洗涤⑥定容⑦冷却
其正确的操作顺序为____________________________。
(4)在配制过程中,其他操作都正确的,下列操作会引起误差偏高的是__________。
①没有洗涤烧杯和玻璃棒 ②未等NaOH溶液冷却至室温就转移到容量中
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视标线
⑤定容时仰视标线
25、(11分)海洋植物如海带.海藻中含有丰富的碘元素,其主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:(已知: 2I-+ Cl2=2Cl-+I2)
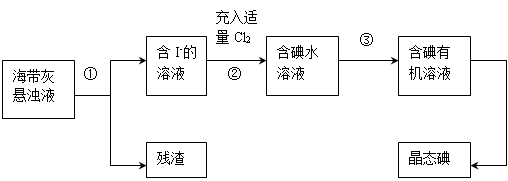
(1)指出提取碘的过程中有关的实验操作名称:① ,③ ;
(2)操作③中所用的有机试剂可以是 (只填一种),简述选择其理由 。
(3)操作过程③可以分解为如下几步:
A. 把盛有溶液的分液漏斗放在铁架台的铁圈中;
B. 把50ml碘水和15ml有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;
C. 检验分液漏斗活塞和上口的玻璃塞是否漏液;
D. 倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E. 旋开活塞,用烧杯接收溶液;
F. 从分液漏斗上口倒出上层液体;
G. 将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H. 静置、分层。
(a)过程③正确操作步骤的顺序是:(填编号字母) ;
(b)上述G步操作的目的是: ;
(c)最后碘的有机溶液是通过 获得(填“漏斗上口”或“漏斗下口”)。
四、计算(本题包括1小题 共6分)
26、常温下,将150mL 22% NaNO3溶液加100g蒸馏水后,溶液中溶质的质量分数变为14%。求原溶液的物质的量浓度。
高一化学第一次月考参考答案

21、(12分)(1)m/M(2)2mNA/M (3)22.4m/M(4)m/(m+1000) 1000mp/(1000+m)M (5)m/MV
22、(12分)(1)H2 H2 H2O H20 (2)、相 不相 相 3︰2
23、(5分)(1)F (2)C (3)D (4)E (5)A
24、(14分)(1)①④⑤⑥ 胶头滴管 加速溶解 引流
(2)检查是否漏夜 (3)②①③⑦④⑤⑥ (4)②④
25、(11分)(1)(2分)①过滤 ③萃取和分液
(2)(3分)CCl4 (1分);因为I2易溶于CCl4而难溶于水(1分),且CCl4与水又互不相溶,符合作萃取剂的条件(1分)
(3)(6分) (a) C B D A H G E F(错1个零分)(3分);
(b)保持分液漏斗内外压力平衡,使液体易于流下(2分) (c)漏斗下口(1分)
26、(6分)解:设原溶液质量为x, 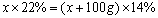
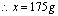
原来溶液的密度为:
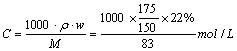 =
=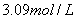
第二篇:高一化学必修1第一次月考题
高中2010—2011学年第一学期第一次月考试卷
高一化学(必修1)
本试卷共4页,满分100分。考试时间90分钟。
相对原子质量 H:1 C:12 N:14 O:16 Na:23 Mg:24 S:32 K:39 Cu:64 Cl:35.5
一、选择题(本题包括16个小题,每小题3分,共48分。每题只有一个选项符合题意)
1. 如果你家里的食用花生油混有水份,你将采用下列何种方法分离 ( )
A.过滤 B.蒸馏 C.分液 D.萃取
2.除去液体中的不溶性固体可用过滤的方法,该操作中不需要用到的仪器是 ( )
A.容量瓶 B.玻璃棒 C.烧杯 D.漏斗
3. 以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是 ( )
A. B. C. D.
4. 实验过程中下列操作正确的是 ( )
A. 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂
倒入试剂瓶中。
B. CuSO4溶于水,可将含有CuSO4的废液倒入水槽中,再用水冲入下水道。
C. 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干。
D. 用浓硫酸配置一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转
移到容量瓶中
5.下列实验操作中正确的是 ( )
A.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
B.蒸馏时,应使温度计水银球插入蒸馏烧瓶中液体的液面以下
C.可用酒精萃取碘水中的碘
D.称量时,称量物放在托盘天平的右盘,砝码放在托盘天平的左盘
6. 现有下列三种溶液:①45%的乙醇溶液 ②汽油和氯化钾溶液 ③氯化钠和单质碘的水溶
液,分离上述各组混合液的正确方法依次是 (




) 第 1 页 (共4页)
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、分液、萃取
7. 下列叙述正确的是 ( )
A. 摩尔是国际科学界建议采用的一种物理量
B. 任何物质的摩尔质量就等于它的相对分子质量或相对原子质量
C. 物质的量实质上是物质的质量
D. 1mol H2SO4中含有2mol H、1mol S和4mol O
8. 下列叙述正确的是 ( )
A. 1mol H2O的质量为18g/mol B. 3.01ⅹ1023个SO2分子的质量为32g
C.CH4的摩尔质量为16g D. 标准状况下,1mol任何物质体积均为22.4L
9. 设NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A. 标准状况下,11.2 L H2O含有的分子数为0.5NA
B. 常温常压下,1.06g Na2CO3含有Na+数目为0.02NA
C. 通常状况下,1NA个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA
10. 在0.5molK2SO4中含有K+的数目是 个 ( )
A.6.02ⅹ1023 B.0.5 C. 3.01ⅹ1023 D. 1
11. 科学家已发现一种新型氢分子,其化学是为H3,在同温同压下,等质量的H3和H2具 有相同的 ( )
A. 原子数 B. 分子数 C. 体积 D. 物质的量
12.实验室要配制0.5mol/L硫酸溶液500mL,需要用10mol/L的硫酸溶液的体积是( )
A.25 B.25L C.25mL D.50mL
13.所含分子数相同的一组物质是 ( )
A.1g H2和1g N2 B.1molH2O和1gH2O
C.3.2gO2和2.24L的空气(标准状况下) D.44gCO2和6.02×1022个O2
14. 0.5L 1mol/LFeCl3溶液与0.2L 1mol/L KCl溶液中的Cl-的数目之比为 ( )
A. 5:2 B. 3:1 C. 15:2 D. 1:3
15. 已知1.505ⅹ1023个X气体分子的质量为8g ,则X气体的摩尔质量为 ( )
A. 16g B. 64g/mol C. 32g D. 32g/mol
16. 欲配制100mL 1mol/LNa2SO4溶液,正确的方法是 ( ) 第 2 页 (共4页)
①将14.2g Na2SO4溶于100mL水中
②将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100mL
③将20mL5mol/L Na2SO4溶液用水稀释至100mL
A. ①② B. ②③ C. ①③ D. ①②③
二、填空题:
17.(共10分)
对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、加热分解等。 下列各组混合物的分离或提纯应采用什么方法?请填空:
⑴ 实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可采用 的方法除
去Ca(OH)2溶液中悬浮的CaCO3微粒。
⑵ 提取碘水中的碘,用
⑶ 除去食盐溶液中的水,可采用
⑷ 淡化海水得饮用水,可采用
⑸ 除去氧化钙中的碳酸钙可用 的方法
18.(共20分)
⑴ 计算0.5mol CO2的质量是 ,约含有 个CO2分子; 计算1.204×1024个H2O分子的物质的量是,质量是 ⑵ 100 mL 5mol/LNa2CO3溶液中所含Na2CO3的物质的量是 。
⑶ 1mol H2SO4中含 mol硫原子, 个氢原子。
⑷ 计算在标准状况下2mol NH3的体积是 ;在标准状况下,某气体的密度
是1.429g·L-1,则该气体的摩尔质量是 ,在相同条件下,该气体是 H2密度的 倍。
19.(共10分)
用氯化钠固体配制1.00mol/L的NaCl溶液500mL,有如下操作步骤;
①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解。
②把①所得溶液小心转入500mL容量瓶中。
③继续向容量瓶中加蒸馏水至液面距刻度线1㎝~2㎝处,改用胶头滴管小心滴加蒸馏水
至溶液凹液面与刻度线相切。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并摇匀。 ⑤将容量瓶瓶塞塞紧,充分摇匀。
第 3 页 (共4页)
⑥计算、称量NaCl的质量。
请填写下列空白:
⑴操作步骤的正确顺序为(填序号) ⑵ 所需仪器为:
除托盘天平外,还用到 ; 使用容量瓶前必须进行的操作是。
⑶ 试分析下列操作对所配溶液的浓度有何影响。(填“偏高”“偏低”或“无影响”)
a. 为加速固体溶解,可稍微加热并不断搅拌。在未降至室温时,立即将溶液转移至容
量瓶定容。对所配溶液浓度的影响: 。
b. 定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶
液浓度的影响: 。
c. 定容时俯视液面,对所配溶液浓度将有何影响: ⑷ 某同学从该溶液中取出50mL,其中NaCl的物质的量浓度为
三、简答题(共12分)
20.(4分)实验室欲配制100mL 0.5mol/LNaOH溶液需要称取NaOH的质量是多少?
21.(4分) 游泳池里的水常加入适量的CuSO4用来杀灭其中的细菌,而对游泳者的身体无
害。现取一水样300mL,经分析其中含有0.0192gCu2+,则水样中CuSO4的物质的量浓 度是多少?
22.(4分) 右图为某市售硫酸试剂瓶标签上部分数据。
问该硫酸的物质的量浓度为多少?

第 4 页 (共4页)
