第三单元 自然界的水
课题1 水的组成
一、水的组成
1、水的组成:
(1)电解水的实验
A.装置―――水电解器
B.电源种类---直流电
C.加入硫酸或氢氧化钠的目的----增强水的导电性
D.化学反应:文字表达式::水(H2O) 氢气(H2) + 氧气(O2)
氢气(H2) + 氧气(O2)
 化学方程式:2H
2O
化学方程式:2H
2O
 2H
2↑+ O
2↑
2H
2↑+ O
2↑
产生位置 负极 正极
体积比 2 : 1
质量比 1 : 8
E.检验:O2---出气口置一根带火星的木条----木条复燃
H2---出气口置一根燃着的木条------气体燃烧,发出淡蓝色的火焰
(2)结论: ①水是由氢、氧元素组成的。
②化学变化中,分子可分而原子不可分。
2、水的性质
物理性质:无色无味的液体、40C时密度最大,为1g/cm3
化学性质:通电分解
文字表达式:水(H2O) 氢气(H2) + 氧气(O2)
氢气(H2) + 氧气(O2)
化学方程式: 2H2O  2H2↑+O2↑
2H2↑+O2↑
3、氢气
1、物理性质:密度最小的气体(向下排空气法)(氢气与其它气体的显著区别之处);难溶于水(排水法)、无色无臭的气体
证明氢气密度比空气小的方法:用氢气吹肥皂泡,若肥皂泡上升,则密度比空气小
2、化学性质:
可燃性(用途:高能燃料;氢氧焰焊接,切割金属)
文字表达式:氢气(H2) + 氧气(O2)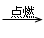 水(H2O)
水(H2O)
化学方程式:2H2 + O2  2H2O 点燃前,要验纯
2H2O 点燃前,要验纯
现象:发出淡蓝色火焰,放出热量,有水珠产生
注意:混有一定量的空气或氧气的氢气遇明火会发生爆炸,因此点燃前必须验纯。
二、物质的分类
1、概念
单质:由同种元素组成的纯净物 例:氢气、氧气、红磷等
化合物:由不同种元素组成的纯净物 例:水、高锰酸钾等
氧化物:由两种元素组成,且含有氧元素的纯净物 例:二氧化硫、氧化铁等
注意:单质、化合物前提必须是纯净物,即划分单质、化合物的标准是根据纯净物的元素种类来划分的。若只含一种元素的纯净物就属于单质;若含有几种元素的纯净物就属于化合物
2、物质分类的步骤
①根据物质种类分为纯净物与混合物
②写出纯净物的化学符号
③根据元素种类将纯净物分为单质与化合物
④在化合物中根据氧化物的概念找出氧化物
课题2 分子和原子
一、构成物质的微粒:分子、原子等微粒
1、由分子构成的物质:例如水、二氧化碳、氢气、氧气等物质
2、由原子构成的物质:金属、稀有气体、金刚石、石墨等物质
3、物质构成的描述:物质由××分子(或原子)构成。例如:铁由铁原子构成;氧气由氧分子构成。
二、分子
1、基本性质:⑴质量、体积都很小;
⑵在不停地运动且与温度有关。温度越高,运动速率越快 例:水的挥发、品红的扩散;
⑶分子间存在间隔。同一物质气态时分子间隔最大,固体时分子间隔最小 ;物体的热胀冷缩现象就是分子间的间隔受热时增大,遇冷时变小的缘故。
⑷同种物质间分子的性质相同,不同物质间分子的性质不同。
2、分子的构成:分子由原子构成。
分子构成的描述:①××分子由××原子和××原子构成。
例如:水分子由氢原子和氧原子构成
②一个××分子由几个××原子和几个××原子构成。
例如:一个水分子由一个氧原子和二个氢原子构成
3、含义:分子是保持物质化学性质的最小微粒。
例:氢分子是保持氢气化学性质的最小粒子
4、从分子和原子角度来区别下列几组概念
⑴物理变化与化学变化
由分子构成的物质,发生物理变化时,分子种类不变。
发生化学变化时,分子种类发生了改变。
⑵纯净物与混合物
由分子构成的物质,纯净物由同种分子构成;混合物由不同种分子构成。
⑶单质与化合物
单质的分子由同种原子构成;化合物的分子由不同种原子构成。
三、原子
1、含义:原子是化学变化中最小的微粒。例:氢原子、氧原子是电解水中的最小粒子
2、分子与原子的比较

3、化学反应的实质:在化学反应中分子分裂为原子,原子重新组合成新的分子。
课题3 水的净化
一、净化水的方法:沉淀、过滤、吸附、蒸馏
1、沉淀(吸附沉淀):试剂:明矾
净水原理:利用明矾溶于水形成的胶状物对水的杂质进行吸附,从而达到净化的目的。
2、过滤 ①适用范围:用于分离难溶性固体与液体(或可溶性固体)
②操作注意事项:“一贴二低三靠”
“一贴”:滤纸紧贴漏斗的内壁
“二低”:(1)滤纸的边缘低于漏斗口 (2)漏斗内的液面低于滤纸的边缘
“三靠”:(1)漏斗下端的管口紧靠烧杯内壁
(2)用玻璃棒引流时,玻璃棒下端轻靠在三层滤纸的一边
(3)用玻璃棒引流时,烧杯尖嘴紧靠玻璃棒中部
③仪器:铁架台、烧杯、玻璃棒、漏斗 玻璃棒的作用:引流作用
④过滤后,滤液仍然浑浊的可能原因有:
A承接滤液的烧杯不干净 B倾倒液体时液面高于滤纸边缘 C滤纸破损
3、吸附 常用的吸附剂:活性炭(具有吸附性):除去水的难溶性杂质、色素和异味。
4、蒸馏:利用液体沸点不同将液体分离的方法
蒸馏的装置:见书P57,图3-21和3-22
各种静化方法除去的杂质的种类

二、硬水与软水1、定义 硬水是含有较多可溶性钙、镁化合物的水;例:井水
软水是不含或含较少可溶性钙、镁化合物的水。例:开水
2.鉴别方法:用肥皂水,有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水
3.硬水软化的方法:蒸馏、煮沸
4.长期使用硬水的坏处:浪费肥皂,洗不干净衣服;锅炉容易结成水垢,不仅浪费燃料,还易使管道变形甚至引起锅炉爆炸。
水的净化效果由低到高的是 沉淀、过滤、吸附、蒸馏(均为 物理 方法),其中净化效果最好的操作是 蒸馏;既有过滤作用又有吸附作用的净水剂是活性炭。
课题4 水资源的保护
一、水资源
1、地球表面71%被水覆盖,但供人类利用的淡水小于 1%
2、海洋是地球上最大的储水库。海水中含有80多种元素。海水中含量最多的物质是 H2O,最多的金属元素是 Na ,最多的元素是 O 。
3、我国水资源的状况分布不均,人均量少
二、爱护水资源:节约用水,防止水体污染
1、节约用水即提高水的利用率。生活中提倡一水多用,使用节水型器具;
农业中改大水漫灌为喷灌、滴灌;
工业中提倡对水重复利用,循环使用
2、水污染
A、水污染物:工业“三废”(废渣、废液、废气);农药、化肥的不合理施用
生活垃圾、生活污水的任意排放
B、防止水污染:工业三废要经处理达标排放、提倡零排放;生活污水要集中处理达标排放、提倡零排放;合理施用农药、化肥,提倡使用农家肥;加强水质监测。
拓展性课题 氢气(H2)
1、物理性质:密度最小的气体(向下排空气法)(氢气与其它气体的显著区别之处);难溶于水(排水法)、无色无臭的气体
证明氢气密度比空气小的方法:用氢气吹肥皂泡,若肥皂泡上升,则密度比空气小
2、化学性质:
(1) 可燃性(用途:高能燃料;氢氧焰焊接,切割金属)
文字表达式:氢气(H2) + 氧气(O2) 水(H2O)
水(H2O)
化学方程式:2H2 + O2  2H2O 点燃前,要验纯
2H2O 点燃前,要验纯
现象:发出淡蓝色火焰,放出热量,有水珠产生
注意:任何可燃性气体或可燃性的粉尘如果跟空气充分混合,遇火时都有可能发生爆炸。因此当可燃性气体发生泄漏时,应杜绝一切火源、火星,以防发生爆炸。应立即打开门窗、关闭阀门。
(2) 还原性(用途:冶炼金属)
 文字表达式:氢气 + 氧化铜
文字表达式:氢气 + 氧化铜 铜 + 水
铜 + 水
化学方程式:H2 + CuO Cu + H2O 氢气“早出晚归”
现象:黑色粉末变红色,试管口有水珠生成
(小结:既有可燃性,又有还原性的物质 H2、C、CO)
3、氢能源 三大优点:产物无污染、放热量高、以水制取氢气来源广
不能推广使用的原因:制取氢气的成本太高,氢气的储存和运输比较困难
四、物质的组成、构成及分类
 组成:物质(纯净物)由元素组成
组成:物质(纯净物)由元素组成
 原子:金属、稀有气体、碳、硅等。
原子:金属、稀有气体、碳、硅等。
物质 构成 分子:如氯化氢由氯化氢分子构成。 H2、O2、N2、Cl2。
离子:NaCl等离子化合物,如氯化钠由钠离子(Na+)氯离子(Cl-)构成
 混合物(多种物质)
混合物(多种物质)
 分类 单质 :金属、非金属、稀有气体
分类 单质 :金属、非金属、稀有气体
纯净物 (一种元素)
 (一种物质)化合物: 有机化合物 CH4、C2H5OH、C6H12O6、淀粉、蛋白质 (多种元素) 氧化物 H2O CuO CO2
(一种物质)化合物: 有机化合物 CH4、C2H5OH、C6H12O6、淀粉、蛋白质 (多种元素) 氧化物 H2O CuO CO2
酸 HCl H2SO4 HNO3
 无机化合物 碱 NaOH Ca(OH)2 KOH
无机化合物 碱 NaOH Ca(OH)2 KOH
第二篇:人教版初三化学第五章知识点总结
第五单元 化学方程式
课题1 质量守恒定律
一、质量守恒定律
1、含义: 说明:①质量守恒定律只适用于化学变化,不适用于物理变化; ........
②没有参加反应的物质质量及不是反应生成的物质质量不能计入“总和”中; .. ③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏。
2、微观解释:在化学反应前后,原子的种类、数目、质量均保持不变(原子的“三不变”)。 3、化学反应前后
(1)一定不变宏观:反应物、生成物的总质量不变;元素种类、质量不变
微观:原子的种类、数目、质量不变
(2)一定改变宏观:物质的种类一定变
微观:分子种类一定变
(3)可能改变:分子总数可能变 二、化学方程式
1、含义:用化学式表示化学反应的式子。能直接反映质量守恒定律。 2、表示的意义:⑴表示反应物、生成物和反应条件
⑵表示各物质间的质量比(质量比=各物质的相对分子质量×各化学式前面的系数的积的比)
⑶表示各物质的微粒个数比(即各化学式前面的系数比) 点燃 例如:以2H2+O22O为例
①表示氢气与氧气在点燃条件下生成水 ②表示氢气、氧气与水的质量比为4:32:36 ③表示氢分子、氧分子与水分子的个数比为2:1:2 点燃 3、化学方程式的读法 以2H2+O22O为例
①从反应物、生成物和反应条件角度:氢气与氧气在点燃条件下生成水
②从各物质的质量比角度:每4份质量的氢气与32份质量的氧气在点燃条件下生成36份质量的水
③从各物质的微粒个数比角度:每2个氢分子与1个氧分子在点燃条件下生成2个水分子。
课题2 如何正确书写化学方程式
一、书写原则:
1、以客观事实为基础 2、遵守质量守恒定律(标准:两边原子的种类和数目相等) 二、方程式的配平
1、标准:方程式两边原子种类和数目相等即配平了
2、配平的原则:在化学式前面加上适当的系数来保证方程式两边原子种类和数目相等。 3、方法:最小公倍数法
最小公倍数法配平化学方程式的步骤
⑴、确定配平的起点元素:横线两边出现次数最少,且原子个数的最小公倍数最大的元素作为起点元素。
⑵、确定起点元素原子个数的最小公倍数。
⑶、确定含有起点元素的化学式的系数:用最小公倍数除以化学式中起点元素原子的个数的商作为该化学式前面的系数。
⑷、确定其它化学式前面的系数的顺序:依次确定含有除起点元素以外,横线两边出现次数由少到多的元素的化学式前面的系数。 ⑸、最后将各系数调整为最简整数比。
举例:配平化学方程式: FeS2 + O2 点燃 Fe2O3 + SO2
⑴确定起点元素:由于Fe、S 元素在横线两边只出现了一次,且最小公倍数都为2,因此Fe、S元素都可作为起点元素。
⑵若选择Fe作为起点元素,则原子个数的最小公倍数为2。
⑶确定FeS2 、SO2前面的系数:用最小公倍数2除以FeS2中Fe元素的原子个数1的商2作为的FeS2系数;用最小公倍数2除以Fe2O3中Fe元素的原子个数2的商1作为Fe2O3的系数;
2FeS2 + O2 点燃 1Fe2O3 + SO2
⑷确定O2 、SO2的系数:
①由于O2 、SO2中只含有O、S两种元素,S元素在方程式两边只出现了一次,因此先确定SO2 的系数,再确定O2的系数。由于方程式左边S原子的个数已确定为4,所以右边S原子的个数也为4。因此SO2的系数为4除以SO2中S元素的原子个数1的商4作为SO2。的系数。
2FeS2 + O2 点燃 1Fe2O3 + 4SO2
②由于方程式右边O原子的个数已确定为11,因此左边O原子的个数也为11。所以O2的系数为11除以O2中O元素的原子个数2的商11/2作为SO2。的系数。
2FeS2 + 11/2O2 点燃 1Fe2O3 + 4SO2
⑸再将各系数调整为最简整数比:即在方程式两边同时乘以2就可以。
点燃
4FeS2 + 11O2 2Fe2O3 + 8SO2
一、书写的步骤
1、写 写出反应物、生成物的化学式 2、配 配平方程式 3、注 注明反应条件和生成物的状态 4、等 将横线改为等号
课题3 利用化学方程式的简单计算
一、依据:利用化学方程式能反映物质间的质量比,且质量比呈正比例关系。
二、步骤:①设未知数;②根据题意写出方程式;③根据化学方程式找出已知量与未知量的质量比;④列出比例式,并求出未知数;⑤答 注意:
①由于方程式只能反应物质间的质量比,因此代入方程式中的各个量必须是质量。 ②由于方程式中各物质是纯净物,因此代入方程式中的量必须是纯净物的质量。 ③单位必须统一。
附:前面一至五单元要求掌握的化学方程式:
C + O2 点燃
CO2 S + O2
点燃
SO2
4P + 5O2 3Fe + 2O2
2H2O2 2KClO3
△
点燃
2P2O5 4Al + 3O2 Fe3O4 2Mg + O2
点燃
2Al2O3 2MgO
点燃
点燃
2H2O + O2↑ 2KMnO42KCl+3O2↑ 2H2O
△
K2MnO4 + MnO2 + O2↑
MnO
通电
2H2↑+ O2↑
点燃
2H2 + O22O
