常考实验总结
化学实验在高考题的比重是越来越大,目前高考实验命题的特点有二:一是突出考查实验的基础知识和基本操作能力,二是突出考查实验探究能力,这一点在考试大纲中已有明确要求。课本实验往往成为考查学生实验探究能力命题的载体。
一、配制一定物质的量浓度的溶液:(见二轮专题75页)
【补充】
1、 所用主要仪器:(由步骤写仪器)托盘天平、烧杯、玻璃棒、(量筒)、500mL容量瓶、胶头滴管
2、 注意事项:
(1)常见的容量瓶:50 mL、100mL、250mL、500mL、1000mL。若配制480mL与240mL溶液,应分别用500mL容量瓶和250mL容量瓶。
(2)容量瓶查漏方法:向容量瓶内加少量水,塞好瓶塞,用食指顶住瓶塞,用另一只手的五指托住瓶底,把瓶倒立过来,如不漏水,正立,把瓶塞旋转1800后塞紧,再倒立若不漏水,方可使用。
【命题角度】一是计算所需的固体和液体的量,二是仪器缺失与选择,三是误差分析。
二、Fe(OH)3胶体的制备:
1、步骤:向沸水中加入FeCl3的饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
【操作要点】①先煮沸,②加入饱和的FeCl3溶液,③再煮沸至红褐色,④停止加热
2、涉及的化学方程式:Fe3++3H2O =Fe(OH)3(胶体)+3H+
【强调】之一是用等号,之二是标明胶体而不是沉淀,之三是加热。
【命题角度】配制步骤及对应离子方程式的书写
 三、焰色反应:
三、焰色反应:
1、步骤:洗—烧—蘸—烧—洗—烧
2 、该实验用铂丝或铁丝
3 、焰色反应是金属元素的性质,可以是单质,也可以是化合物,是物理性质
4 、Na ,K 的焰色:黄色,紫色(透过蓝色的钴玻璃)
5 、某物质作焰色反应,有黄色火焰一定有Na ,可能有K
6、用盐酸洗铂丝或铁丝。
【命题角度】实验操作步骤及Na ,K 的焰色
四、Fe(OH)2的制备:
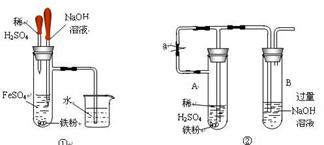
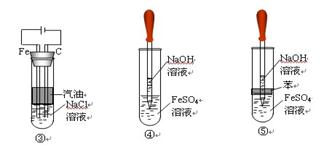
1、实验现象:白色沉淀立即转化灰绿色,最后变成红褐色沉淀。
2、化学方程式为:Fe2++2OH-=Fe(OH)2 ↓ 4Fe(OH)2+O2+2H2O= 4Fe(OH)3
3、注意事项:(1)所用亚铁盐溶液必须是新制的,NaOH溶液必须煮沸。
(2)胶头滴管须插入液以下。
(3)往往在液面加一层油膜,如苯或食物油等(以防止氧气的氧化)。
【命题角度】制备过程中的现象、方程式书写及有关采取措施的原因
五、硅酸的制备:
1、步骤:在试管中加入3—5mL饱和Na2SiO3溶液,滴入1—2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边加边振荡,至溶液颜色变浅并接近消失时停止。
2、现象:有透明的硅酸凝胶形成
3、化学方程式:NaSiO3+2HCl= H2SiO3(胶体)+2NaCl(强酸制弱酸)
4、 NaSiO3溶液由于SiO32-水解而显碱性,从而使酚酞试液呈红色。
六、重要离子的检验: (见二轮专题63页)
【命题角度】检验方法、除杂、沉淀洗涤及相关纯度的计算
七、重要气体的检验: (见二轮专题63页)
八、常见的除杂: (见二轮专题64页)
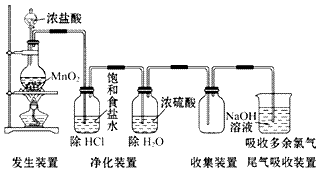
九、氯气的实验室制法(见二轮专题73页)
 【补充】
【补充】
1、氯气的实验室制法的离子方程式:
2、尾气吸收:常用 吸收,反应的化学方程式为 ,
离子方程式为 。
十、氨气的实验室制法 (见二轮专题72页)
【补充】
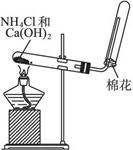 1、检验:方法一
1、检验:方法一
方法二
2、制取氨气的其他可行方法:
①
②
③
【命题角度】因氨气作为中学化学实验制取气体中唯一的实验,其地位不可估量。主要角度为:反应原理、收集、干燥及验满等,并以此基础进行性质探究实验。
十一、喷泉实验(见二轮专题76页)
十二、铜与浓硫酸反应的实验

1、实验原理:
2、现象:
3、如何检验产物?
【提示】由于此反应快,利用铜丝,便于及时抽出,减少污染。
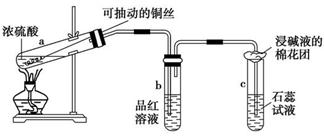

【命题角度】SO2的性质及产物的探究、“绿色化学”及尾气的处理等。
 十三、铝热反应(见二轮专题76页)
十三、铝热反应(见二轮专题76页)
【补充】
1、实验操作步骤:把少量干燥的氧化铁和适量的铝粉均匀混合后放在纸漏斗中,在混合物上面加少量氯酸钾固体中,中间插一根用砂纸打磨过的镁条,点燃。
2、实验现象:立即剧烈反应,发出耀眼的光芒,产生大量的烟,纸漏斗被烧破,有红热状态的液珠,落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
3、注意事项:
(1)要用打磨净的镁条表面的氧化膜,否则难以点燃。
(2)玻璃漏斗内的纸漏斗要厚一些,并用水润湿,以防损坏漏斗
(3)蒸发皿要垫适量的细沙:一是防止蒸发皿炸裂,二是防止熔融的液体溅出伤人。
 (4)实验装置不要距人太近,防止使人受伤。
(4)实验装置不要距人太近,防止使人受伤。
【命题角度】实验操作步骤及化学方程式。
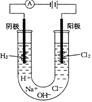
十四、氯碱工业 (用惰性电极电解饱和食盐水)
【命题角度】两极上析出产物的判断、产物的性质及相关电解原理
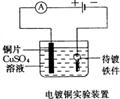 十五、粗铜的精炼、电镀铜(见二轮专题21-22页)
十五、粗铜的精炼、电镀铜(见二轮专题21-22页)
1、粗铜的精炼:电解质溶液:CuSO4溶液
阳极材料:粗铜 阳极反应式:Cu-2 e-= Cu2+(主要)
阴极材料:纯铜 阴极反应式:Cu2+ +2 e-= Cu
问题的解释:铜属于活性电极,电解时阳极材料发生氧化反应而溶解。粗铜中含有Zn、Ni、Fe、Ag、Au等多种杂质,当含有杂质的铜在阳极不断溶解时,位于金属活动性顺序表铜以前的金属杂质,如Zn、Ni、Fe、等也会同时失去电子,但它们的阳离子得电子能力比铜离子弱,难以被还原,所以并不能在阴极上得电子析出,而只能留在电解液里,位于金属活动性表铜之后的银、金等杂质,因失去电子的能力比铜更弱,难以在阳极失去电子变成阳离子溶解,所以以金属单质的形式沉积在电解槽底,形成阳极泥(阳极泥可作为提炼金、银等贵重金属的原料)。
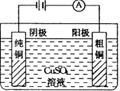 2、铁上镀铜:电解质溶液:CuSO4溶液
2、铁上镀铜:电解质溶液:CuSO4溶液
阳极材料:铜 阳极反应式:Cu-2 e-= Cu2+
阴极材料:铁 阴极反应式:Cu2+ +2 e-= Cu
(1)电镀的原理:与电解原理相同。电镀时,一般用含有镀层金属阳离子的电解质溶液作电镀液,把待镀金属制品浸入电镀液中,与直流电源的负极相连,作阴极;用镀层金属作阳极,与直流电源的正极相连,阳极金属溶解,成为阳离子,移向阴极,这些离子在阴极上得电子被还原成金属,覆盖在镀件的表面。
(2)电镀池的组成:待镀金属制品作阴极,镀层金属作阳极,含有镀层金属离子的溶液作电镀液,阳极反应:M – ne- =Mn+(进入溶液),阴极反应Mn+ + ne- =M(在镀件上沉积金属)
十六、卤代烃中卤原子的检验方法(取代反应、消去反应):
【知识铺垫】溴乙烷的水解反应(或取代反应)
溴乙烷的消去反应
检验产物:卤离子
1、实验步骤:(以溴乙烷为例)
。
2、若为白色沉淀,卤原子为氯;若浅黄色沉淀,为溴;若黄色沉淀,为碘。
 3、加入硝酸银溶液之前,须加入硝酸酸化中和掉混合液中的碱液方可。
3、加入硝酸银溶液之前,须加入硝酸酸化中和掉混合液中的碱液方可。
检验产物:乙烯:
用酸性KMnO4溶液验证消去反应产物乙烯时,要注意先通入水中除去乙醇,再通入酸性KMnO4溶液中;也可用溴水直接检验(则不用先通入水中)。
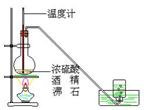 十七、乙烯的实验室制法(见二轮专题73页)
十七、乙烯的实验室制法(见二轮专题73页)
【补充】
(1)反应主要仪器
(2)反应类型
【注意事项】
①乙醇和浓硫酸的体积比为1:3
②向乙醇中注入浓硫酸;边慢注入,边搅拌
③反应温度要迅速升高到170℃
④实验中会产生副产物SO2, 故检验乙烯时,一定先用碱液除去SO2,再通入KMnO4或溴水
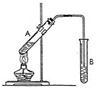 十八、乙酸乙酯的制备 (见二轮专题74页)
十八、乙酸乙酯的制备 (见二轮专题74页)
【补充】【注意事项】
1、先加乙醇,再加浓硫酸和乙酸的混合液;
2、低温加热小心均匀的进行,以防乙酸、乙醇的大量挥发和液体剧烈沸腾;
【命题角度】加入药品顺序、导管的位置、饱和Na2CO3溶液的作用及考查运用化学平衡提高乙酸乙酯转化率的措施。
十九、醛基的检验(以乙醛为例):
1、“银镜反应”:(反应类型 )
化学方程式
实验操作
【注意】
(1)实验后附着银镜的试管可用 浸泡,再用水洗而除去。
(2)该实验在工业上也可用来 或制 。
2、与新制Cu(OH)2 反应:(反应类型 )
化学方程式
实验操作
【注意】新制Cu(OH)2 悬浊液时要保证NaOH溶液过量。
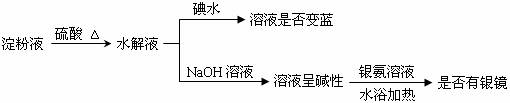 二十、淀粉(或蔗糖)水解及产物的验证:
二十、淀粉(或蔗糖)水解及产物的验证:
【注意】检验产物的还原性之前要先加碱液中和硫酸
第二篇:跨专业综合实验实训个人总结
跨专业综合实验实训个人总结
光阴似箭韶华易逝,短短15天的小学期实训画上了圆满的句号。在这15天里,我受益匪浅,收获多多。
读万卷书不如行万里路,纸上谈兵不如亲自实践,身体力行。仅仅知道了解书本上的会计知识是远远不够的,不进行实务操作就根本不知道自己是否真正掌握这些知识,而这次为期7天的财务会计手工实训和为期8天的VBSE为我们动手实际操作能力的提高提供了契机。通过会计实训,我较系统地练习企业会计核算的基本程序和具体方法,加强对所学专业理论知识的理解、增强实际操作的动手能力,提高运用会计基本技能的水平,也是对所学专业知识的一个检验;使我掌握填制和审核原始凭证与记账凭证,登记账薄的会计工作技能和方法,而且能够切身的体会出纳员、材料核算员、记账员等会计工作岗位的具体工作,从而对所学理论有一个较系统、完整的认识,最终达到会计理论与会计实践相结合的目的。
然而,该实训项目仍存在一些不足:首先,实验实训系统平台存在的不足。系统页面有时候会卡住,需要重新登录页面就会显得麻烦;业务流程描述有时候不是特别详细准确为我们正确理解业务流程、快速完成任务带来不便;其次,实验实训中涉及的单据、票据、账簿、报表在格式上存在需要完善的环节。我们领用的票据很多都没有派上用场并且任务上也没有明确要求需要用到但又必须得填写而有些票据却不够或者在格式上需要重新更改;再次,实验实训组织管理存在不足,抢答环节老师无法准确知道哪组同学先举手,不能保证评分的
绝对公平,老师们应该统一一下对各种可能出现问题的解决办法而不是各说其词(就比如实训中对于数字的确定一人说保留整数一人说保留两位小数或者其他的);最后本人存在不足之处,首先自己的会计专业不扎实,不能将所学知识应用到实际操作中,由一个任务不能马上知道做该任务的思路方法所以不能保质保量完成任务;其次实操能力弱,对业务流程不了解;最后,我的耐心也不足,没有认真看相关业务流程就开始做,忽略了重要细节,出现问题就变得急躁,这脾气要改改。然而值得高兴的是随着实习的进行,我的各项能力一点一点得到提高。
财务会计手工实验与本次跨专业综合实验实训都是将会计专业知识应用到具体实际中,要求团队之间的友好协作。财务会计手工实验比较注重手工操作及对会计基础知识的理解掌握;而跨专业综合实验实训主要注重会计信息化操作,不仅要求掌握会计基础知识,也要求熟练应用成本会计、财务会计等知识,注重要求对会计综合知识的理解掌握。信息化实训能够方便会计资料的传递,明确人员分工跟责任,防止弄虚作假,可以随时查看每个岗位人员的工作进度,以便企业管理。所以我个人认为综合实验实训更能检验一个会计专业人员的知识水平及掌握能力,激励学生加强学习专业知识,增强职业能力,努力成为一名合格的会计人员。
这次跨专业综合实验实训从总体上说是比较令人满意的,增强了我们的实操能力,巩固了我们所学的专业知识,但仍存在一些小瑕疵。工作分配不合理,有些人任务多且重,而有些人很悠闲任务轻或者某
天任务特别多压得人忙不过来但有时却没什么任务特别无聊。分组不合理,我们组全是转到会计专业的,每个人至少都有一门考试,所以进度比较慢。当然这也与我们是否熟练掌握专业知识有很大的关系。通过15天的实训,我明白了只有把专业知识学得更加扎实牢固,才能将工作完成得又快又好;我知道了作为一名会计人员要有细心、耐心、更重要的是责任心,为了成为一名合格的专业会计人员,我会更加的努力,不断完善自己,超越自己!
