钠元素单质及其化合物

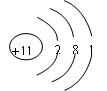 (1)钠的物理性质:钠是银白色金属,密度小(0.97g/cm3),熔点低(97℃),硬度小,质软,可用刀切割。钠通常保存在煤油中。是电和热的良导体。
(1)钠的物理性质:钠是银白色金属,密度小(0.97g/cm3),熔点低(97℃),硬度小,质软,可用刀切割。钠通常保存在煤油中。是电和热的良导体。
(2)钠的化学性质:从原子结构可知钠是活泼的金属单质。
①钠与非金属单质反应:常温:4Na + O2 == 2Na2O,加热:2Na + O2  Na2O2;
Na2O2;
2Na + Cl2  2NaCl; 2Na + S
2NaCl; 2Na + S  Na2S等。
Na2S等。
②钠与水反应:2Na + 2H2O == 2NaOH + H2↑;实验现象:钠浮在水面上,熔成小球,
在水面上游动,有哧哧的声音,最后消失,在反应后的溶液中滴加酚酞,溶液变红
注意:钠在空气中的变化:银白色的钠 变暗(生成了氧化钠)
变暗(生成了氧化钠) 变白(生成氢氧化钠)
变白(生成氢氧化钠) 潮解
潮解 变成白色固体(生成碳酸钠)。常温下金属钠在空气中表面变暗,生成氧化膜,说明钠比Al、Fe活泼得多
变成白色固体(生成碳酸钠)。常温下金属钠在空气中表面变暗,生成氧化膜,说明钠比Al、Fe活泼得多
(应用)钠保存在石蜡油或煤油中,因为钠易与水或者空气中的氧气反应,而钠不与煤油反应,且钠的密度大于煤油的密度,所以保存在煤油中
③钠与酸反应:如2Na + 2HCl == 2NaCl + H2↑,Na放入稀盐酸中,是先与酸反应,酸不足再与水反应。因此Na放入到酸中Na是不可能过量的。同时Na与H2的物质的量比始终是2:1。当然反应要比钠与水的反应剧烈多。
④钠与盐的溶液反应:钠不能置换出溶液中的金属,钠是直接与水反应。反应后的碱再与溶液中的其他物质反应。如钠投入到硫酸铜溶液的反应式:2Na + CuSO4 + 2H2O == Cu(OH)2 ↓+ Na2SO4 + H2 ↑。
⑤钠与氢气的反应:2Na + H2 == 2NaH。NaH + H2O == NaOH + H2 ;NaH是强的还原剂。
(3)工业制钠:电解熔融的NaCl,2NaCl(熔融)  2Na + Cl2↑。
2Na + Cl2↑。
(4)钠的用途:①在熔融的条件下钠可以制取一些金属,如钛、锆、铌、钽等;
②钠钾合金是快中子反应堆的热交换剂;
③钠蒸气可作高压钠灯,发出黄光,射程远,透雾能力强。
2、氧化钠和过氧化钠
(1)Na2O:白色固体,是碱性氧化物,具有碱性氧化物的通性:Na2O + H2O == 2NaOH,Na2O + CO2 == Na2CO3,Na2O + 2HCl == 2NaCl + H2O .另外:加热时,2Na2O + O2 == 2Na2O2.
(2)Na2O2:淡黄色固体是复杂氧化物,易与水和二氧化碳反应。
2Na2O2 + 2H2O == 4NaOH + O2 ,2Na2O2 + 2CO2 == 2Na2CO3 + O2 (作供氧剂)。
因此Na2O2常做生氧剂,同时,Na2O2还具有强氧化性,有漂白作用。如实验:Na2O2和水反应后的溶液中滴加酚酞,变红后又褪色,实验研究表明是有:Na2O2 + H2O == 2NaOH + H2O2,2H2O2 == 2H2O + O2 反应发生。因为H2O2也具有漂白作用。当然过氧化钠也可以直接漂白的。
1、向饱和的Na2CO3溶液中通足量的CO2有晶体NaHCO3析出。
2、Na2CO3溶液与稀HCl的反应①向Na2CO3溶液中滴加稀HCl,先无气体,后有气体,如果n(HCl)小于n(Na2CO3)时反应无气体放出。发生的反应:先①Na2CO3 + HCl == NaCl + NaHCO3,后②NaHCO3 + HCl == NaCl + H2O +CO2 .
②向稀HCl中滴加Na2CO3溶液,先有气体,反应是:Na2CO3 + 2HCl == 2NaCl + H2O + CO2.
如果用2mol的Na2CO3和2.4mol的稀HCl反应,采用①方法放出CO2是0.4mol;采用方法放出CO2为1.2mol。希望同学们在解题时要留意。
3、Na2CO3溶液和NaHCO3溶液的鉴别:取两种试液少量,分别滴加CaCl2或BaCl2溶液,有白色沉淀的原取溶液为Na2CO3,另一无明显现象的原取溶液为NaHCO3.
4、侯氏制碱法
反应式:NaCl + NH3 + CO2 + H2O == NaHCO3 + NH4Cl.
注意:在生产中应先在饱和的NaCl溶液中先通入NH3,后通入CO2,NaHCO3晶体析出过滤,在滤液中加入NaCl细末和通NH3析出NH4Cl晶体为副产品。NH4Cl晶体析出后的母液进行循环试用,提高原料的利用率
一.选择题(共15小题)
1. (2010·西安高一检测)实验室中对于少量金属钠的保存方法,正确的是 ( )
A.保存在水中 B.密封,保存在广口瓶中
C.用铝箔包裹,密封在广口瓶中 D.密封,保存在煤油中
2. (2010·大庆高一检测)在实验室中,用镊子从煤油中取出一小块金属钠,然后用滤纸将煤油吸干,再用小刀切开观察。在这一实验过程中不能得出的钠的物理性质是 ( )
A.钠在常温下是固体 B.钠具有银白色的金属光泽
C.钠的熔点很低 D.金属钠很软
3.(2010·长春高一检测)钠与水反应时产生的各种现象如下:
①钠浮在水面上;②钠沉在水底;③钠熔化成小球;④小球迅速游动逐渐减小,最后消失;⑤发出嘶嘶的声音;⑥滴入酚酞后溶液显红色。其中正确的一组是 ( )
A.①②③④⑤ B.全部 C.①③④⑤⑥ D.①③④⑥
4.(2010·宜春高一检测)下列六种物质:①Na2O ②Na2O2 ③NaCl ④Na2CO3溶液 ⑤NaOH ⑥NaHCO3其中不能与CO2反应的是 ( )
A.①④ B.②③ C.③⑥ D.⑤⑥
5.(2010·广元高一检测)有关焰色反应的实验操作说明错误的是 ( )
A. 先将铂丝灼烧到与原火焰颜色相同,再蘸取被检验的物质
B. 所有金属阳离子的焰色都要透过蓝色钴玻璃观察
C. 实验时,要尽可能选用本身颜色较浅的火焰
D. 每次实验完,均要用盐酸洗净铂丝
6.(2010·广元高一检测)Na2O2晶体和Na2O晶体中阳离子与阴离子的个数比,前者和后者的关系是( )
A. 前者大 B. 前者小
C. 相等 D.不能肯定
7.(2010·大连高一检测)下列关于Na和Na+的叙述中,错误的是 ( )
A.它们相差一个电子层 B.它们的化学性质相似
C.钠原子,钠离子均为同一元素 D.灼烧时,它们的焰色反应都呈黄色
8.(2010·广元高一检测)将金属钠分别投入下列物质的水溶液中,生成白色沉淀的是 ( )
A.HCl B.K2SO4 C.Ca(HCO3)2 D.CuCl2
9.(2010·广元高一检测)不能正确表示下列反应的离子方程式的是 ( )
A.钠与水反应:2Na+2H2O===2Na++2OH-+H2↑
B.钠与CuSO4溶液反应:2Na+Cu2+===Cu↓+2Na+
C.钠与足量的盐酸溶液反应:2Na+2H+===2Na++H2↑
D.钠与KCl溶液反应:2Na+2H2O===2Na++2OH-+H2↑
10.(2010·长春高一检测)下列有关Na2CO3和NaHCO3性质比较中,正确的是 ( )
A.热稳定性:Na2CO3<NaHCO3
B.常温时水溶液中的溶解度:Na2CO3<NaHCO3
C.与稀盐酸反应快慢:Na2CO3<NaHCO3
D.物质的量相同时,消耗盐酸:Na2CO3<NaHCO3
11.(2010·杭州高一检测)下列各组中的两物质反应时,反应条件或反应物用量的改变对生成物没有影响的是 ( )
A、CO2与Ca(ClO)2 B、NaOH与CO2 C、Na与O2 D、Na与H2O
12.(2010·泉州高一检测)有一位学生将一小块钠投入到盛有煤油和水的试管中(煤油和水均足够多),想一想可能观察到的现象是 ( )
A.钠浮在试管中的液面上并四处游动
B.钠沉入试管底部
C.钠与水剧烈反应
D.钠处于煤油和水的交界处并可能作上、下跳动
13.(2010·社旗高一检测)现有NaOH、Na2CO3和Ba(OH)2三种无色溶液,用一种试剂就可将它们鉴别出来,这种试剂是 ( )
A.HCl B.H2SO4 C.Na2SO4 D.CaCl2
14.(2010·大连高一检测)少量的金属钠长期暴露在空气中,它的最终产物是 ( )
A.NaOH B. Na2CO3?10H2O C.Na2CO3 D.NaHCO3
15.(2010·白银高一检测)有关Na2CO3和NaHCO3的性质,下列叙述中错误的是 ( )
A. Na2CO3受热不分解,而NaHCO3受热易分解
B. Na2CO3溶液和 NaHCO3溶液都显碱性
C.等物质的量的Na2CO3和NaHCO3跟同一种盐酸充分反应时,消耗酸的体积之比是2∶1
D.将澄清的石灰水分别加入Na2CO3和NaHCO3溶液时,前者产生沉淀,后者不产生沉淀
 二.非选择题(共2个小题)
二.非选择题(共2个小题)
16.(2010·宜春高一检测)如右图所示,在烧杯中盛有100 mL 蒸馏水,水中悬浮着一个表面光滑、耐热、耐碱的小球(此球稳定在水的中央)。将1.0 g 金属钠分多次投入到水中,最后使烧杯内的液体恢复到原来的蒸馏水的温度。
回答下列问题:
(1)1.0 g 钠要分多次投入的主要原因是 。
(2)实验结束时,从烧杯内小球的位置观察到的现象是 ,出现此种现象的主要原因是 。
(3)实验过程中所发生的化学反应方程式是 。
17.(2010·宜春高一检测) A、B、C、D、E、F六种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体。而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体,该气体能使带火星的木条复燃。请回答下列问题:
(1)写出B、C、F的化学式B ;C ; F
(2)写出F和H反应的化学方程式 。
(3)写出下列反应的离子方程式:
①D+盐酸 。
②D+A 。
18.(2010·白银高一检测)取100 mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到14.51 g白色沉淀和滤液(溶液体积为200 mL),再用过量稀硝酸处理沉淀,最后减少到4.66 g,并有气体放出。计算:[第(3)问请写出计算过程]
⑴ 原混合液中Na2SO4的物质的量浓度为 mol ·L-1;
⑵ 产生的气体在标准状况下的体积为 L;
⑶ 过滤出沉淀后,计算所得滤液的物质的量浓度为多少?
第二篇:金属及其化合物知识点总结
金属单质及其化合物
考点聚焦
1.《考试大纲》中对金属元素及化合物这块内容可分成二部分来理解。第一部分是钠、镁等典型的金属元素的化合物;第二部分是其他金属(如铁和铝)元素的化合物。每年的化学高考试题中往往都要考查到典型金属。
2.《考试大纲》中有多条类似于“以××为例,了解(或理解、掌握)××××”的内容叙述,如:以过氧化钠为例,了解过氧化物的性质;以Fe(Ⅱ)、Fe(Ⅲ)的相互转化为例,了解变价金属元素的氧化还原性。对这些内容的要注意理解实质,达到“举一反三”的要求。在这些内容往往是高考命题的重点。
3.金属元素及其化合物跟化学实验的综合。近几年的实验试题中比较多地出现了以金属元素及其化合物为落点的实验试题和元素推断题,请大家加以重视。
4. 常见金属元素(如Na、Al、Fe、Cu等)
⑴了解常见金属的活动顺序。
⑵了解常见金属及其重要化合物的主要性质及其应用。
⑶了解合金的概念及其重要应用。
知识梳理
1、钠及其化合物
2、镁及其化合物
3、铝及其化合物
4、铁、铜及其化合物
一、钠及其化合物
1、钠
(1)钠的物理性质:钠是银白色金属,密度小(0.97g/cm3),熔点低(97℃),硬度小,质软,可用刀切割。钠通常保存在煤油中。是电和热的良导体。
(2)钠的化学性质:从原子结构可知钠是活泼的金属单质。
①钠与非金属单质反应:常温:4Na + O2 == 2Na2O,加热:2Na + O2 Na2O2; 2Na + Cl2 2NaCl; 2Na + S Na2S等。
②钠与水反应:2Na + 2H2O == 2NaOH + H2↑;实验现象:钠浮在水面上,熔成小球, 注意:钠在空气中的变化:银白色的钠 变暗(生成了氧化钠) 变白(生成氢氧化钠) 潮解 变成白色固体(生成碳酸钠)。
③钠与酸反应:如2Na + 2HCl == 2NaCl + H2↑,Na放入稀盐酸中,是先与酸反应,酸不足再与水反应。因此Na放入到酸溶液中Na是不可能过量的。同时Na与H2的物质的量比始终是2:1。当然反应要比钠与水的反应剧烈多。
④钠与盐的溶液反应:钠不能置换出溶液中的金属,钠是直接与水反应。反应后的碱再与溶液中的其他物质反应。如钠投入到硫酸铜溶液的反应式:2Na + CuSO4 + 2H2O ==
Cu(OH)2 ↓+ Na2SO4 + H2 ↑。 ⑤钠与氢气的反应:2Na + H2 == 2NaH。NaH + H2O == NaOH + H2 ↑;NaH是强的还原在水面上游动,有哧哧的声音,最后消失,在反应后的溶液中滴加酚酞,溶液变红。
剂。
(3)工业制钠:电解熔融的NaCl,2NaCl(熔融) 2Na + Cl2↑。
(4)钠的用途:①在熔融的条件下钠可以制取一些金属,如钛、锆、铌、钽等; ②钠钾合金是快中子反应堆的热交换剂;
③钠蒸气可作高压钠灯,发出黄光,射程远,透雾能力强。
2、氧化钠和过氧化钠
(1)Na2O:白色固体,是碱性氧化物,具有碱性氧化物的通性:Na2O + H2O == 2NaOH, Na2O + CO2 == Na2CO3,Na2O + 2HCl == 2NaCl + H2O .另外:加热时,2Na2O + O2 == 2Na2O2.
(2)Na2O2:淡黄色固体是复杂氧化物,易与水、二氧化碳反应放出氧气。
2Na2O2 + 2H2O == 4NaOH + O2 ↑,2Na2O2 + 2CO2 == 2Na2CO3 + O2 ↑(作供氧剂)。 因此Na2O2常做生氧剂,同时,Na2O2还具有强氧化性,有漂白作用。如实验:Na2O2和水反应后的溶液中滴加酚酞,变红后又褪色,实验研究表明是有:Na2O2 + H2O == 2NaOH + H2O2,2H2O2 == 2H2O + O2 反应发生。因为H2O2也具有漂白作用。当然过氧化钠也可以直接漂白的。
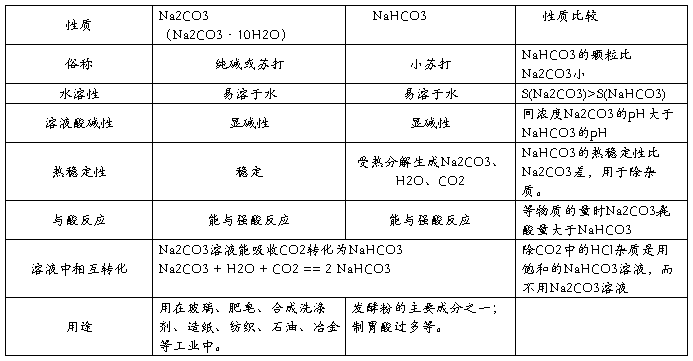
3、碳酸钠和碳酸氢钠 性质 Na2CO3(Na2CO3?10H2O) NaHCO3 性质比较
俗称 纯碱或苏打 小苏打 NaHCO3的颗粒比Na2CO3小
水溶性 易溶于水 易溶于水 S(Na2CO3)>S(NaHCO3)
溶液酸碱性 显碱性 显碱性 同浓度Na2CO3溶液的pH大于NaHCO3溶液的pH
热稳定性 稳定 受热分解生成Na2CO3、H2O、CO2 NaHCO3的热稳定性比Na2CO3差,用于除杂质。
与酸反应 能与强酸反应 能与强酸反应 等物质的量时Na2CO3耗酸量大于NaHCO3 溶液中相互转化 Na2CO3溶液能吸收CO2转化为NaHCO3
Na2CO3 + H2O + CO2 == 2 NaHCO3
除CO2中的HCl杂质是用饱和的NaHCO3溶液,而不用Na2CO3溶液
用途 用在玻璃、肥皂、合成洗涤剂、造纸、纺织、石油、冶金等工业中。 发酵粉的主要成分之一;制胃酸过多等。
注意几个实验的问题:
1、向饱和的Na2CO3溶液中通足量的CO2有晶体NaHCO3析出。
2、Na2CO3溶液与稀HCl的反应①向Na2CO3溶液中滴加稀HCl,先无气体,后有气体,如果n(HCl)小于n(Na2CO3)时反应无气体放出。发生的反应:先①Na2CO3 + HCl == NaCl + NaHCO3,后②NaHCO3 + HCl == NaCl + H2O +CO2 .
②向稀HCl中滴加Na2CO3溶液,先有气体,反应是:Na2CO3 + 2HCl == 2NaCl + H2O + CO2.
如果用2mol的Na2CO3和2.4mol的稀HCl反应,采用①方法放出CO2是0.4mol;采用
②方法放出CO2为1.2mol。希望同学们在解题时要留意。
3、Na2CO3溶液和NaHCO3溶液的鉴别:取两种试液少量,分别滴加CaCl2或BaCl2溶液,有白色沉淀的原取溶液为Na2CO3,另一无明显现象的原取溶液为NaHCO3。
4、侯氏制碱法
反应式:NaCl + NH3 + CO2 + H2O == NaHCO3 ↓+ NH4Cl.
注意:在生产中应先在饱和的NaCl溶液中先通入NH3,后通入CO2,NaHCO3晶体析出过滤,在滤液中加入NaCl细末和通NH3析出NH4Cl晶体为副产品。NH4Cl晶体析出后的母液进行循环试用,提高原料的利用率。
二、镁及其化合物
1、镁的性质
(1)物理性质:镁是银白色金属,质较软,密度1.74g/cm3,是轻金属,硬度小。
(2)化学性质:镁是较活泼金属
①与非金属反应:2Mg + O2 == 2MgO,Mg + Cl2 MgCl2,3Mg + N2 Mg3N2等。 ②与沸水反应:Mg + 2H2O(沸水)== Mg(OH)2 + H2 ↑.
③与酸反应:与非强氧化性酸反应:是酸中的H+与Mg反应,有H2放出。
与强氧化性酸反应:如浓H2SO4、HNO3,反应比较复杂,但是没有H2放出。
④与某些盐溶液反应:如CuSO4溶液、FeCl2溶液、FeCl3溶液等。
Mg + 2FeCl3 == 2FeCl2 + MgCl2, Mg + FeCl2 == Fe + MgCl2.
2、镁的提取:海水中含有大量的MgCl2,因此,工业上主要是从分离了NaCl的海水中来提取MgCl2.
流程:海水中加入CaO或Ca(OH)2 Mg(OH)2沉淀、过滤、洗涤沉淀,用稀HCl溶解 MgCl2溶液,蒸发结晶 MgCl2?6H2O晶体,在HCl气体环境中加热 MgCl2固体,电解熔融的MgCl2 Mg + Cl2 ↑。
主要反应:MgCl2 + Ca(OH)2 == Mg(OH)2↓+ CaCl2, Mg(OH)2 + 2HCl == MgCl2 + 2H2O, MgCl2?6H2O MgCl2 + 6H2O , MgCl2(熔融) Mg + Cl2↑。
3、镁的用途:镁主要是广泛用于制造合金。制造的合金硬度和强度都较大。因此镁合金被大量用火箭、导弹、飞机等制造业中。
4、氧化镁(MgO):白色固体,熔点高(2800℃),是优质的耐高温材料(耐火材料)。是碱性氧化物。
MgO + H2O == Mg(OH)2, MgO + 2HCl == MgCl2 + H2O 。
注意以下几种情况的离子方程式的书写:
(1)n(Mg(HCO3)2):n(NaOH)=1:4:Mg2+ + 2HCO3- + 4OH- == Mg(OH)2↓+ 2CO32- + 2H2O;
(2)n(Mg(HCO3)2):n(NaOH)=1:2:Mg2+ + 2HCO3- + 2OH- == MgCO3↓+ CO32- + 2H2O;
(3)n(Mg(HCO3)2):N(NaOH)=1:1: Mg2+ + HCO3- + OH- == MgCO3↓+H2O 。
三、铝及其化合物
1、铝的性质:
(1)物理性质:银白色金属,质较软,但比镁要硬,熔点比镁高。有良好的导电、导热性和延展性。
(2)化学性质:铝是较活泼的金属。
①通常与氧气易反应,生成致密的氧化物起保护作用。4Al + 3O2 == 2Al2O3。同时也容易与Cl2、S等非金属单质反应。
②与酸反应:强氧化性酸,如浓硫酸和浓硝酸在常温下,使铝发生钝化现象;加热时,能反应,但无氢气放出;非强氧化性酸反应时放出氢气。
③与强碱溶液反应:2Al + 2NaOH + 2H2O == 2NaAlO2 + 3H2↑。
④与某些盐溶液反应:如能置换出CuSO4、AgNO3等溶液中的金属。
⑤铝热反应:2Al + Fe2O3 Al2O3 + 2Fe。该反应放热大,能使置换出的铁成液态,适用性强。在实验室中演示时要加入引燃剂,如浓硫酸和蔗糖或镁条和氯酸钾等。
2、氧化铝(Al2O3):白色固体,熔点高(2054℃),沸点2980℃,常作为耐火材料;是两性氧化物。我们常见到的宝石的主要成分是氧化铝。有各种不同颜色的原因是在宝石中含有一些金属氧化物的表现。如红宝石因含有少量的铬元素而显红色,蓝宝石因含有少量的铁和钛元素而显蓝色。工业生产中的矿石刚玉主要成分是α-氧化铝,硬度仅次于金刚石,用途广泛。
两性氧化物:既能与强酸反应又能与强碱反应生成盐和水的氧化物。
Al2O3 + 6HCl == 2AlCl3 + 3H2O ,Al2O3 + 2NaOH == 2NaAlO2 + H2O 。
Al2O3是工业冶炼铝的原料,由于氧化铝的熔点高,电解时,难熔化,因此铝的冶炼直到1886年美国科学家霍尔发现在氧化铝中加入冰晶石(Na3AlF6),使氧化铝的熔点降至1000度左右,铝的冶炼才快速发展起来,铝及其合金才被广泛的应用。2Al2O3 4Al + 3O2↑。
3、氢氧化铝(Al(OH)3):白色难溶于水的胶状沉淀,是两性氢氧化物。热易分解。 两性氢氧化物:既能与强酸又能与强碱反应生成盐和水的氢氧化物。
Al(OH)3 + 3HCl == AlCl3 + 3H2O, Al(OH)3 + NaOH == NaAlO2 + 2H2O.2Al(OH)3 Al2O3 +3 H2O
4、铝的冶炼:铝是地壳中含量最多的金属元素,自然界中主要是以氧化铝的形式存在。工业生产的流程:铝土矿(主要成分是氧化铝) 用氢氧化钠溶解过滤 向滤液中通入二氧化碳酸化,过滤 氢氧化铝 氧化铝 铝。
主要反应:Al2O3 + 2NaOH == 2NaAlO2 + H2O ,CO2 + 3H2O + 2NaAlO2 == 2Al(OH)3↓+ Na2CO3 ,2Al(OH)3 Al2O3 +3 H2O ,2Al2O3 4Al + 3O2↑。
5、铝的用途:铝有良好的导电、导热性和延展性,主要用于导线、炊具等,铝的最大用途是制合金,铝合金强度高,密度小,易成型,有较好的耐腐蚀性。迅速风靡建筑业。也是飞
机制造业的主要原料。
6、明矾的净水:化学式:KAl(SO4)2?12H2O,它在水中能电离:KAl(SO4)2 == K+ + Al3+ + 2SO42-。铝离子与水反应,生成氢氧化铝胶体,具有很强的吸附能力,吸附水中的悬浮物,使之沉降已达净水目的。Al3+ + 3H2O == Al(OH)3 (胶体)+ 3H+ 。
知识整理:
①(Al(OH)3)的制备:在氯化铝溶液中加足量氨水。AlCl3 + 3NH3?H2O == Al(OH)3↓+ 3NH4Cl 。
②实验:A、向氯化铝溶液中滴加氢氧化钠溶液,现象是先有沉淀,后溶解。
反应式:先Al3+ + 3OH- == Al(OH)3↓, 后Al3+ + 4OH- == AlO2- + 2H2O。
B、向氢氧化钠溶液中滴加氯化铝溶液,现象是开始无沉淀,后来有沉淀,且不溶解。 反应式:先Al3+ + 4OH- == AlO2- + 2H2O,后Al3+ + 3AlO2- + 6H2O == 4Al(OH)3↓。 ③实验:向偏铝酸钠溶液中通二氧化碳,有沉淀出现。CO2 + 3H2O + 2NaAlO2 == 2Al(OH)3↓+ Na2CO3。
④将氯化铝溶液和偏铝酸钠溶液混和有沉淀出现。 Al3+ + 3AlO2- + 6H2O == 4Al(OH)3↓。 ⑤实验:A、向偏铝酸钠溶液中滴加稀盐酸,先有沉定,后溶解。
反应的离子方程式:AlO2- + H+ + H2O == Al(OH)3 ,Al(OH)3 + 3H+ == Al3+ + 2H2O 。
B、向稀盐酸中滴加偏铝酸钠溶液,先无沉淀,后有沉淀且不溶解。
反应的离子方程式:AlO2- + 4H+ == Al3+ + 2H2O ,3AlO2- + Al3+ + 6H2O == 4Al(OH)3↓。
