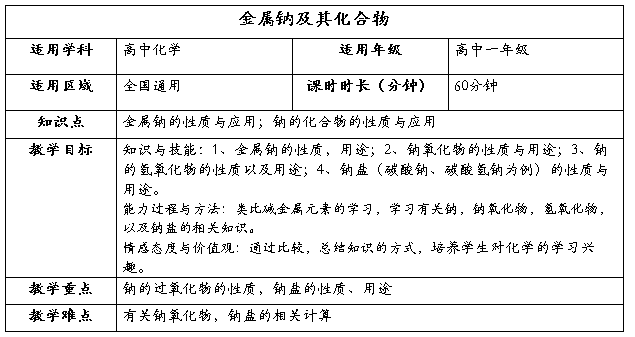
教学过程
一、 课堂导入



二、复习预习
1. 通过回忆初中学过的镁、铝、铁、铜的部分性质,来认识钠是一种活泼金属
2. 写出一些与钠元素相关的反应方程式
3. 金属的性质与存在
三、知识讲解
考点/易错点1 金属钠
1、钠原子结构:钠原子最外层只有一个电子,在化学变化中易失去最外层电子,呈现很强的金属性,在氧化还原反应中做还原剂。
2、钠的物理性质:钠是银白色金属,密度小(0.97g/cm3),熔点低(97℃),硬度小,质软,可用刀切割。钠通常保存在煤油中。是电和热的良导体。
3、钠的化学性质: 从原子结构可知钠是活泼的金属单质。
(1)钠与非金属反应: 2Na+S=Na2S 4Na+O2=2Na2O 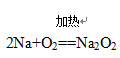 (钠先熔化成小球,再燃烧,发出黄色火焰,生成淡黄色固体)
(钠先熔化成小球,再燃烧,发出黄色火焰,生成淡黄色固体)
(2)钠与水(冷水)反应 2Na+2H2O=2NaOH+H2↑
钠与水反应的现象 实验原理
钠浮在水面上, 钠的密度比水小
熔成小球, 钠的熔点低,反应放热
在水面上迅速游动,逐渐变小,最后消失, 反应产生的气体推动小球运动
与水反应发出 哧哧 的声音 钠与水反应剧烈,反应放热
在反应后的溶液中滴加酚酞,溶液变红。 有碱性物质生成
(3)钠与酸反应: 2Na+2HCl=2NaCl+H2↑
(4)钠与碱反应:实质是钠与水的反应
(5)钠与盐反应:Na与盐溶液一般不发生置换反应,但与熔融的盐可发生置换反应。 (如4Na+TiCl4(熔融) Ti+4NaCl)
Ti+4NaCl)
Na放入盐溶液时,先与水反应,它包括两种情况:(1)如果盐溶液的溶质不与NaOH反应:如氯化钠溶液;(2)如果盐溶液中的溶质与NaOH反应:生成的碱与盐发生复分解反应,
例如:将Na放入CuSO4溶液中,反应剧烈,有气体和沉淀生成。
2Na+H2O=2NaOH+H2↑ 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
因Na与水反应时有热量放出,生成的Cu(OH)2是难溶性碱,受热易分解,所以此反应中有时会有黑色沉淀CuO生成。(Cu(OH)2 CuO+H2O)
CuO+H2O)
4、工业制钠:电解熔融的NaCl,2NaCl(熔融)  2Na + Cl2↑。
2Na + Cl2↑。
5、钠的用途:在熔融的条件下钠可以制取一些金属,如钛、锆、铌、钽等;钠钾合金是快中子反应堆的热交换剂;钠蒸气可作高压钠灯,发出黄光,射程远,透雾能力强。
6、碱金属元素原子结构、性质的相似性和递变性
(1)相似性:
与Na结构相似的还有Li、K、Rb、Cs等元素。它们原子的最外层都只有1个电子,均易失1个电子形成带1个单位正电荷的阳离子,所以它们均为活泼金属,均具有很强的还原性,能与氧气、非金属、水、酸等反应,生成产物均为离子化合物。
(2)差异性与递变性
随着核电荷数的增加,由Li到Cs,电子层数依次递增,核到最外电子层的距离逐渐增大,核对最外层电子的引力逐渐减小,失电子能力增强,即还原性增强,与其它物质间的反应程度更加剧烈。如与氧气反应时,Li常温或燃烧均生成Li2O,Na常温时生成Na2O,燃烧时则生成Na2O2,而K常温生成K2O2,燃烧生成KO2(超氧化钾)。
它们的最高价氧化物的对应水化物——碱--均为强碱,且碱性依次增强。
考点/易错点2 钠的氧化物
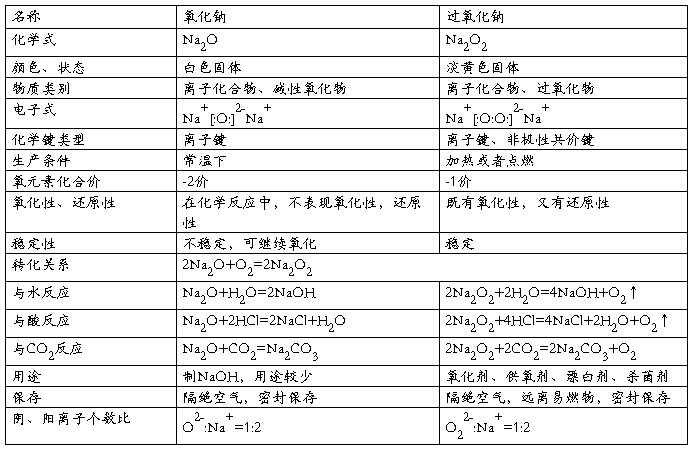
考点/易错点3 钠的氢氧化物
1、物理性质:氢氧化钠具有很强的腐蚀性。俗称:苛性钠、烧碱、火碱。氢氧化钠是一种白色固体,易吸收水分而发生潮解,易溶于水,溶于水放出大量的热量。
2、化学性质:
(1)与酸碱指示剂作用:能使紫色石蕊试液变蓝色,使无色酚酞变红色。
(2)与酸发生中和反应 : 与酸反应中和生成盐和水。
(3)与非金属氧化物反应 :与二氧化硫、二氧化碳等酸性气体反应,生成盐和水。
(4)与某些盐溶液反应:与硫酸铜溶液反应生成蓝色沉淀;与硫酸铁溶液反应生成红褐色沉淀;与铵盐反应生成碱性气体。
3、氢氧化钠的保存
密封保存在橡胶塞的玻璃瓶(原因是玻璃的主要成分是二氧化硅,会跟氢氧化钠反应,生成硅酸钠,硅酸钠具有粘稠性,会是塞子黏住导致开不了。)
考点/易错点4 钠盐
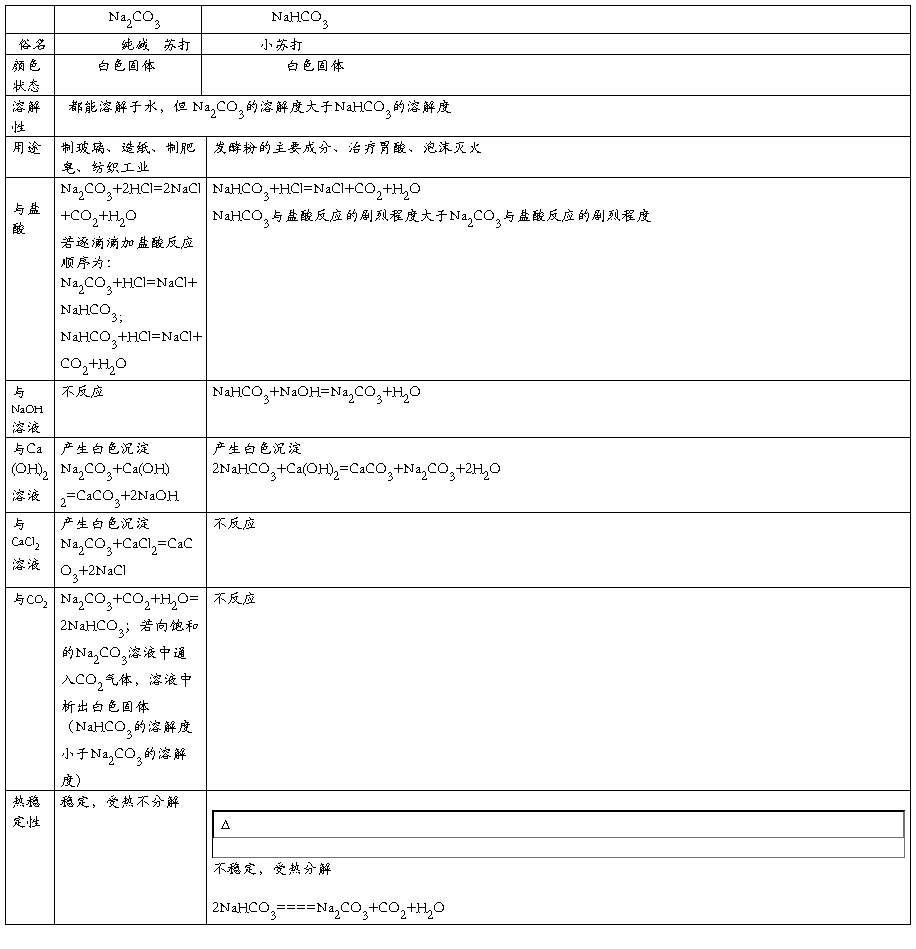
四、例题精析
【例题1】
.有一小块钠久置于空气中,最后生成的产物是( )
A.Na2O2 B.NaHCO3 C.Na2CO3 D.Na2CO3·10H2O
【答案】 C
【解析】钠在空气中久置,其变化过程是:
Na Na
Na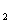 O
O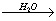 NaOH
NaOH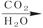 Na2CO
Na2CO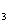 ·10H
·10H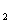 O
O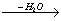 Na
Na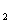 CO
CO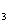
【例题2】
将31.2 g过氧化钠和100 g水充分反应后所得溶液的质量分数为( )
A.25.6% B.31.2% C.32.0% D.34.5%
【答案】A
【解析】过氧化钠溶于水生成氢氧化钠溶液,故所求溶液的溶质为NaOH。
2Na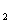 O
O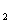 +2H
+2H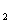 O
O 4NaOH+O
4NaOH+O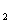 ↑
↑
2×78 4×40 32
31.2 g x y
x=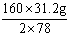 =32 g(NaOH) y=
=32 g(NaOH) y= =6.4 g(O
=6.4 g(O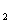 )w(NaOH)=
)w(NaOH)= 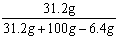 ×100%=25.6%
×100%=25.6%
【例题3】
有关热稳定性的强弱比较,不正确的是( )
A.K2MnO4<KMnO4 B.Na2O2>Na2O C.NaHCO3<Na2CO3 D.KClO3<KCl
【答案】A
【解析】在加热条件下,Na2O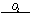 Na2O2,NaHCO3
Na2O2,NaHCO3 Na2CO3,KClO3
Na2CO3,KClO3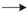 KCl,KMnO4
KCl,KMnO4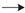 K2MnO4,故A不正确。
K2MnO4,故A不正确。
五、课堂运用
【基础】
1、下列各组内的两种物质发生反应时,其产物不随反应物用量比的改变而发生变化的是( )
A.C和O2 B.NaOH溶液和CO2
C.Na2CO3溶液和盐酸 D.Na和Cl2
【答案】D
【解析】A选项中,O2不足量,生成CO2;O2过量,生成CO2。B选项中,CO2不足,生成Na2CO3;CO2过量,生成NaHCO3。C选项中,盐酸不足,生成NaHCO3和NaCl;盐酸足量,生成NaCl、H2O和CO2。D选项正确。
2、将11.5 g金属钠投入到88.5 g水中,反应完毕后,求生成溶液的质量分数(不考虑水的蒸发)。
【答案】20.1%
【解析】本题的解题关键是弄清钠跟水反应有氢气产生,所得溶液中的溶质是NaOH。
设消耗水的质量为x,生成NaOH和H2的质量分别为y、z,则:
2Na + 2H2O 2NaOH+ H2↑
2NaOH+ H2↑
2×23 2 ×18 2×40 2
11.5 g x y z
46∶36=11.5 g∶x x=9 g
46∶80=11.5 g∶y y=20 g
46∶2=11.5 g∶z z=0.5 g
解法1:w(NaOH)= 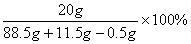 =20.1%
=20.1%
解法2:w(NaOH)= 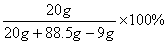 =20.1%
=20.1%
【巩固】
1、下列各步反应中,A为金属,B为淡黄色固体,且每一物质均含A元素
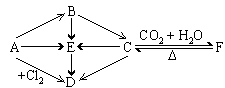
写出A、B、C、D、E、F的化学式及有关化学方程式。
【答案】A—Na B—Na2O2 C—Na2CO3 D—NaCl E—NaOH F—NaHCO3
【解析】此题的解题关键是要先判断出已知具体色态的B为何物质,金属对应的化合物呈现淡黄色的暂判定为Na2O2,那么就可以引出D为NaCl,C + CO2 + H2O®F,F 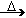 C,而Na2O2可以生成C,C可以生成NaCl,从而推导出各物质。
C,而Na2O2可以生成C,C可以生成NaCl,从而推导出各物质。
2、在盛有5 mL澄清饱和石灰水的试管中放入一小块钠,不可能观察到的现象是( )
A.钠熔化成银白色的小球 B.浮在液面快速游动 C.液体底部出现银白色固体 D.溶液变浑浊
【答案】C
【解析】钠首先跟水反应,发生的现象有:熔化成银白色的小球,浮在液面上迅速游动,有气泡产生等。因跟水反应需消耗水(减少溶剂)且生成OH-,都会使澄清石灰水变浑浊,析出Ca(OH)2 沉淀。
【拔高】
1.200℃时,11.6g CO2和水蒸气的混合气体与足量的Na2O2充分反应,反应后固体的质量增加了3.6g。则原混合气体的平均式量为( )
A.5.8 B.11.6 C.23.2 D.46.4
【答案】C
【解析】解法一:差量法
设原混合气体中含CO2和H2O物质的量分别为x、y
2Na2O2 + 2CO2 === 2Na2CO3 + O2 固体质量增加
78×2g 2mol 106×2g (212-156)g
x 28x
2Na2O2 + 2H2O === 4NaOH + O2 固体质量增加
78×2g 2mol 40×4g 4g
y 2y

则混合气的平均式量为:
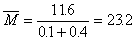 故选C
故选C
解法二:平均值法
由方程式:2CO2 + 2Na2O2 === 2Na2CO3 + O2和2H2O + 2Na2O2 === 4NaOH + O2可知,固体增加的质量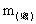 ,应是
,应是 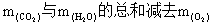 之值,即:
之值,即:
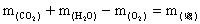 所以,
所以,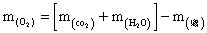
这样, 
则O2物质的量
又由于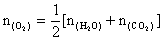 所以混合气总物质的量
所以混合气总物质的量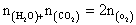
因此混合气体的平均式量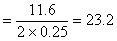
解法三:估算法
CO2的式量为44,水蒸气的式量为18,因此两种气体的混合物的平均式量必介于二者之间,故应选C。
2、将a g水煤气(成分为CO和H2)充分燃烧,将燃烧生成的气 体(150℃)通过盛有过量的Na2O2的干燥管(反应气体无 损失),充 分反应后干燥管增重b g,则a和b的关系为( )
A.a>b B.a=b C.a<b D.无法比较
【答案】B
【解析】2H2+O2=2H2O, 2H2O+2Na2O2=4NaOH+O2 把这两个反应加和,得到:2H2+Na2O2=2NaOH 相当于过氧化钠直接吸收了氢气。 同样道理:2CO+O2=2CO2, 2CO2+2Na2O2=2Na2CO3+O2 把这两个反应加和,得到:CO+Na2O2=Na2CO3 也是相当于过氧化钠直接吸收了CO 所以有多少克CO和H2的混合物,最后Na2O2的质量就会增加多少。
课程小结
1. 金属钠的性质
2. 钠氧化物的性质与用途
3. 钠盐的性质与用途
第二篇:金属钠及其化合物计算课






