20##-2012ѧ����ѧ�ڸ�һ��ѧ����1
�����½������仯����ĵ�Ԫ�ܽ�
һ. ��ѧ���ݣ�
�����½������仯����ĵ�Ԫ�ܽ�
��. �ص㡢�ѵ�
1. �Լ��ֳ��������Ļ�ѧ���ʽ��й����ܽᣬ���ս����Ļ�ѧ���ʵĹ��Ժ������ԡ�
2. �ѱ���Ԫ�ػ������֪ʶ��ǰ���µ�֪ʶ�л��Ľ�ϡ�
��. ��������
�����½����˹��ڽ���Ԫ�ص����֪ʶ����Ҫ��Na��Al��Fe��Cu����Ԫ�ء�
�����漰��֪ʶ����Ҫ�漰���㣺
��һ���Ƶ��ʼ��仯����
1. �Ƶĵ���
���������ķ�Ӧ�����ºͼ����������
����ˮ��Ӧ������Ӧ��˵��������
�ƺ���������ķ�Ӧ
2. �ƵĻ�����
�����ƺ������Ƶ����ʱȽ�
̼���ƺ�̼�����Ƶ����ʱȽ�
�����������ʼ��仯����
1. ������
����������Ӧ
�����ᷴӦ
���ͼӦ
2. ���Ļ�����
����������������������
�����������ʼ��仯����
1. ������
����ˮ�ķ�Ӧ
2. ���Ļ�����
��������������ıȽ�
�������εıȽ�
���ģ���ɫ��Ӧ
���壩��������
�����������ϵ����ʺ�Ӧ��
�������й����ʵ���������
������������
[��1] �������������ƣ���һ�������������м��ȣ��ڶ������������������£��г�ַ�Ӧ��������˵����ȷ���ǣ� ��
A. ��һ����ʧȥ���Ӷ� B. ������ʧȥ����һ����
C. �ڶ����Ƶķ�Ӧ����������� D. �����Ƶķ�Ӧ��������һ����
�𰸣�B
�������������ڲ�ͬ�����·�Ӧ�IJ�ͬ��������ԭ��Ӧ���жϡ�
[��2] ͨ�����ý������������ƣ�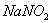 ���ڿ����й��ȵķ�����ȡ�����ƣ���Ӧ����һ����Ϊ
���ڿ����й��ȵķ�����ȡ�����ƣ���Ӧ����һ����Ϊ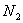 ����÷�Ӧ�Ļ�ѧ����ʽΪ_______________���÷�Ӧ����������________����������Ԫ����____����˵��Ϊʲô����������������ȼ�յķ��������ô˷���ȡ�����Ƶ�ԭ��_________________��
����÷�Ӧ�Ļ�ѧ����ʽΪ_______________���÷�Ӧ����������________����������Ԫ����____����˵��Ϊʲô����������������ȼ�յķ��������ô˷���ȡ�����Ƶ�ԭ��_________________��
�𰸣�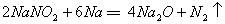 ���������ƣ���Ԫ�أ�����������ȼ�ջ����ɹ������ƣ����ܵõ������ơ������������������ڿ����й�����ȡ������ʱ�����ڷ�Ӧ���������˵��������������ɵ�������������������ĽӴ��������Ʋ��ܱ�������һ���������ʿɵõ��ϴ��������ơ�
���������ƣ���Ԫ�أ�����������ȼ�ջ����ɹ������ƣ����ܵõ������ơ������������������ڿ����й�����ȡ������ʱ�����ڷ�Ӧ���������˵��������������ɵ�������������������ĽӴ��������Ʋ��ܱ�������һ���������ʿɵõ��ϴ��������ơ�
������ѧ�������Ϣ����ѧ֪ʶ��������⡣
[��3] ���ڸ��������������������ϳɰ�ɫNaH����Ӧ�Ļ�ѧ����ʽΪ_____________������������Ϊ______________��NaH�н�ǿ�Ļ�ԭ�ԣ���˿����⻯���ڸ����½����Ȼ��� ��ԭ���ѣ�д���÷�Ӧ�Ļ�ѧ����ʽ____________��NaH����ˮ���ҷ�Ӧ��
��ԭ���ѣ�д���÷�Ӧ�Ļ�ѧ����ʽ____________��NaH����ˮ���ҷ�Ӧ��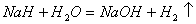 ��NaH��Һ��
��NaH��Һ�� Ҳ�����Ʒ�Ӧ��д����Ӧ�Ļ�ѧ����ʽ______________��
Ҳ�����Ʒ�Ӧ��д����Ӧ�Ļ�ѧ����ʽ______________��
�𰸣�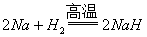 ������
������
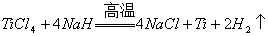 ��
��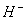 �������ɵ���
�������ɵ���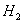 ��
��
 ��NaH�е�
��NaH�е�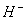 ���һ��+1�۵���ԭ���γ�һ��
���һ��+1�۵���ԭ���γ�һ��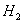 ���ӣ�
���ӣ�
������������������������д��Ӧ����ע��Աȷ�Ӧ�������ԡ�
[��4] ����һ��������Na2O���ʵ�Na2O2�����������ͼ��ѡ���ʵ���ʵ��װ�ã����һ�����ʵ�飬�ⶨNa2O2�����Ĵ��ȣ��ɹ�ѡ�õķ�Ӧ��ֻ��CaCO3���壬6mol��L���������ˮ����

����д���пհף�
��1��д����ʵ����Na2O2��Na2O�ֱ�����Ӧ�Ļ�ѧ����ʽ_______��____��
��2��Ӧѡ�õ�װ���ǣ�ֻҪ��д��ͼ��װ�õı�ţ�____��
��3����ѡ��װ�õ�����˳��Ӧ�ǣ�����ӿڵ���ĸ�����ӽ���ʡ�ԣ�______��
������1��2Na2O2 +2 CO2 ��2Na2 CO3 + O2����Na2O + CO2 == Na2 CO3 ��2���ݢޢߢ٢ܣ�3��GHIJKABF
�������Ա��Ƶ������������������̼��Ӧ�IJ�ͬ�㡣
[��5] ��һ������������ͨ���ۺ�ˮ������Ӧ�����Եõ�������������������ֿ��Ծ����˷�Ӧ���淴Ӧ�����ɿ�����ϸ�����ۣ��������۾��кܸߵķ�Ӧ���ԣ��ڿ�������ײ��������ʱ��ȼ�գ������׳ơ�������������ֱ�����ͼ��ʾ�����������װ�ã���ȡ��������������͡�����������ʵ���б���ʹ����ͨ���ۡ�6mol·L��1���ᣬ�����Լ���ѡ��װ���б�Ҫ������̨�����С���Ȧ��ʯ�����������豸����ͼ�о�����ȥ����
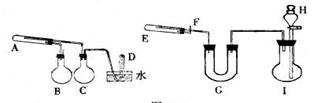
��д���пհף�
��1��ʵ�����ʱ�Թ�A��Ӧ������Լ��� ����ƿB�������� ����ƿC�������� �����Թ�D���ռ��õ����� ��
��2��ʵ��ʱ��U��G��Ӧ������Լ��� �� ��Һ©��H��Ӧ���� ��
��3������װ���У���ʵ��ʱ��Ҫ���ȵ������ǣ����������Ӧ��ĸ�� ��
��4����ƿI�з����ķ�Ӧ��ʱҪ������������ͭ��Һ����Ŀ���� ��
��5���Թ�E�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��6��Ϊ�˰�ȫ����E���еķ�Ӧ����ǰ����F���ڴ����� ��E���з�Ӧ��ʼ����F���ڴ�Ӧ ��
�𰸣�
��1����ͨ���ۣ���Ϊˮ��������������ֹˮ������������
��2������NaOH�����ʯ�ҡ�CaO�ȼ��Թ�����������6mol·L��1HCl
��3��A��B��E
��4���ӿ������������ٶ�
��5��
��6�����������Ĵ��ȣ���ȼ����
�������Ӹ�ʵ�����������������̽���������ʡ�
[��6] ���������ַ��������Ƶð�ɫ�� ������
������
����һ���ò���Fe3����FeSO4��Һ���ò���O2������ˮ���Ƶ�NaOH��Һ��Ӧ�Ʊ���
��1������������������������FeSO4��Һʱ������� ��
��2����ȥ����ˮ���ܽ��O2������ �ķ�����
��3�����ɰ�ɫ �����IJ������ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ������������������ ��
�����IJ������ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ������������������ ��
������������ͼװ���У���NaOH��Һ����м��ϡH2SO4���Լ��Ʊ���
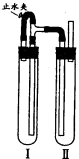
��1�����Թܢ��������Լ��� ��
��2�����Թܢ��������Լ��� ��
��3��Ϊ���Ƶð�ɫ ���������Թܢ�͢��м����Լ�����ֹˮ�У��������Ӻ��ʵ�鲽���� ��
���������Թܢ�͢��м����Լ�����ֹˮ�У��������Ӻ��ʵ�鲽���� ��
��4���������ɵ� �����ܽϳ�ʱ�䱣�ְ�ɫ���������� ��
�����ܽϳ�ʱ�䱣�ְ�ɫ���������� ��
�𰸣�
����һ��
��1��ϡH2SO4����м
��2�����
��3���������ɵ� �����Ӵ�O2��
�����Ӵ�O2��
��������
��1��ϡH2SO4����м
��2��NaOH��Һ��
��3�������Թܢ���ڴ��ų��������Ĵ��ȡ����ų���H2����ʱ���ټн�ֹˮ�С���
��4���Թܢ��з�Ӧ���ɵ�H2�������Թܢ���Թܢ����������������룬������ ��Ѹ��������
��Ѹ��������
��������ʵ����Ӧ��������ԭ��ԭ����˼·��
[��7] ��ͬ������������������У��������������ǣ� ��
A. ��������ˮ�� B. ��������������
C. ������������ͭ��Һ�� D. �ô���С�������÷�������ˮ��
�𰸣�D
�������ӵ�ʧ�����غ�ĽǶ��жϣ�ͬʱע��ʵ������ʹ�õ���Ʒ��
[��8] ��������֮���ܹ�������ͼ��ʾ�Ļ�ѧ��Ӧ���Ͻ������ֽ�����ɣ�ȡC��Һ������ɫ��Ӧ�����ʻ�ɫ���ڷ�Ӧ�в�����ˮ��δ��ͼ�б����
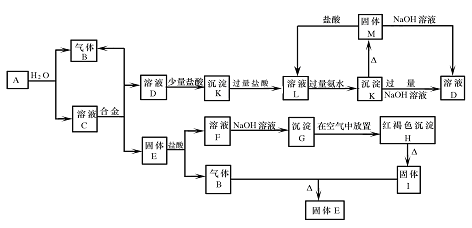
��1��д���������ʵĻ�ѧʽ��A�� M�� H��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ�����������ת�������
GH��
��3��д�����з�Ӧ�����ӷ���ʽ��
AB��C��
KD��
�𰸣���1��A��Na M��Al2O3 H��Fe��OH��3
��2��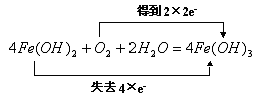
��3��A B��C��2Na+2H2O=2Na++2OH��+H2��
KD��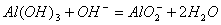
�����������Ԫ�ػ�����֪ʶ���ۺ����á�
��ģ��������������ʱ�䣺30���ӣ�
1. ���ڿ������ܹ��ȶ����ڵ�ԭ���ǣ� ��
A. ���Ļ����Բ� B. ���Ļ�ԭ�Բ�
C. ������������Ӧ D. �����������ܵ�����Ĥ
2. ֻ�������Լ��е�һ�־��ܽ�FeCl3��FeCl2��AlCl3��NaCl������Һ�����ǣ� ��
A. KSCN��Һ B. BaCl2��Һ C. NaOH��Һ D. AgNO3��Һ
3. ��ȥFeCl2��Һ��������FeCl3����õİ취�ǣ� ��
A. ��������������Һ B. ͨ������
C. ����ͭ�� D. ��������
4. ���й����Ƶ������У���ȷ���ǣ� ��
A. ������Ȼ���д�������̬ B. ����һ�ֻ�ɫ�Ĺ���
C. �ƿ��Ա�����ú�ͻ�CCl4�� D. ���Ż�ʱ������ɳ������
5. �����ڵ��Դ������ѹ�Ƶƣ�������Ϊ�� ��
A. �ƵĻ�ԭ��ǿ B. ��ȼ��ʱ������ɫ����
C. ��ѹ�ƵƷ����Ļƹ����Զ������ǿ D. �����Ƶĵ���������
6.�����ݺš����˺������ڣ��Ա�����Ĺ���պͷ��زն����ܷ�ģ�Ϊ�˱�֤�Ա�ں����������������ʵ������� ��Ҫ�ں�����ڷ��루 ��
A. Na2O2 B. Na2CO3 C. NaOH D. ����ƿ
7. �����Ľ����Ƴ��ڱ�¶�ڿ����У��������ղ����ǣ� ��
A. NaOH B. Na2CO3?10H2O C. Na2CO3 D. NaHCO3
8. �й�����ˮ��Ӧ��˵���У���ȷ���ǣ� ��
A. ���κ������£�����ˮ����������Ӧ��
B. �ڸ���ʱ������ˮ������Ӧ��������������������
C. �ڸ���ʱ������ˮ������Ӧ������������������
D. �ڸ���ʱ������ˮ������Ӧ��������������������
9. ��������������ַ�����ȥϸС���������л��е�ϸС��������������Ҫ˵����
 10. ���ڷ�Ӧ��2Na+Cl2��ȼ 2NaCl��˵����ȷ���ǣ� ��
10. ���ڷ�Ӧ��2Na+Cl2��ȼ 2NaCl��˵����ȷ���ǣ� ��
A. Na�ǻ�ԭ����Cl2����������NaClֻ���������
B. ͨ�����ȿ���NaCl�Ʊ�Na��Cl2��
C. ��Ӧ��Cl2ʧȥ����
D. �÷�Ӧ�����з���
11. �ֱ����������ʵ�ˮ��Һ�м��������Ĺ������ƹ��壬������ֻ��ǵ��ǣ� ��
A. �Ȼ�þ��Һ B. ̼�������Һ
C. ��������������Һ D. ����̼��������Һ
12. ��̼��������Һ����������Һ�У��ܷ�Ӧ���ų�������ǣ� ��
A. NaOH��Һ B. ����ʯ��ˮ C. NaHSO4��Һ D. HNO3��Һ
���������
1. D 2. C 3. D 4. D 5. C 6. A 7. C 8. D
9. ����һ������ʹ��NaOH��Һϴ�ӻ�������NaOH��Һ��������Ӧ����Al������NaOH��Һ��2Al��2NaOH��2H2O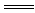 2NaAlO2��3H2���������ˡ�ϴ�ӿ��Եõ�����
2NaAlO2��3H2���������ˡ�ϴ�ӿ��Եõ�����
������������ʹ�ô�����������е�������������������������
���������������м�FeCl2��Һ��Al��FeCl2��Ӧ��2A1��3FeCl2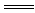 3Fe��2AlCl3����ˮϴ�Ӳ����
3Fe��2AlCl3����ˮϴ�Ӳ����
10. D 11. D 12. CD
�����������
2. �ֱ���ֺ��ɫ��������ɫ������ת��Ϊ���ɫ��������ɫ������������
3. A�ķ���Ӱ����Ҫ���ʣ�B����Ҫ���ʳ�ȥ�ˣ�C�����������ʡ�
4. A��Ϊ�ƵĻ�ѧ���ʻ��ã�����û��������̬���ڵģ�B��ɫ������ɫ��C��Ϊ�Ƶ��ܶ�С��CCl4���ܶȣ����Ը��������棬��Ȼ�ܺ�������Ӧ�����Բ��ܱ��������С�
6. ���ù������ƺͶ�����̼�ķ�Ӧ��
7. �������������������ƣ��ٺ�ˮ��Ӧ�����������ƣ��ٺͶ�����̼��Ӧ����̼���ƾ��壻�����ٷ绯��
10. NaCl��������������ǻ�ԭ���Ӧ�ǵ��ķ�����Cl2�����������õ����ӡ�
11. ����������ˮ��Ӧ�����������ƣ�������������þ��������������þ��������̼���������̼������ӣ������ӳ�����������Һ����������������ˮ������������
12. ̼��������������������ɶ�����̼���塣
�ڶ�ƪ������ϸ����һ��ѧ�����½������仯���ﻯѧ����ʽ�ܽ�
������ �������仯���﷽��ʽ�ܽ�
----------�Ӵֵ��Ƕ�Ӧ�����ӷ���ʽ
1�������ƵĻ�ѧ���ʣ�
��¶�ÿ����б䰵��4Na+O2=2Na2O(��ɫ)
�Ƶ�ȼ�գ�2Na+O2Na2O2(����ɫ)
��Ͷ��ˮ�У�2Na+2H2O=2NaOH+H2�� 2Na+2H2O=2Na++2OH�C+H2��
���������ڡ��Ρ��졢�죩
�������ᣨ�����ˮ����2Na+ 2HCl===2NaCl+H2�� 2Na+ 2H+===2Na++H2��
��������ͭ��Һ����ˮ���Σ���2Na+2H2O+CuSO4=Na2SO4+Cu(OH)2��+H2������ʽ��
2Na+2H2O=2NaOH+H2�� 2NaOH+CuSO4=Cu(OH)2��+Na2SO4
2�������ƵĻ�ѧ���ʣ�
��������ˮ��Na2O+H2O=2NaOH Na2O+H2O=2Na++2OH�C
�������������̼��Na2O+CO2=Na2CO3
�����������Na2O+2HCl=2NaCl+H2O Na2O+2H+=2Na++H2O
3���������ƵĻ�ѧ���ʣ�Ư���ԡ�ǿ�����ԣ���
����������ˮ��2Na2O2+2H2O=4NaOH+O2�� 2Na2O2+2H2O=4Na++4OH�C+O2
���������������̼��2Na2O2+2CO2=2Na2CO3+O2
4��̼������̼�����ƵĻ�ѧ���ʣ�
�ܽ��ԵĵıȽϣ�Na2CO3��NaHCO3
���ԵıȽϣ�Na2CO3�� NaHCO3
���ȶ��ԵıȽϣ�Na2CO3��NaHCO3
Na2CO3+H2O+CO2�� ̼���������ȷֽ⣺2NaHCO3
̼��������ķ�Ӧ��Na2CO3+HCl =NaCl+ NaHCO3 CO32�C+ H+= HCO3-
Na2CO3+2HCl =2NaCl+H2O+CO2�� CO32�C+ 2H+=CO2��+H2O
̼����������ķ�Ӧ��NaHCO3+HCl=NaCl+H2O+CO2�� HCO3-+H+=CO2��+H2O ̼����ת����̼�����ƣ�Na2CO3��NaHCO3����
ͨ��CO2��Na2CO3+H2O+CO2=2NaHCO3 CO32�C+H2O+CO2=2HCO3-
��������ϡ���Na2CO3+HCl =NaCl+ NaHCO3 CO32�C+ H+= HCO3-
̼������ת����̼���ƣ�NaHCO3��Na2CO3����
̼���������ȷֽ⣺2NaHCO3Na2CO3+H2O+CO2������ȥNaHCO3��ѷ�����
���������������ƣ�NaHCO3+NaOH= Na2CO3 + H2O HCO3-+OH-=CO32�C+H2O
5���������Ļ�ѧ���ʣ�
���ڿ����г��»���������¶��������ܵ�����Ĥ�� 4Al+3O2=2Al2O3
����ϡ����ķ�Ӧ��2Al+6HCl===2AlCl3+3H2�� 2Al+6H+=2Al3++3H2��
�����������Ƶķ�Ӧ��2Al+2NaOH+2H2O=2NaAlO2+3H2�� 2Al+2OH�C+2H2O=2AlO2�C+3H2��
ע�⣺1.�������Ļ�����ʵ�������������ϡ������������Ʒ�Ӧ������������������ȵ�
2.��Ӧ�տ�ʼ�Ƚ���������Ϊ���������ܵ�����Ĥ(Al2O3)
3.��Ϊ���ȿ������ᷴӦ�ֿ����������Ʒ�Ӧ�����κ���������������˵Al�����Խ�����
6���������Ļ�ѧ���ʣ����������ʣ�������ˮ���۵�ߣ�Ӳ�ȴ�
��������ϡ����ķ�Ӧ�� Al2O3+6HCl=2AlCl3+3H2O Al2O3+6H+=2Al3++3H2O ���������������Ƶķ�Ӧ��Al2O3+2NaOH=2NaAlO2+H2O Al2O3+2OH�C=2AlO2�D+H2O
ע�⣺��Ϊ�������ȿ������ᷴӦ�����κ�ˮ���ֿ����������Ʒ�Ӧ�����κ�ˮ��������
��˵Al2O3�����������
7�����������Ļ�ѧ���ʣ�
������������ȡ��AlCl3+3NH3��H2O=Al(OH)3��+3NH4Cl Al3++3NH3��H2O=Al(OH)3��+3NH4+ Al2(SO4)3+6NH3��H2O=2Al(OH)3��+3(NH4 )2SO4 Al3++3NH3��H2O=Al(OH)3��+3NH4+ ����������ϡ����ķ�Ӧ��Al(OH)3+3HCl=AlCl3+3H2O Al(OH)3+3H+=Al3++3H2O �����������������Ƶķ�Ӧ��Al(OH)3+ NaOH =NaAlO2+2H2O Al(OH)3+ OH�C =AlO2�C+2H2O
ע�⣺��Ϊ���������ȿ������ᷴӦ�����κ�ˮ���ֿ����������Ʒ�Ӧ�����κ�ˮ������
����˵Al(OH)3�������������
���������ܽ��Բ���ȶ���Ҳ���ã������ֽ⣺2Al(OH)3
8���������Ļ�ѧ���ʣ�
����ˮ�����ڼ��������ķ�Ӧ��3Fe+4H2O(g)
����������ȼ�գ�3Fe+ 2O2Fe3O4 Fe3O4+4H2 Al2O3+3H2O
������ķ�Ӧ��Fe+2HCl = FeCl2+H2�� Fe+2H+= Fe 2++H2��
���Ļ�ԭ��Fe2O3+3CO=2Fe+3CO2(�����Ǹ���)
�����εķ�Ӧ��Fe+CuSO4=FeSO4+Cu Fe+Cu2+=Fe2++Cu
9������������Ļ�ѧ���ʣ�
����������������������������FeO������������Fe2O3����������������Fe3O4��
��������������ķ�Ӧ��FeO+2HCl=FeCl2+H2O FeO+2H+=Fe2++H2O
������������ķ�Ӧ��Fe2O3+6HCl=2FeCl3+3H2O Fe2O3+6H+=2Fe3++3H2O
����������������ķ�Ӧ��Fe3O4+8HCl=FeCl2+2FeCl3+4H2O Fe3O4+8H+=2Fe3++Fe2++4H2O
10��������������Ļ�ѧ���ʣ�
����������������ȡ��FeSO4 + 2NaOH = Fe(OH)2��+ Na2SO4 Fe2+ + 2OH = Fe(OH)2��
�������а�ɫ����������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��
Fe(OH)2������ɫ�ķ���ʽ�ǣ�4Fe(OH)2+O2+2H2O=4Fe(OH)3
��������������ȡ��FeCl3 + 3NaOH = Fe(OH)3��+ 3NaCl Fe3+ + 3OH = Fe(OH)3��
����Ѹ�ٲ������ɫ������
��������������ķ�Ӧ��Fe(OH)2 + 2HCl = FeCl2 + 2H2O Fe(OH)2 + 2H+= Fe2+ + 2H2O ������������ķ�Ӧ�� Fe(OH)3 + 3HCl = FeCl3 + 3H2O Fe(OH)3 + 3H+= Fe3+ + 3H2O
���������ܽ��Բ���ȶ���Ҳ���ã������ֽ⣺2Fe(OH)3Fe2O3+3H2O
11��Fe2+ ��Fe3+֮����ת���������
���������ӣ�Fe3+���ļ���������Һ�е��뼸��KSCN��Һ����ҺѸ�ٱ�ɺ�ɫ������������Fe2+��
�����κ��������漰�ķ���ʽ���˽⣩��Fe3+ + 3SCN- =Fe(SCN)3
������ת��Ϊ��������Fe3 ��+Fe2+����������������ǿ������������ǿ��ԭ���ᱻ��ԭ�ɶ�������
�Ȼ�����ͭ�ķ�Ӧ��FeCl3+Cu=2FeCl2+CuCl2 (�����ܽ�ͭ��·��) 2Fe3++Cu=2Fe2++Cu2+ �Ȼ��������۵ķ�Ӧ�� 2FeCl3+Fe=3FeCl2 2Fe3++Fe=3Fe2+
������ת��Ϊ��������Fe2+ ��Fe3+����������������ǿ��ԭ��������ǿ�������ᱻ��������������
�Ȼ�������Һ��ͨ��������2FeCl2+Cl2=2FeCl3 2Fe2++Cl2=2Fe3++2Cl-
����Fe2+ ��Fe3+��һ���������ǿ����ת���ġ�
12���ص㣺��������
������̼���������Ƶķ�Ӧ��
CO2+2NaOH(����)=Na2CO3+H2O �� 2OH�C+CO2=CO32�C+H2O
Na2CO3+H2O+CO2=2NaHCO3 ���м䷴Ӧ CO32�C+H2O+CO2=2HCO3 -
CO2(����)+NaOH=NaHCO3 ����ʽ+��ʽ�� OH�C+CO2=HCO3�C
������̼���������Ƶķ�Ӧ�������ɳ������������ʧ��
CO2+Ca(OH)2(����)=CaCO3��+H2O�� Ca2++2 OH�C+CO2=CaCO3��+H2O
CaCO3+CO2+ H2O=Ca(HCO3)2���м䷴Ӧ CaCO3+CO2+ H2O=Ca2++2HCO3�C
2CO2(����)+ Ca(OH)2=Ca(HCO3)2����ʽ+��ʽ�� OH�C+CO2=HCO3�C
̼��������ķ�Ӧ��
Na2CO3(����)+HCl =NaCl+ NaHCO3 CO32�C+ H+= HCO3-
Na2CO3+2HCl(����) =2NaCl+H2O+CO2�� CO32�C+ 2H+=CO2��+H2O
�Ȼ������������Ƶķ�Ӧ�������ɳ������������ʧ��
3NaOH+AlCl3(����) =Al(OH)3��+3NaCl �� 3OH�C+Al3+=Al(OH)3��
NaOH+Al(OH)3=NaAlO2+2H2O ���м䷴Ӧ OH�C+Al(OH)3=AlO2�C+2H2O 4NaOH(����)+AlCl3 =NaAlO2+2H2O+3NaCl����ʽ+��ʽ�� 4OH�C+Al3+=AlO2�C+2H2O
ƫ������������ķ�Ӧ�������ɳ������������ʧ��
NaAlO2(����)+HCl+H2O = Al(OH)3��+NaCl �� AlO2�C+H++H2O=Al(OH)3��
Al(OH)3+3HCl=AlCl3+3H2O���м䷴Ӧ Al(OH)3+3H+=Al3++3H2O
NaAlO2+4HCl(����) =AlCl3+NaCl +2H2O����ʽ+��ʽ�� AlO2�C+4H+=Al3++2H2O
��1�����˽⣬������ص�~~~��
������̼��ƫ�����Ƶķ�Ӧ��
CO2(����)+2NaAlO2+3H2O=2Al(OH)3��+Na2CO3 CO2+3H2O+2AlO2�C=2Al(OH)3��+CO32�C CO2(����)+NaAlO2+2H2O=Al(OH)3��+NaHCO3 CO2+2H2O+AlO2�C=Al(OH)3��+HCO3�C
�Ȼ�����ƫ�����Ƶ�˫ˮ�ⷴӦ��
3NaAlO2+AlCl3+6H2O=4Al(OH)3��+3NaCl 3AlO2-+Al3++6H2O=4Al(OH)3��
��2���������仯����֮����ת����
1���Ƽ�����Ҫ������֮���ת����ϵ��д����Ӧ�Ļ�ѧ��Ӧ����ʽ��
3 ��
2����������Ҫ������֮���ת����ϵ��д����Ӧ�Ļ�ѧ��Ӧ����ʽ��
3
3
����������Ҫ������֮���ת����ϵ��д����Ӧ�Ļ�ѧ��Ӧ����ʽ��
Fe3O3��
4�������ƣ�Na���ڿ����г�ʱ����õı��ʹ��̣�
