烃的燃烧计算题的技巧解法
河南商城高级中学 甘继旺
一 基本功
1. 熟练写出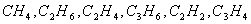 等燃烧的化学方程式
等燃烧的化学方程式
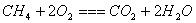
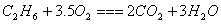
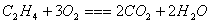

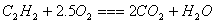
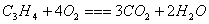
2. 通试燃烧
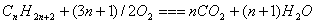
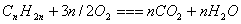
二. 规律总结
1. 元素耗 规律
规律
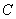 ~
~ , 4H~
, 4H~
2. 气态烃 燃烧高于100 ,气体体积变化规律
,气体体积变化规律
(1)体积变化与C原子无关
(2)nH=4, 气体体积不变化
nH>4, 气体体积变大
nH<4, 气体体积变小
三. 知识拓展
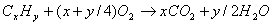 气体体积变化(t>100
气体体积变化(t>100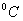 )
)
1 x+y/4 x y/2 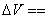 1-y/4
1-y/4
1, 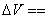 1-y/4==O, y=4
1-y/4==O, y=4
2,  =1-y/4>O, y<4
=1-y/4>O, y<4
3,  =1-y/4<O, y>4
=1-y/4<O, y>4
4, 用此法可以计算烃的平均分子式
四,应用举例
例1,某芳香烃完全燃烧生成水的质量和芳香烃的质量相等,则该芳香烃是
A,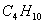 B,
B, C,
C, 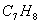 D,
D, 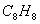
答案:D
简析:烃和水的质量相等,即 C和O的质量相当,取C和O的质量的最小公倍数48,则C原子数应为4,而 的烃不是芳香烃,所以子数应为4的整数倍,即选D
的烃不是芳香烃,所以子数应为4的整数倍,即选D
 例2, 10.0 mL 某气态烃在 50.0 mL O2 中充分燃烧,得到液态水和 35.0 mL 的气体混合物(所有气体的体积都是在同温同压下测得的),该气态烃可能是A.CH4 B.C2H6 C.C3H8 D.C3H6
例2, 10.0 mL 某气态烃在 50.0 mL O2 中充分燃烧,得到液态水和 35.0 mL 的气体混合物(所有气体的体积都是在同温同压下测得的),该气态烃可能是A.CH4 B.C2H6 C.C3H8 D.C3H6
简析:用体积差进行计算: 答案:BD
CxHy(g)+(x+ y/4)O2(g)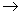 x CO2(g)+y/2
x CO2(g)+y/2 H2O(l) V前-V后
H2O(l) V前-V后
1 1+ y/4
y/4
10.0 ml 10.0+50.0-35.0=25.0 ml y = 6
例3. 某10ml气态烃在50mLO2中恰好充分燃烧,生成气态水,得到同状况下的气体70ml,求该烃的化学式。
简析:CxHy(g)+(x+y/4)O2(g)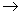 x CO2(g)+
x CO2(g)+ y/2 H2O(g) V前-V后
y/2 H2O(g) V前-V后
1 x+y/4 1-
1- y/4
y/4
10ml 50ml -10ml
根据体积差,得 y = 8
又气态烃恰好充分燃烧,得x + y/4 = 50/10,则x = 3 因此,答案为:C3H8
例4. 室温时20mL某气态烃与过量的氧气混合,完全燃烧后的产物通过浓硫酸,再恢复至室温,气体体积减少了50 mL,剩余气体再通过氢氧化钠溶液,体积又减少了40mL,求气态烃的分子式。
简析:CxHy(g)+(x+y/4 )O2(g)
)O2(g) 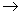 x CO2(g)+y/2
x CO2(g)+y/2 H2O(l) V前-V后
H2O(l) V前-V后
1 x 1+ y/4
y/4
20 ml 40ml 50 ml
根据体积差,得y = 6 又通过氢氧化钠溶液,体积又减少了40mL,说明CO2的体积是40ml,故x = 2因此, 答案为:C2H6
例5. 某气态烃在密闭容器中与O2恰好完全反应,反应后恢复至原室温,测得压强为原来的50%,则该烃可能是( )
A. CH4 B. C2H6 C. C3H8 D. C4H10
简析:CxHy(g)+(x+y/4 )O2(g)
)O2(g) 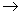 x CO2(g)+
x CO2(g)+ H2O(l) V前-V后
H2O(l) V前-V后
反应前总体积:1+x+y/4 1+y/4
V 50%V
解得,x = 1+y/4 讨论:x和y都是整数,故y是4的倍数,则y=4,x=2,为C2H4若y=8,则x=3,为C3H8答案:C
练 习
1. 在20℃时,某气态烃与氧气混合,装入密闭容器中,点燃爆炸后,恢复到原来的温度,此时容器内气体的压强是反应前的一半。经NaOH溶液吸收后,容器内几乎为真空,此烃的分子式可能为
A. CH4 B. C2H6 C. C3H6 D. C2H4
2. a毫升三种气态烃混合物与足量氧气混合点燃爆炸后,恢复到原来的状态(常温常压)体积缩小2a毫升,则三种烃可能是
A. CH4 C2H4 C3H4 B. C2H6 C3H6 C4H
C. CH4 C2H6 C3H8 D. C2H2 C2H4 CH4
3. 下列各组有机物以等物质的量组成混合物,在氧气中充分燃烧后,生成的CO2和H2O的物质的量之比为1:1的是
A. CH4、C2H4 B. C2H4、C3H6 C. C2H4、C2H2 D. C2H6、C3H6
4、将体积比为1∶1∶2的H2、CO、CH4混合气体VL完全燃烧,所需氧气的体积为:
A.1.25VL B.5VL C.VL D.1.5VL
5、在20℃时,某气态烃与氧气混合,装入密闭容器中,点燃爆炸生,又恢复到原来状态,此时容器内气体的压强为反应前的一半,经氢氧化钠溶液吸收后,容器内几乎成真空,此烃的分子式可能是:
A.CH4 B.C2H6 C.C3H8 D.C2H4
6、a mL三种气态烃与足量的氧气形成的混合物点燃爆炸后,恢复到原来的状态(150℃、1.01×105 Pa)气体体积仍为a mL,则三种烃可能是:
A.CH4、C2H4、C3H4 B.C2H6、C3H6、C4H6
C.CH4、C2H6、C3H6 D.C2H4、C2H2、C4H6
7、下列各组有机物不管它们的物质的量以何种比例混合,只要混合物的物质的量一定,则在完全燃烧时,消耗氧气的量恒定不变的是:
A.C3H6 C3H8 B.C4H6 C3H8 C.C5H10 C6H6 D.C3H6 C3H8O
8、常温下一种烷烃A和一种烯烃B组成的混合气体,A和B分子最多只含4个碳原子,且B分子的碳原子数比A分子中多。该1L混合气体充分燃烧生成2.5LCO2,A和B的可能组合及其体积比为:
A.CH4与C3H6,体积比为1∶3 B.CH4与C4H8,体积比为1∶1
C.C2H6与C3H6,体积比为2∶1 D.C2H6与C4H8,体积比为1∶3
9、标况下,碳原子为n和n+1的两种气态烯烃的混合物1L。其质量为2克,则n值为:
A.2 B.3 C.4 D.不能确定
10、燃烧3克某有机物生成0.1molCO2和1.8克H2O,该有机物的蒸气对H2的相对密度为30,则该有机物的化学式为:
A.C2H4 B.C3H8O2 C.C2H4O2 D.C2H6O
11、充分燃烧等质量的下列各组有机物,在相同条件下需O2的体积不完全相同的一组是
A.C2H2、C6H6 B.HCOOCH3、CH3COOH
C.C3H4、C9H12 D.C3H6、C3H8O
12、50mL三种气态烃的混合物与足量氧气混合点燃爆炸后,恢复到原来的状况(常温常压),体积共缩小100mL,则该三种烃可能是:
A.CH4、C2H4、C3H4 B.C2H6、C3H6、C4H6
C.CH4、C2H6、C3H8 D.C2H4、C2H6、C2H2
13、在常温下常压下,将16mL的H2、CH4、C2H2的混合气体与足量的氧气混合点燃,完全反应后,冷却到常温常压下,体积比原来缩小了26mL,则混合气体中CH4的体积为:
A.2mL B.4mL C.8mL D.无法求解
14、20mL某烃与适量氧气充分燃烧后,生成等体积的CO2和水蒸气,将生成的气体在高温下通过过氧化钠固体,最后得到 40mL氧气(以上体积均在同温同压下测定)。此烃分子式为_______________。
15、含C为83.3%(质量分数)的烷烃的分子式为____________,它的同分异构体为______ __
沸点由高到低的顺序为_________________(填名称)
16,混合烃的燃烧(平均值法)例1. 3LCH4、C2H6 混合气在20L O2中充分燃烧后恢复到原来的室温,余下16.5L气体,求CH4、C2H6的体积。
参考答案:
1, D 2,A 3,B 4,A 5, C D 6,A D 7,C D 8,A B
9, B 10, C 11,D 12, A D 13, B 14

15,



正戊烷》异戊烷》新戊烷 16,2L, 1L
第二篇:烃燃烧的相关计算题
烃燃烧的相关计算题
1、将体积比为1∶1∶2的H2、CO、CH4混合气体VL完全燃烧,所需氧气的体积为:
A.1.25VL B.5VL C.VL D.1.5VL
2、在20℃时,某气态烃与氧气混合,装入密闭容器中,点燃爆炸生,又恢复到原来状态,此时容器内气体的压强为反应前的一半,经氢氧化钠溶液吸收后,容器内几乎成真空,此烃的分子式可能是:
A.CH4 B.C2H6 C.C3H8 D.C2H4
3、已知1mol某气态烃CmHn完全燃烧时,需耗氧气5mol 。则m与n 的关系正确的是:
A.m=8-n B.m=10-n C.m=11-n D.m=12-n
4、a mL三种气态烃与足量的氧气形成的混合物点燃爆炸后,恢复到原来的状态(150℃、1.01×105 Pa)气体体积仍为a mL,则三种烃可能是:
A.CH4、C2H4、C3H4 B.C2H6、C3H6、C4H6
C.CH4、C2H6、C3H6 D.C2H4、C2H2、C4H6
5、下列各组有机物不管它们的物质的量以何种比例混合,只要混合物的物质的量一定,则在完全燃烧时,消耗氧气的量恒定不变的是:
A.C3H6 C3H8 B.C4H6 C3H8 C.C5H10 C6H6 D.C3H6 C3H8O
6、常温下一种烷烃A和一种烯烃B组成的混合气体,A和B分子最多只含4个碳原子,且B分子的碳原子数比A分子中多。该1L混合气体充分燃烧生成2.5LCO2,A和B的可能组合及其体积比为:
A.CH4与C3H6,体积比为1∶3 B.CH4与C4H8,体积比为1∶1
C.C2H6与C3H6,体积比为2∶1 D.C2H6与C4H8,体积比为1∶3
7、标况下,碳原子为n和n+1的两种气态烯烃的混合物1L。其质量为2克,则n值为:
A.2 B.3 C.4 D.不能确定
8、燃烧3克某有机物生成0.1molCO2和1.8克H2O,该有机物的蒸气对H2的相对密度为30,则该有机物的化学式为:
A.C2H4 B.C3H8O2 C.C2H4O2 D.C2H6O
9、充分燃烧等质量的下列各组有机物,在相同条件下需O2的体积不完全相同的一组是
充分燃烧等物质的量的下列各组有机物,在相同条件下需O2的体积完全相同的一组
A.C2H2、C6H6 B.HCOOCH3、CH3COOH
C.C3H4、C9H12 D.C3H6、C3H8O
10、50mL三种气态烃的混合物与足量氧气混合点燃爆炸后,恢复到原来的状况(常温常压),体积共缩小100mL,则该三种烃可能是:
A.CH4、C2H4、C3H4 B.C2H6、C3H6、C4H6
C.CH4、C2H6、C3H8 D.C2H4、C2H6、C2H2
11、在常温下常压下,将16mL的H2、CH4、C2H2的混合气体与足量的氧气混合点燃,完全反应后,冷却到常温常压下,体积比原来缩小了26mL,则混合气体中CH4的体积为:
A.2mL B.4mL C.8mL D.无法求解
12、当分子式为CxHyOz的有机物1mol在O2中完全燃烧,产生CO2和水蒸气的体积相等,并消耗O23.5mol时,该有机物中的x、y的值分别为:
A.1、2 B.2、4 C.3、6 D.4、8
13、20mL某烃与适量氧气充分燃烧后,生成等体积的CO2和水蒸气,将生成的气体在高温下通过过氧化钠固体,最后得到 40mL氧气(以上体积均在同温同压下测定)。此烃分子式为_______________。
14、含C为83.3%(质量分数)的烷烃的分子式为____________,它的同分异构体为________,沸点由高到低的顺序为_________________(填名称)
15、已知甲烷与氧气的混合气体,在有足量过氧化钠存在的密闭容器中,点燃充分反应,总的化学方程式为:2CH4+O2+6Na2O2=2Na2CO3+8NaOH
(1)假设原混合气体中CH4和O2的物质的量分别为x mol 、y mol ,反应后气体的物质的量为n mol ,试确定x与y在不同比值条件下的n值。将结果填入下表:
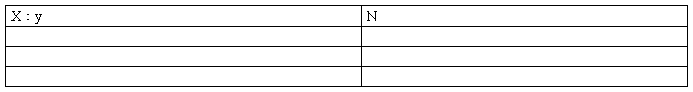
(2)某烃(CxHy)与O2的混合气体在上述条件下反应。若该烃与O2的物质的量之比分别为3∶3和2∶4时,充分反应后剩余气体的物质的量相同。计算推断该烃可能的分子式。
16、A盐和碱石灰微热生成气体B,再升温至500℃以上又生成气体C,在同温同压下,B、C两气体的密度相近,余下残渣与硝酸反应又得到气体D,将D通入一种淡黄色固体中,又可得到一种气体E,试写出上列各物质的化学式及转化的化学方程式。
17、在120℃,101kPa条件下,由H2、CH4、CO组成的混合气体a mL,通入一定量(设为x mL)氧气使其完全燃烧。
(1)若a mL混合气体完全燃烧消耗相同条件下氧气的体积也为a mL(即x= a mL),则原混合气体中CH4的体积分数是_____________。
(2)若完全燃烧后生成CO2和H2O(g)的总体积在相同条件下为2a mL,则原混合气体中CH4的体积分数是_____________。现要测定原混合气体中H2的体积分数,还必须知道相同条件下的其它数据可以是 _____________(填选项字母)
A.2a mL混合气体的密度 B.生成CO2气体的总体积 C.生成H2O(g)的总质量
(3)若使原混合气体完全燃烧,所得混合气体为CO2和H2O(g),则x的取值范围是 _____________。
18、0.2mol有机物和0.4molO2在密闭容器中燃烧后的产物为CO2、CO、H2O(气),产物经过浓H2SO4后,质量增加10.8克,再通过灼热的氧化铜充分反应后,质量减轻3.2克,最后气体再通过碱石灰被完全吸收,质量增加17.6克。试确定该有机物的化学式。
19、在120℃,1体积烃和4体积的O2点燃,充分反应,体积不变,则烃分子中碳原子数的范围为________________
20、有A、B两份混合气体。A是烷烃R和足量氧气的混合气体,B是烷烃R、炔烃Q及足O2的混合气体,在标况下,各取A、B2.24L引燃,A充分燃烧后气体总体积仍为2.24L;B充分燃烧后气体总体积变为2.38L。假使燃烧后的产物均为气态,其体积已换算为标况下的体积,试推算:
(1) 烷烃R和炔烃Q的分子式
(2) 2.24LB中,烷烃R所允许的最大体积是多少?
[答 案]
1、A 2、C D 3、A C 4、A D 5、C D 6、A B 7、B 8、C 9、D;B D
10、A D 11、B 12、C D 13、C2H4
14、C5H12 正戍烷 异戍烷 新戍烷
15
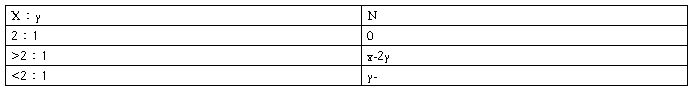
当烃与氧气物质的量之比为2∶3时,两者恰好完全反应
CxHy+  O2+(x+
O2+(x+  )Na2O2====x Na2CO3+yNaOH
)Na2O2====x Na2CO3+yNaOH
有:1∶  ∶3 x=3
∶3 x=3
C3H4 C3H6 C3H8
 16、A.CH3COONH4 B.NH3 C.CH4 D.CO2 E.O2
16、A.CH3COONH4 B.NH3 C.CH4 D.CO2 E.O2
 CH3COONH4+NaOH===CH3COONa+NH3↑+H2O
CH3COONH4+NaOH===CH3COONa+NH3↑+H2O
CH3COONa+NaOH====CH4↑+Na2CO3
Na2CO3+2HNO3===2NaNO3+CO2↑+H2O
2CO2+2Na2O2===2Na2CO3+O2
17、(1)33.3% (2)50% A或B或C  a〈x〈2a
a〈x〈2a
18、C2H6O2
19、由反应方程式可知:1+x+  和
和 
 解得:y=4 x≤3
解得:y=4 x≤3
20、(1)CH4、C4H6 (2)≤0.23L
