专题练习——除杂及离子共存
作者:吴云逸
1、下列各组离子在水溶液中能大量共存的是( )
A. H+、Ba2+、NO3-、OH- B. H+、K+、Cl-、CO32-
C. Na+、Ag+、NO3-、CO32- D. Na+、K+、OH-、SO42-
3、在分开盛放的A、B两溶液中,共含有Na+、Cu2+、Ba2+、Mg2+、OH-、NO3-、
SO42-七种离子两溶液中所含离子各不相同,已知A溶液里含三种阳离子和两种阴离子,其余在B溶液里,则B溶液里所含离子应该是 。
5、分离NaCl、FeCl3和BaSO4的混合物,应选用的一组试剂是( )
A. H2O、AgNO3、HNO3 B. H2O、NaOH、HNO3
C. H2O、NaOH、HCl D. H2O、KOH、HNO3
6、欲除去下列各物质中的少量杂质(括号内的物质为杂质),同时,又不能引入新的杂质,分别写出所加试剂和发生反应的化学方程式。
(1)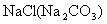 (2)
(2)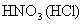
(3) (4)
(4)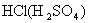
7、除去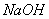 中混有的少量
中混有的少量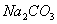 杂质,可加入试剂( )
杂质,可加入试剂( )
A. 盐酸 B. 石灰水 C. 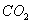 D.
D.  溶液
溶液
8、下列试管内壁的物质能用括号内所给试剂除去的是( )
A. 盛石灰水后留下的固体(氢氧化钠溶液)
B. 用足量 还原
还原 后留下的光亮红色固体(稀盐酸)
后留下的光亮红色固体(稀盐酸)
C. 盛过植物油的试管(热碱液)
D. 氯化铁溶液和氢氧化钠溶液反应后留下的固体(水)
9、下列物质中,不能与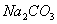 溶液发生反应的是( )
溶液发生反应的是( )
A. 稀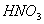 B.
B. 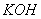 溶液 C.
溶液 C. 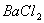 溶液 D.
溶液 D.  溶液
溶液
10、下列各组物质的溶液,两两混合都能发生反应的一组是( )
A. 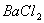 、
、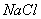 、
、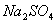 B.
B.  、
、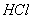 、
、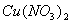
C.  、
、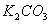 、
、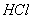 D.
D. 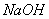 、
、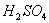 、
、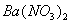
11、硫酸钠溶液中含有少量碳酸钠杂质,除去该杂质可加入适量( )
A. 稀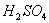 B.
B. 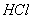 C. 硝酸 D. 石灰水
C. 硝酸 D. 石灰水
12、为了除去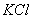 溶液中含有的少量
溶液中含有的少量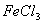 和
和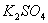 杂质,应依次加入的试剂是( )
杂质,应依次加入的试剂是( )
A. 先加入适量 溶液,再加入适量
溶液,再加入适量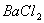 溶液。
溶液。
B. 先加入适量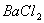 溶液,再加入适量
溶液,再加入适量 溶液。
溶液。
C. 先加入适量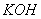 溶液,再加入适量
溶液,再加入适量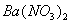 溶液。
溶液。
D. 先加入适量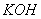 溶液,再加入适量
溶液,再加入适量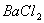 溶液。
溶液。
13、某溶液中大量含有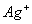 ,
,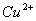 ,
,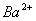 ,三种阳离子中的两种离子和离子
,三种阳离子中的两种离子和离子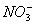 ,
,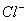 ,
, ,
, 四种阴离子中的两种离子溶液中大量含有的四种离子应该是( )
四种阴离子中的两种离子溶液中大量含有的四种离子应该是( )
A. 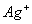 、
、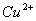 、
、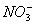 、
、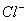 B.
B. 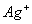 、
、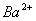 、
、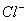 、
、
C. 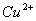 、
、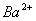 、
、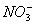 、
、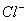 D.
D. 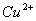 、
、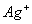 、
、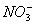 、
、
14、除去硝酸中混有的少量盐酸,可加入的试剂是( )
A. 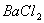 溶液 B.
溶液 B. 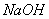 溶液 C.
溶液 C.  溶液 D.
溶液 D. 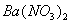 溶液
溶液
15、除去铜粉中混有的少量氧化铜,其主要操作过程是( )
A. 加入过量稀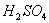 微热后,过滤,洗涤。 B. 加强热或在空气中灼热。
微热后,过滤,洗涤。 B. 加强热或在空气中灼热。
C. 加适量水,加热,过滤,洗涤。 D. 加适量稀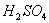 ,微热,过滤,洗涤。
,微热,过滤,洗涤。
16、有 、
、 、
、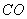 、
、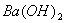 溶液、
溶液、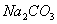 溶液、
溶液、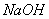 溶液和稀
溶液和稀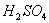 等7种物质,常温下每两种物质间能发生的化学反应有( )
等7种物质,常温下每两种物质间能发生的化学反应有( )
A. 7个 B. 6个 C. 5个 D. 4个
17、工业上食盐水的精制是为了除去粗盐中的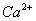 ,
,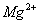 ,
,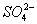 及泥沙,可将粗盐溶于水,然后进行下列五项操作:
及泥沙,可将粗盐溶于水,然后进行下列五项操作:
① 过滤 ② 加过量的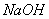 溶液
溶液
③ 加适量的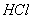 ④ 加过量的
④ 加过量的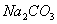 溶液
溶液
⑤ 加过量的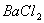 溶液。正确操作顺序是( )
溶液。正确操作顺序是( )
A. ①④②⑤③ B. ④①②⑤③ C. ②⑤④①③ D. ⑤④①②③
18、某溶液中仅含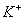 ,
,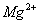 ,
,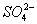 ,
,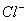 四种离子,其中离子个数比为
四种离子,其中离子个数比为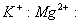
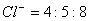 ,若
,若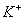 为8m个,则
为8m个,则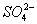 离子个数可能是( )
离子个数可能是( )
A. 1m B. 2m C. 4m D. 6m
19、将下列试剂分别滴入硝酸铜溶液,碳酸钠溶液和稀盐酸中,能观察到三种不同现象的是( )
A. 氢氧化钾溶液 B. 氯化钡溶液 C. 氢氧化钙溶液 D. 氯化钾溶液
20、在不用指示剂的条件下,欲将含有盐酸的氯化钡溶液由酸性变为中性,应选用的最佳试剂是( )
A. 氢氧化钡溶液 B. 硝酸银溶液 C. 碳酸钡粉末 D. 生石灰粉末
21、 某工厂的废渣中混有少量的锌粒和氧化铜(其它成分不跟酸反应),与大量废盐酸接触能形成污水,产生公害,若向污水中撒入铁粉,且反应后铁粉有剩余,此时污水中一定含有金属离子是( )
A. 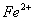 ,
,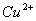 B.
B. 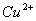 ,
,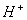 C.
C. 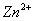 ,
,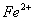 D.
D. 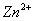 ,
,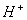
22、当土壤的pH值为4时,农作物不能生长,现要改良它,应撒施的物质是( )
A. 食盐 B. 石灰石 C. 熟石灰 D. 胆矾
23、某溶液中存在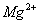 、
、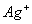 、
、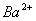 三种阳离子,现用
三种阳离子,现用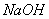 ,
,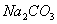 和
和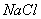 三种溶液使它们转化为沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,则所加溶液的顺序正确的是( )
三种溶液使它们转化为沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,则所加溶液的顺序正确的是( )
A. 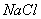 、
、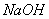 、
、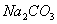 B.
B. 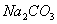 、
、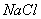 、
、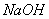
C. 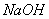 、
、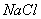 、
、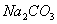 D.
D. 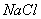 、
、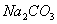 、
、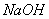
24、某溶液中滴加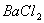 溶液,产生不溶于稀
溶液,产生不溶于稀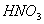 的白色沉淀,则该溶液中可能含有的离子是( )
的白色沉淀,则该溶液中可能含有的离子是( )
A. 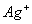 B.
B. 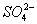 C.
C. 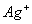 或
或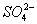 D.
D. 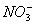
25、下列反应能够一步实现的是( )
A. 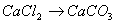 B.
B. 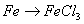
C. 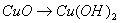 D.
D. 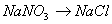
26、在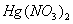 、
、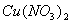 和
和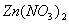 的混合溶液中,加入足量的铁粉,充分反应后,溶液中存在的溶质是( )
的混合溶液中,加入足量的铁粉,充分反应后,溶液中存在的溶质是( )
A. 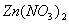 和
和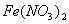 B.
B. 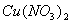 和
和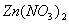
C. 只有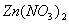 D. 只有
D. 只有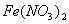
27、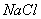 溶液中混有少量
溶液中混有少量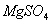 ,若加一种试剂除去,该试剂是 。若加两种试剂除去,应加 和 (写化学式)。
,若加一种试剂除去,该试剂是 。若加两种试剂除去,应加 和 (写化学式)。
28、 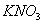 溶液中混入少量
溶液中混入少量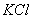 ,可加入 除去
,可加入 除去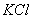 ,实验现象 ,化学方程式 。
,实验现象 ,化学方程式 。
29、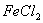 溶液中混入少量
溶液中混入少量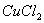 ,可加入 除去
,可加入 除去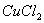 ,现象 ,充分反应经过 (填写实验操作)可得纯净
,现象 ,充分反应经过 (填写实验操作)可得纯净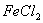 溶液,化学方程式 。
溶液,化学方程式 。
30、选用一种试剂除去硝酸钠中含有的少量硫酸铁,该试剂是 ,选用一种试剂除去硝酸钠中含有的少量氯化钠,该试剂是 。
31、填表:欲除去下表中各物质溶液中含有的少量杂质(括号内的物质为杂质),试分别写出所要加入物质(适量)的名称和发生反应的化学方程式:
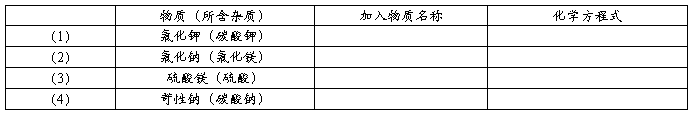
32、含有少量水蒸气、氢气、一氧化碳、二氧化碳的氮气,欲得纯净氮气,可使混合气体先通过足量 ,再通过 ,最后通过 。
33、硝酸钠溶液中含有少量氯化钠、碳酸钠和硫酸钠杂质,欲分别除去这些杂质,可先加入 试剂,除去 ,再向溶液中加入 试剂,除去 ,过滤后再向滤液中加入 试剂,以除去 ,可得纯净硝酸钠溶液。
1、四位同学检验某瓶无色溶液中所含的离子得出如下四种不同的结论,你认为可能正确的是( )
A.FeCl2、Na2SO4、HCl B. NaOH、NaCl、HNO3
C.MgSO4、NaNO3、KOH D. Na2CO3、KNO3、HCl
2、下列各组物质在溶液中能够大量共存,得到无色溶液的是的是( )
A. BaCl2 NaCl H2SO4 B. H2SO4 CuCl2 Na2CO3
C. Na2SO4 KNO3 NaOH D. NaOH H2SO4 NH4Cl
3、下列各组物质在某PH=14的无色溶液中,能大量共存的是( )
A.FeCl3、NaCl、KNO3 B.NaCl、NaOH、NaNO3
C.CaCl2、NaNO3、Na2CO3 D.KNO3、H2SO4、NaCl
4、某溶液能与镁反应生成氢气,则下列各组物质在该溶液中能大量存在的是( )
A.KCl、NaCl、Na2SO4 B.NaCl、NaNO3、AgNO3
C.Na2CO3、NaCl、Na2SO4 D.HCl、NaCl、Na2SO4
5、M和N两溶液中共含有7 种离子:Na+、Cu2+、Ba2+ 、 Mg2+ 、NO3- 、OH-、SO42 - 。已知两种溶液中所含离子不同,M中有4种且能使紫色石蕊试液变蓝。则N 中含有的离子是
6.下列各组物质在水溶液中能大量共存的是:( )
A.NaOH、HNO3、BaCl2
B.Na2SO4、MgCl2、KOH
C.Na2CO3、K2SO4、HCl
D.BaCl2、Na2SO4、AgNO3
E.KNO3、Na2CO3、NaCl
F.K2CO3、Ca(NO3)2、NaOH
7.将下列各组中的溶液混合,能形成无色溶液且无沉淀生成的一组是( )
A.CuSO4、Ca(NO3)2 B.AgNO3、K2CO3
C.Ba(OH)2、H2SO4 D.Na2CO3、HNO3
8.下列各组物质能在pH=1的溶液中大量共存且得到无色溶液的是( )
A.BaCl2、NaNO3、KOH、MgCl2
B.Cu(NO3)2、NaCl、H2SO4、KNO3
C.Na2CO3、NaCl、KNO3、NH4Cl
D.ZnSO4、Mg(NO3)2、NaNO3、KCl
9.下列各组中的离子,在水溶液中能共存的是( )
A.H+、CO32-、Ba2+、NO3-
B.Ca2+、Na+、CO32-、OH-
C.Mg2+、K+、NO3-、Cl-
D.H+、Ba2+、SO42-、NO3-
10.下列各组离子在碱性溶液中能大量共存的是( )
A. NH4+、Cl-、Ba2+、Fe3+
B.Cu2+、Fe3+、Ag+、NO3-
C.H+、SO42+、Cl-、Zn2+
D.Cl–、Na+、Ba2+、NO3-
11.某无色溶液,在pH=0和pH=14的条件下都能共存的是( )
A.Fe2+、K+、SO42-、NO3-
B.Mg2+、NH4+、SO42-、Cl-
C.Na+、K+、Cl-、NO3-
D.Ba2+、Na+、MnO4-、SO42-
12.由Cu2+、Zn2+、K+、NH4+中的一种阳离子和SO42-、
Cl-、NO3-、CO32-中的一种阴离子组成的化合物形成无色溶液,分别加入HCl、AgNO3、BaCl2溶液均无明显现象。该物质可能是( )
A.Cu(NO3)2 B.KCl
C.NH4NO3 D.K2CO3
13.某工厂甲乙两车间排放的废水中分别含有以下五种物质:MgSO4、CuSO4、NaOH、FeCl3、BaCl2中的三种和两种,且甲、乙两车间各自的废水中均无沉淀物。则甲车间废水中含有的三种物质是 、 、 。
14.在强酸性溶液中,可以大量共存的离子组是( )
A.Na+、K+、CH3COO—、Cl— B.Ba2+、Na+、CO32—、NO3—
C.Na+、Ag+、SO42—、Cl— D.K+ 、Fe3+、NO3—、SO42—
15.下列离子能在pH=1的无色溶液中大量共存的是( )
A.Cu2+、SO42-、Cl-、Na+ B.OH-、K+、NO3-、Ba2+
C.Mg2+、SO42-、Al3+、NO3- D.Na+、CO32-、Ca2+、Cl-
16. 将下列各组物质混合后溶于水,得到无色溶液的是( )
A.NaNO3、KCl、Na2SO4 B.FeCl3、NaOH、KNO3
C.CuSO4、CaCl2、KOH D.BaCl2、K2CO3、H2SO4
17、在pH=1的溶液中,能够共存的一组物质是 ( )
A.KCl,NaNO3,H2SO4 B.NH4Cl,NaOH, K2CO3
C.AgNO3,HCl,KNO3 D.CaCl2,Na2CO3,KCl
18. 下列各组物质投入水中,搅拌后能得到无色、澄清溶液的是( )
A.KNO3、HCl、CuCl2 B.Ba(OH)2、BaCl2、、Na2SO4
C.Na2CO3、NaCl、Ca(OH)2 D.NaOH、KCl、H2SO4
19. 室温下,在pH=13的溶液中不可能大量共存的是( )
A.Fe3+、Cl-、SO42-、Na+ B. K+、SO42-、CO32-、Cl-
C.K+、Na+、Ba2+、N03- D. Na+、CO32-、Cl-、K+
20.在水溶液中,一般不会与其它物质发生复分解反应的是( )
A.NaCl B.KNO3 C.NaOH D.H2SO4
21. 室温下,在pH=13的溶液中不可能大量共存的是( )
A.Fe3+、Cl-、SO42-、Na+ B. K+、SO42-、CO32-、Cl-
C.K+、Na+、Ba2+、N03- D. Na+、CO32-、Cl-、K+
22.某工厂排出的废水澄清透明,测得该废水的pH=13,此废水中还可能大量共存的是
A.SO42-、Cl-、Na+、H+ B.K+、SO42-、Cu2+、NO3-
C.Cl-、K+、SO42-、Na+ D.Ca2+、Cl-、CO32-、Na+
23. 向AgNO3、Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后有金属析出,过滤、洗涤后向滤液中滴加稀盐酸,产生白色沉淀,则滤液中一定存在的溶质是( )
A.Fe(NO3)2 、AgNO3 B.Cu(NO3)2 、Fe(NO3)2
C.Fe(NO3)2 D.AgNO3 、Cu(NO3)2 、Fe(NO3)2
24.下列各组物质,只用组内溶液相互混合,不能鉴别出来的是 ( )
A.K2SO4、BaCl2、NaNO3、NaCl B.HCl、Na2CO3、BaCl2、Na2SO4
C.KOH、Na2SO4、CuSO4、HCl D.MgSO4、NaOH、HNO3、FeCl3
25、下列各组物质投入水中,搅拌后能得到无色、澄清溶液的是( )
A.NaOH、KCl、H2SO4 B.KCl、HCl、Cu(NO3)2
C.Na2CO3、NaOH、CaCl2 D.Ba(OH)2、BaCl2、、Na2SO4
26.下列物质的溶液能共存的一组是( )
A.NaCl、BaCl2、KNO3 B.HNO3、AgNO3、FeCl3
C.H2SO4、Na2CO3、BaCl2 D.NH4NO3、NaOH、MgCl2
27、下列离子能在PH = 12的水溶液中大量共存的是( )
A、SO42-、NO3-、K+、H+ B、Na+、Cl-、OH-、Al3+
C、Cl-、NO3-、K+、Na+ D、Ag+、Cl-、CO32-、K+
28.下列离子能在PH = 12的水溶液中大量共存的是( )
A、SO42-、NO3-、K+、H+ B、Na+、Cl-、CO32-、SO42-
C、Cl-、NO3-、K+、Na+ D、Ag+、Cl-、NH4+、K+
29.室温下,在pH=1的溶液中可能大量共存的是( )
A.K+、Cl-、SO42-、OH- B. Na+、SO42-、NO3-、CO32-
C.NH4+、Cl-、NO3-、SO42- D. Ba2+、NO3-、Cl-、SO42-
