2010高考化学试题分类汇编
离子共存 离子反应
(2010,全国卷1,8)能正确表示下列反应的离子方程式是
A. 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
B. 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
C. 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3- =Fe3++2H2O+NO
D. 将铜屑加入Fe3+溶液中: 2 Fe3++Cu=2 Fe2+ +Cu2+
【解析】A错误,不符合客观实际,反应后铁只能产生Fe2和H2;B错误,电荷不守+
恒,Fe3O4中Fe有两种价态,正确应该为:Fe3O4+8H=2Fe3+Fe2+4H2O;C错误,得+++
失电子不守恒,电荷不守恒;正确的应为:3Fe2+NO3+4H=3Fe3+NO↑+2H2O;D正+-++
确,符合3个守恒;
【答案】D
【命题意图】考查离子方程式的正误判断方法!
【点评】离子方程式正误判断是个老生常谈的问题了,本题出得太没有创意了,如D这是个重现率很高的的经典错误,考生绝对做过原题!B项也见得多,一般考查不是用盐酸而是用氢碘酸,有些专家多次指出,磁性氧化铁不溶于任何酸,这样的典型错误在高考题中再次出现,这道题就没什么意思了!A直接取材于课本第二册,C选项,考生也绝对做过,都是太常见不过了! (2010,天津卷,5)下列实验设计及其对应的离子方程式均正确的是
A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe = Cu + 2Fe
B.Na2O2与H2O反应制备O2 :Na2O2 + H2O = 2Na + 2OH + O2↑
C.将氯气溶于水制备次氯酸:Cl2 + H2O = 2H + Cl + ClO+-- +-3+2+2+
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO4 + 6H + 5H2O2 = 2Mn + 5O2↑ + 8H2O
解析:B中元素不守恒,正确的离子方程式为:2Na2O2+2H2O==4Na++4OH-+O2;C中的HClO是弱酸,不能拆成离子形式;D的离子方程式本身没有问题,但KMnO4的强氧化性能将-+2+浓盐酸氧化,不能实现证明H2O2具有还原性的目的(还原性:HCl>H2O2,HCl先反应),D错。
答案:A
(2010安徽卷)9.在pH=1的溶液中能大量共存的一组离子或分子是
A.Na+、Mg2+、ClO—、NO3— B. Al3+、 NH4+、 Br- 、Cl-
C. K+ 、Cr2O72- 、CH3CHO、 SO42- D. Na+、K+ 、SiO32-、Cl-
答案:B
解析:酸性环境下A中生成次氯酸,C中Cr2O72-氧化CH3CHO,D中生成硅酸沉淀。
(2010广东理综卷)7.能在溶液中大量共存的一组离子是
A.NH4+ 、Ag+、PO43-、Cl- B.Fe3+、H+、I-、HCO3-
C.K+、Na+、NO3- 、MnO4- D.Al3+、Mg2+ 、SO42- 、CO32-
解析:A中Ag+和PO43-、Cl-因生成沉淀不共存;B中H+和HCO3-离子生成气体不共存,Fe3+和I-因发生氧化还原反应不共存;D中Al3+和CO32-因互促水解不共存。 答案:C
(2010上海卷,9)下列离子组一定能大量共存的是
A.甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+
B.石蕊呈蓝色的溶液中:Na+、AlO2-、NO3-、HCO3- C.含大量Al3+的溶液中:K+、Na+、NO3-、ClO- D.含大量OH一的溶液中:CO32-、Cl-、F-、K+ 答案:D
解析:此题考查了化学实验中的离子共存知识。使甲基橙呈黄色的溶液pH大于4.4,当其处于4.4-7之间时,NO3-表现强氧化性,将I-氧化为I2,排除A;石蕊呈蓝色的溶液pH大于8,溶液呈碱性,OH-能和HCO3-反应,排除B;含大量Al3+的溶液中,溶液呈酸性,其中的H+能和ClO-结合成HClO,排除C。
(2010,上海化学,19)下列反应的离子方程式正确的是 A.苯酚与碳酸钠溶液的反应
B.等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合
Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液
Fe2++2H++H2O2=Fe3++2H2O
D.淀粉碘化钾溶液在空气中变蓝4I-+O2+2H2O=2I2+4OH-
答案:AD
解析:此题考查了离子方程式的正误判断。苯酚是一种具有弱酸性的有机物,故其在离子方程式中应保留化学式,生成的苯酚钠是强电解质,离子方程式正确,A对;等体积等浓度的碳酸氢钙和氢氧化钠溶液混合时,氢氧化钠不足量,离子方程式为:OH-+HCO3-+Ca2+=H2O+CaCO3↓,B错;反应前后的电荷不守恒,C错;空气中的氧气可以氧化I-为I2,其遇淀粉变蓝,D对。
(2010,江苏,3)下列离子方程式表达正确的是
A.用惰性电极电解熔融氯化钠:2Cl-+2H22↑+H2↑+2OH- B-=2AlO2-+H2O C.用稀氢氧化钠溶液吸收二氧化氮:2OH-+2NO2=NO3-+NO↑+H2O D.用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O
【答案】B【解析】本题主要考查的是离子方程式的正误判断。A项,电解的是熔融状态的NaCl,不是NaCl溶液,2NaCl2Na + Cl2↑;B项,Al2O3能溶于NaOH溶液,生成偏铝酸盐;C项,NO2与NaOH反应,生成硝酸盐和亚硝酸盐,2OH- + 2NO2 = NO3- + NO2- + H2O;D项,水垢中的主要成分为CaCO3,是难溶物。综上分析可知,本题选B项。
(2010江苏卷,6)常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+
B.由水电离的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3- C.c(H+)/ c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl-
D.c(Fe3+)=0.1mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
【答案】C
【解析】本题主要考查的是离子共存问题。A项,由于H+、NO3-与Fe2+发生氧化还原反应而不能大量共存;B项,抑制了水的电离,溶液中存在大量的H+或OH-,但都不能与HCO3-共存;C项,溶液中的c(H+)=0.1mol/L,能与本组离子共存;D项,Fe3+能与SCN-发生络合反应。综上分析可知,本题选C项。 (2010浙江卷)12. 下列热化学方程式或离子方程式中,正确的是:
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
催化剂??????N(g)?3H(g)2(MHg) △H=-38.6kJ·mol-1 ?????22?3500℃、30MPa
g?2OH?Mg(OH)?C. 氯化镁溶液与氨水反应:M 2
lO?2OH??3HO?2Al(OH)D. 氧化铝溶于NaOH溶液:A2322??
试题解析:
本题考查热化学方程式与离子方程式的书写。A、标准燃烧热的定义,1mol可燃物完全燃烧生成稳定氧化物时方出的热量(标准指298K,1atm)。水液态稳定,方程式系数就是物质的量,故A错。B、根据热化学方程式的含义,与
催化剂??????N(g)?3H(g)2(MHg)对应的热量是1mol氮气完全反应时的热?????22?3500℃、30MPa
量,但次反应为可逆反应故,投入0.5mol的氮气,最终参加反应的氮气一定小于0.5mol。所以△H的值大于38.6。B错。D、氢氧化铝沉淀没有沉淀符号。
本题答案:C
教与学提示:
化学用语的教学是化学学科技术规范,强调准确性,强调正确理解与应用。特别重视热化学方程式的系数与反应热的对应关系。重视离子方程式的拆与不拆的问题。热化学方程式的书写问题由:聚集状态、系数、系数与反应热数值对应、反应热单位、可逆反应的反应热等内容构成。离子方程式的书写问题由:强弱电解质、最简整数比、定组成规律、离子方程式正误判断、守恒、定量离子方程式等内容组成。
(2010,四川,9)下列离子方程式书写正确的是
A.向明矾溶液中加入过量的氢氧化钡溶液:
Al3++2SO42-+2Ba2++4OH- =2BaSO4↓+AlO2-+2H2O
B.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O
C.向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH4++OH- =NH3·H2O
D.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:
CH2BrCOOH+OH- → CH2BrCOO-+H2O
答案: A 解析:本题考查离子方程式正误判断;氢氧化钡溶液过量,Al3+转化为AlO2-,SO42-完全转化为沉淀,A项正确;硝酸有强氧化性,可将Fe2+氧化为Fe3+,硝酸被还原为NO,B不符合客观事实,错误;在磷酸二氢铵中加入足量的氢氧化钠,磷酸二氢根离子中的氢将被中和,C项错误;CH2BrCOOH中存在两种官能团,分别是-Br 和-COOH,加入足量的氢氧化钠后加热,与-COOH发生中和反应,与-Br发生水解反应,故应该生成CH2OHCOO-,D项错误。
(2010全国卷1)28.(15分)有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶
液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1) 能确定溶液是(写出溶液标号与相应溶质的化学式):
(2) 不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:
【解析】(I)由题干表述可知A和E不是盐,又由纯E为无色油状液体,推知E为硫酸(③步操作进一步确定);(II)由题干和①步操作可知A为氨水;
+(III)再由②步操作可知F中阳离子为Ag+发生的反应为:Ag+NH3·H2O=AgOH↓
++-+NH4;AgOH+2NH3·H2O=[Ag(NH3)2]+OH+2H2O;而常见的盐中只有AgNO3可溶于水,故F为AgNO3;(IV)由③步操作可知B中阴离子应为CO32-,由于此无色无味的气体只能是CO2, B、C、D中能生成沉淀说明不能是HCO3-,而阳离子可是常见的K+、Na+、NH4+等待定(V)同样由②步操作D中能与氨水生成沉淀的无色溶液中常见的为阳离子为Mg2+或Al3+,而阴离子需待下步反应再确定;(VI)由④步操作生成的沉淀为可能为AgCl、AgBr、AgI、BaSO4、H2SiO3(不合理)等,但限于题干所述中学常用试剂,则沉淀应为AgCl和BaSO4,才不溶于HNO3,一个是与AgNO3结合生成的沉淀,一个是与硫酸结合形成的沉淀,故C应该同时含有Ba2+和Cl-即,C为BaCl2,进而推出D中阴离子应该为SO42-,因为题干所述盐溶液中阴离子均不同,故D为Al2(SO4)3或MgSO4其他解析见答案
【答案】(1)A NH3·H2O或NH3 ;E H2SO4 F AgNO3 C BaCl2 若C作为不能确定的溶液,进一步鉴别的方法合理,同样给分
(2)B Na2CO3或K2CO3 用洁净的铂丝蘸取少量B,在酒精灯火焰中灼烧,若焰色呈黄色则B为Na2CO3溶液;若透过蓝色钴玻璃观察焰色呈紫色,则B为K2CO3溶液
D Al2(SO4)3或MgSO4 取少量D,向其中滴加NaOH溶液有沉淀生成,继续滴加过量的NaOH溶液,若沉淀溶解,则D为Al2(SO4)3溶液,若沉淀不溶解,则D为MgSO4溶液
【命题意图】考查学生的分析与综合能力,涉及到无机元素及其化合物的性质,离子反应,未知物的推断,物质的检验,常见物质量多与量少的反应不同,现象不同等,此题综合性强,难度大,区分度很好,是一道不可多得的经典好题!
【点评】此题一改过去每年元素推断的通病,思维容量显著增大能力要求高,与20xx年全国卷I理综28题有得一拼,比20xx年的第29题出得高超一些,相比以前的无机推断显然有质的飞跃,看到命题人在进步!但是此题是不是一点瑕疵没有呢?x显然不是,例如本题条件很宽广,没太明显的限制条件,因而答案是丰富多彩的,这不会给阅卷者带来喜出望外,只会增加难度,不好统一评分标准,也就缺乏公平性!特别是B和C上就有争议,如B还可能是(NH4)2CO3,C还可能是BaBr2、BaI2等,当然限制一下沉淀颜色就排除了C的歧义!
(2010广东理综卷)32(16分)
碳酸锂广泛应用于陶瓷和医药等领域。以?-锂辉石(主要成分为Li2O?Al2O3?4SiO2)为原材料制备Li2CO3的工艺流程如下:

已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的PH分别为
3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g.
(1)步骤Ⅰ前,?-锂辉石要粉碎成细颗粒的目的是_____________.
(2)步骤Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO42-,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入_____________(填“石灰石”、“氯化钙”或“稀硫酸”)以调节溶液的PH到6.0~6.5,沉淀部分杂质离子,然后分离得到浸出液。
(3)步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有______________.
(4)步骤Ⅲ中,生成沉淀的离子方程式为________________.
(5)从母液中可回收的主要物质是_____________.
解析:(1)粉碎可以增大接触面积,加快反应速率
(2) 要增强溶液的碱性,只能加入石灰石
3+2+2?2+3+e、Mg、Ca(3) H2O2可以氧化Fe为Fe,石灰乳和Na2CO3使得F沉淀
Li+COLiCO?(4) 步骤Ⅲ生成的沉淀是Li2CO3,离子方程式为:2 3=23
(5) 母液中的溶质是NaOH、Na2SO4,可以回收NaOH。 +2-
答案:(1)加快反应速率
(2)石灰石 e、Mg、Ca (3)F
+2-3+2+2?Li+COLiCO?(4)2 3=23
(5)NaOH。
第二篇:高考化学试题分类解析汇编离子反应离子共存
高考化学试题分类解析汇编
离子共存离子反应
[2012·江苏化学卷3]常温下,下列各组离子在制定溶液中一定能大量共存的是
A.0.1 mol·L-1的NaOH溶液:K+、Na+、SO42-、CO32-
B.0.1 mol·L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl-
C.0.1 mol·L-1FeCl3溶液:K+、NH4+、I-、SCN-
D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO3-
A 解析:本题以溶液中离子共存的方式考查学生对Fe3+的氧化性、其硫氰酸盐的难电离性、碘离子的还原性、碳酸钡的难溶性、次氯酸的弱酸性及难电离性等相关知识的理解程度,考查学生综合运用所学化学知识解决相关化学问题的能力。
2.[2012·江苏化学卷9]下列表示对应化学反应的离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I 2+6OH-
B.向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++6OH- NH3↑+H2O
NH3↑+H2O
C.将过量二氧化硫气体入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+
D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++3NO3-=Ag++NO↑+H2O
C 解析:本题是基本概念中离子方程式判断正误的考查,选题以元素化合物基础和生活内容为背景。
A.一定要注意酸性溶液中不能出现OH-。
B.NH4HCO3溶液HCO3-也能与NaOH反应。
C.过量二氧化硫气体入冷氨水只能酸式盐。
D.得失电子不守恒。
【备考提示】高考常设置的错误形式有:离子反应不符合客观事实;各物质化学式拆分错误;不符合“三个守恒”(质量、电荷、电子);不符合有机物官能团性质;反应环境与产物的矛盾;改写是否正确(注意区别胶体与沉淀);隐含的反应是否遗漏(生成物与反应物不共存、隐含的氧化性物质等);方程式与所给的“量”的条件是否切合“过量”,“适量”,“足量”,“少量”等
解此类问题是应做到:
注意“三看”:看反应环境,看操作顺序,看反应物之间量的关系。
牢记“三查”:查物质是否能拆分成离子形式,查三个守恒,查阴阳离子的比例与它们形成化合物时的比例是否相同。
3. [2012·海南化学卷8]两种盐的固体混合物:①加热时有气体产生,②加水溶解时有沉淀生成,且沉淀溶于稀盐酸。满足上述条件的混合物是
A . BaCl2和(NH4)2S04 B . AgNO3和NH4Cl
C.FeCl3和NaHCO3 D. KCl和Na2CO3
AC 【解析】 (NH4)2SO3加热时会分解放出气体,BaCl2和(NH4)2SO3溶于水生成的沉淀为BaSO3,它能溶解于盐酸,故A选项符合题意;B中两种物质溶于水生成的沉淀为AgCl,不能溶解于盐酸,故B选项不符合题意;C中的NaHCO3 受热会分解放出二氧化碳,FeCl3和NaHCO3 溶于水发生互促水解的反应,生成的Fe(OH)3沉淀溶于盐酸,故C选项符合题意;KCl和Na2CO3受热都不分解生成气体,故D选项不符合题意。
4. [2012·海南化学卷12]能正确表示下列反应的离子方程式为
A.碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH–= CO32-+ H2O
B.二氧化硫通入次氯酸钠溶液:SO2 + ClO- + 2OH–= SO42-+Cl-+ H2O
C.硫化钡加入稀硫酸:BaS + 2H+ = H2S↑+ Ba2+
D.新制的氧化铝可溶于氢氧化钠溶液:Al2O3+2OH–=2AlO2–+H2O
BD 【解析】A选项中反应还应该有CaCO3生成, C选项中还有BaSO4生成,故A选项、C选项漏掉部分离子反应,均错;B中因为ClO- 具有强氧化性,故正确;D中的产物、元素、电荷都守恒,正确。
5.[2012·海南化学卷20-I]

【答案】AC
【解析】加入氨水后,Cu2+会生成络合物,不能生成沉淀,故A错;硫酸钠与Cu2+也不会生成沉淀,故C错。H2S与三种离子会生成CuS、HgS和PbS沉淀;纯碱能增大溶液的pH,使三种离子都生成沉淀。
6.[2012·安徽理综化学卷8]下列离子或分子在溶液中能大量共存,通 后仍能大量共存的一组是
后仍能大量共存的一组是
A.
B.
C.
D.
A 【解析】本题考查离子的共存问题,同时考查考生应用知识解决实际问题的能力。C项中Fe2+ 与Cl2不能大量共存,D项中Ag+与NH3·H2O不能大量共存,可排除;A项通入CO2后不反应,仍能大量共存,正确;B项,因SiO2-3+CO2+H2O===H2SiO3↓+CO2-3,故通入CO2后SiO2-3不能大量存在。
7.[2012·安徽理综化学卷13]已知室 温下, 的K,或溶解度远大于
的K,或溶解度远大于 。向浓度均为0.1
。向浓度均为0.1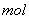

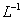 的
的 和
和 混合溶液中,逐滴加入NaOH 溶液。下列示意图表示生成
混合溶液中,逐滴加入NaOH 溶液。下列示意图表示生成 的物质的量与加入NaOH溶液的体积的关系合理的是
的物质的量与加入NaOH溶液的体积的关系合理的是

B 【解析】本题主要考查化学反应的顺序问题,旨在考查考生运用基础知识解决实际问题的能力。因Ksp[Al(OH)3]>> Ksp[Fe(OH)3],因此向混合溶液中滴加NaOH溶液时,首先应生成Fe(OH)3沉淀,当Fe3+ 沉淀完全后,再生成Al(OH)3沉淀,继续滴加NaOH溶液,则Al(OH)3+OH-===AlO-2+2H2O,故B项图像符合实际情况。
8. [2012·重庆理综化学卷11]向10mL 0.1mol·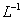
 溶液中,滴加等浓度
溶液中,滴加等浓度 溶液x mL,下列叙述正确的是
溶液x mL,下列叙述正确的是
A.x=10时,溶液中有 、
、 、
、 ,且
,且
B.x=10时,溶液中有 、
、 、
、 ,且
,且
C.x=30时,溶液中有 、
、 、
、 ,且
,且
D.x=30时,溶液中有 、
、 、
、 ,且
,且
【答案】A

9. [2012·广东理综化学卷8]在水溶液中能大量共存的一组是
A 


 B
B 



C 


 D
D 



解析:A.Fe2+和ClO-发生氧化还原反应;B.有氢氧化铜沉淀生成D.有硅酸沉淀生成
10. [2012·四川理综化学卷9]下列离子方程式正确的是
A.钠与水反应:Na+2H2O=Na++2OH-+H2↑
B.硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓
C.0.01mol·L-1NH4Al(SO4)2溶液与0.02mol·L-1Ba(OH)2溶液等体积混合:
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
D.浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+ Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
C【解析】本题考查离子方程式的书写判断。A项的电荷不守恒,A项错误;醋酸是弱酸,不能拆,B项错误;NH4Al(SO4)2与Ba(OH)2以1:2的比值混合,OH—恰与NH4+和Al3+完全反应,C项正确;硝酸与过量Fe反应得到的是Fe2+,D项错误。
【易错警示】离子方程式的正误判断:首先看是否符合客观事实;二看是否可拆,弱电解质、难溶物、单质、氧化物均不能拆;三看电荷是否守恒;四看物质反应的量与滴加顺序。
11.[2012·全国大纲理综化学卷7]能正确表示下列反应的离子方程式是
A 硫酸铝溶液中加入过量氨水  +3OH-=Al(OH)3 ↓
+3OH-=Al(OH)3 ↓
B 碳酸钠溶液中加入澄清石灰水 Ca(OH) 2 + =CaCO3 ↓ + 2
=CaCO3 ↓ + 2
C 冷的氢氧化钠溶液中通入氯气 Cl2 + 2 =Cl
=Cl +
+  + H2O
+ H2O
D 稀硫酸中加入铁粉 2Fe + 6  = 2
= 2 + 3H2 ↑
+ 3H2 ↑
C 【解析】A答案中氨水是弱电解质,应写成分子式,错误;B中澄清石灰水应写成离子形式,错误;D答案中铁粉与稀硫酸反应生成亚铁离子,错误。
【考点】判断离子方程式的正误判时,关键抓住离子方程式是否符合客观事实、化学式的拆分是否准确、是否遵循电荷守恒和质量守恒、氧化还原反应中的得失电子是否守恒等;就能很好的解决问题。
【点评】离子方程式正误判断是个老生常谈的问题了,本题出得没有创意,如D这是个重现率很高的的经典错误,考生绝对做过原题!B项也见得多, A直接取材于课本第二册,C选项,考生也绝对做过,非常常见。
12. [2012·北京理综化学卷7]下列结实实验现象的反映方程式正确的是
A.切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2=Na2O2
B.向AgC1悬浊液中滴加Na2S溶液,白色沉淀变成黑色2AgC1+S2-=Ag2S↓+2C1-
C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2Na2O2=2Na2CO3+O2
D.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
解析:切开的金属钠暴露在空气中,光亮逐渐变暗是因为生成白色氧化钠的缘故,A错误;AgCl的溶解度大于Ag2S溶解度,所以AgCl的悬浊液中加入Na2S溶液可以转化为Ag2S,B正确;过氧化钠在潮湿的空气中生成的白色粘稠物应该是氢氧化钠,C错误;向NaHCO3溶液中加入过量的澄清石灰水,不可能存在CO32—,D错误。答案:B
