第一章 集合与函数概念
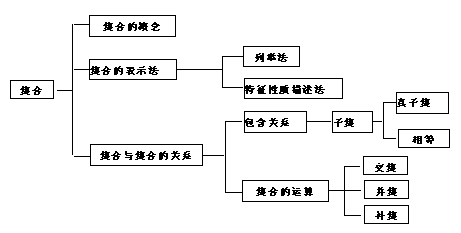
一、集合有关概念
1、集合的含义:某些指定的对象集在一起就成为一个集合,其中每一个对象叫元素。
2、集合的中元素的三个特性:
(1)元素的确定性;{世界上最高的山峰}和{珠穆朗玛峰}
(2)元素的互异性;HAPPY的字母组成的集合{H,A,P,Y}
(3)元素的无序性;{a,b,c}和{a,c,b}是表示同一个集合
说明:(1)对于一个给定的集合,集合中的元素是确定的,任何一个对象或者是或者不是这个给定的集合的元素。
(2)任何一个给定的集合中,任何两个元素都是不同的对象,相同的对象归入一个集合时,仅算一个元素。
(3)集合中的元素是平等的,没有先后顺序,因此判定两个集合是否一样,仅需比较它们的元素是否一样,不需考查排列顺序是否一样。
(4)集合元素的三个特性使集合本身具有了确定性和整体性。
3、集合的表示:{ … } 如{我校的篮球队员},{太平洋,大西洋,印度洋,北冰洋}
(1)用拉丁字母表示集合:A={我校的篮球队员},B={1,2,3,4,5}
(2)集合的表示方法:
列举法:把集合中的元素一一列举出来,然后用一个大括号括上。例如{a,b,c……}
描述法:将集合中的元素的公共属性描述出来,写在大括号内表示集合的方法。用确定的条件表示某些对象是否属于这个集合的方法。{xÎR| x-3>2} ,{x| x-3>2}或{不是直角三角形的三角形}
图示法:
注意:常用数集及其记法:
非负整数集(即自然数集)记作:N
正整数集 N*或 N+ 整数集Z 有理数集Q 实数集R 复数集C
关于“属于”的概念
集合的元素通常用小写的拉丁字母表示,如:a是集合A的元素,就说a属于集合A记作a∈A ,相反,a不属于集合A 记作 a A
①语言描述法:例:{不是直角三角形的三角形}
②数学式子描述法:例:不等式x-3>2的解集是{x∈R| x-3>2}或{x| x-3>2}
4、集合的分类:
(1)有限集 含有有限个元素的集合
(2)无限集 含有无限个元素的集合
(3)空集 不含任何元素的集合 例:{x|x2 =-5}
二、集合间的基本关系
1.“包含”关系— 子集、真子集、非空真子集
注意:(1)A是B的一部分,称为集合A为集合B的子集;记作:A ? B
(2)A与B是同一集合,此时A,B互为包含关系,记作:A? B或B? A。
(3)A是B的一部分,且B集合中至少有一个元素不属于A集合,则称集合A为集合B的真子集,记作:A?B或A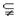 B
B
(4)A是B的一部分,B集合中至少有一个元素不属于A集合,且集合A为非空集合,则称集合A为集合B的非空真子集
(5)任何一个集合是它本身的子集A Í A
(6)如果 A? B, B?C ,那么 A?C
反之: 集合A不包含于集合B,或集合B不包含集合A,记作A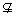 B或B
B或B 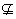 A
A
2.集合的“相等”关系
实例:设A={x|x2 - 1=0} B={-1,1} “元素相同”
结论:对于两个集合A与B,如果集合A的任何一个元素都是集合B的元素,同时,集合B的任何一个元素都是集合A的元素,我们就说集合A等于集合B,即:A=B
① 任何一个集合是它本身的子集。A =A
④ 如果A?B,同时 B?A,那么A=B
3. 不含任何元素的集合叫做空集,记为φ
规定: 空集是任何集合的子集,空集是任何非空集合的真子集。
{Φ}是非空集合
三、集合的运算
1.交集的定义:一般地,由所有属于A且属于B的元素所组成的集合,叫做集合A,B的交集.
记作A∩B(读作“A交B”),即A∩B={x|x∈A,且x∈B}.
2、并集的定义:一般地,由所有属于集合A或属于集合B的元素所组成的集合,叫做A,B的并集。记作:A∪B(读作“A并B”),即A∪B={x|x∈A,或x∈B}.
3、交集与并集的性质:A∩A = A,A∩φ=φ,A∩B = B∩A,A∪A = A,
A∪φ= A,A∪B = B∪A
4、全集与补集
(1)补集:设S是一个集合,A是S的一个子集(即 ),由S中所有不属于A的元素组成的集合,叫做S中子集A的补集(或余集)记作:CsA
(2)全集:如果集合S含有我们所要研究的各个集合的全部元素,这个集合就可以看作一个全集。通常用U来表示。
(3)性质:⑴CU(C UA)=A ⑵(C UA)∩A=φ ⑶(CUA)∪A=U
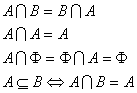
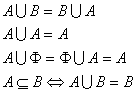
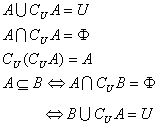
5.映射
一般地,设A、B是两个非空的集合,如果按某一个确定的对应法则f,使对于集合A中的任意一个元素x,在集合B中都有唯一确定的元素y与之对应,那么就称对应f:A B为从集合A到集合B的一个映射。记作“f:A →B”
其中,b称为元素a在映射f下的象,记作:b=f(a); a称为b关于映射f的原像。集合A中所有元素的像的集合成为映射f的值域,记作f(A)。
说明:函数是一种特殊的映射,映射是一种特殊的对应,
① 集合A、B及对应法则f是确定的;
② 对应法则有“方向性”,即强调从集合A到集合B的对应,它与从B到A的对应关系一般是不同的;
③ 对于映射f:A→B来说,则应满足:
(Ⅰ)集合A中的每一个元素,在集合B中都有象,并且象是唯一的;
(Ⅱ)集合A中不同的元素,在集合B中对应的象可以是同一个;
(Ⅲ)不要求集合B中的每一个元素在集合A中都有原象。
典型例题
例1. 已知集合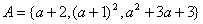 ,若
,若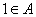 ,求a。
,求a。
(考查)集合元素的确定性和互异性
例2. 已知集合M=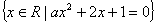 中只含有一个元素,求a的值。
中只含有一个元素,求a的值。
(集合语言的运用)
例3. 已知集合 且B
且B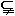 A,求a的值。
A,求a的值。
(真子集和空集)
例4. 设集合 ,
,
(1)若 , 求m的范围;
, 求m的范围;
(2)若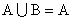 , 求m的范围。
, 求m的范围。
(空集和集合的运算)
例5. 已知A={0,1}, B={x|x A},用列举法表示集合B,并指出集合A与B的关系。
A},用列举法表示集合B,并指出集合A与B的关系。
第二篇:高一化学方程式总结元素化合物化学方程式集锦
氯、溴、碘及其化合物
H2+Cl2=2HCl(爆炸)1.H2+Cl2=2HCl (苍白色火焰)
点燃
光照
2.
MnO2+4HCl(浓)=MnCl2+2H2O+Cl2? (实验室制备Cl2)MnO2+4H+2Cl=Mn+2H2O+Cl2?
+
-?
?
2+
Cu+Cl2=CuCl(棕黄色)3.2Fe+3Cl2=2FeCl3 (棕褐色) 2
点燃点燃
2Na+Cl2 =2NaCl (白烟)
4.Cl2+H2OHCl+HClO (Cl2只有少量的与水反应,大量的Cl2以分子形式存在于水溶液中,所以氯水呈黄绿色)
光照
2HClO2HCl+O2↑(新制氯水久置后成为稀盐酸) 5. Cl2+2NaOH=NaCl+NaClO+H2O 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O (工业生产漂粉精)
漂白原理:Ca(ClO)2+2HCl=CaCl2+2HClO Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO
点燃
Cl2+2KBr=2KCl+Br2 Cl2+2Br-=2Cl-+Br2
6.Cl2+2KI=2KCl+I2 Cl2+2I-=2Cl-+I2
Br2+2KI=2KBr+I2 Br2+2I-=2Br-+I2
7.
AgNO3+NaBr=AgBr?(淡黄色)+NaNO3 Ag++Br-=AgBr?AgNO3+NaI=AgI?(黄色)+NaNO3 Ag++I-=AgI?
8* 2F2+2H2O=4HF+O2
钠、镁及其化合物
1.
4Na+O2=======2Na2O(白色) 2Na2O+O2=2Na2O22Na+O2==2Na2O2 (淡黄色)
点燃
空气中缓慢氧化
?
2Na+S=Na2S (研磨爆炸)
2.
2Na+2H2O=2NaOH+H2? 2Na+2H2O=2Na++2OH-+H2?2Na+2HCl=2NaCl+H2? 2Na+2H+=2Na++H2?*2N+a
Cu4+SO2
2
2
=HO(Cu)2?O+H
+
2
+NS2O4a?
H
2+2N+aCu+2H=O2
Na(+Cu)+H2?2?O
H
3.2NaCl=2Na+Cl2? (工业制备金属钠) 4.Na2O+H2O=2NaOH Na2O+CO2=Na2CO3
2Na2O2+2H2O=4NaOH+O2? 2Na2O2+2H2O=4Na++4OH-+O2?2Na2O2+2CO2=2Na2CO3+O2
(试分析转移电子数)
电解
5..强酸制弱酸:Na2CO3+2HCl=2NaCl+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑
2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑
注意:CaCl2或BaCl2溶液中通入CO2无CaCO3或BaCO3沉淀生成,原因弱酸一般不制强酸 ..常见的弱酸:H2CO3、H2SO3、HClO、H2S、HF、CH3COOH、H3PO4(中强)、H2SiO3 常见的强酸:H2SO4、HNO3、HCl、HBr、HI、HClO4
6.
2-Na2CO3+2HCl=2NaCl+H2O+CO2? CO3+2H+=H2O+CO2?+NaHCO3+HCl=NaCl+H2O+CO2? HCO-3+H=H2O+CO2?
7.Na2CO3
NaHCO3
?+?Na2CO3?
+?3?Na2CO
H=ClC+O2
N+aCl
2
N3aHCO 2- 3+ + = - C3O
2-
2NaH 3 + 2 =C22O3CO +
-
HCO3O2H
HCOHOCO
HCOHO
H=O
--2-
?NaHC+ONa=OHN+aCOHO + = HC+323233O????ONa+CO2+HO?2CO3=23?2NaHC
2NaHCO3+Ca(OH)=Na2CO3+CaCO3?+2H2O2(少)
※
2+2-
2HCO-+2OH-=CO3+CaCO3?+2H2O3+Ca
NaHCO3+Ca(OH)=NaOH+CaCO3?+H2O2(足)
2+HCO-+OH-=CaCO3?+H2O3+Ca
8.NaCl+NH3+CO2+H2O=NaHCO3?+NH4Cl (侯氏制碱法主要反应) 9. CaCO3
高温
CaO+ CO2↑ CaO+H2O=Ca(OH)2
点燃
点燃
10.2Mg+O2=2MgO 3Mg+N2=Mg3N2 2Mg+CO2=2MgO+C
点燃
从铝土矿到铝合金
?Al2O3+2NaOH=2NaAlO2+H2O
?
NaAlO2+CO2+H2O=NaHCO3+Al(OH)3 ? ???1.铝的提取? 2Al(OH)=AlO+HO3232?
电解?
2AlO?23=4Al+3O2??
2.2Al+Fe2O3=2Fe+Al2O3 (铝热反应)利用此反应还可以把其它过渡元素从它们的氧化物(如MnO2、
Fe3O4、Cr2O3、V2O5等)中还原出来但不用来冶炼铁;还可用来焊接钢轨(放出大量的热)
+3+
??2Al+6HCl=2AlCl3+3H2? 2Al+6H=2Al+3H2?3. ? --
2Al+2HO+2NaOH=2NaAlO+3H? 2Al+2HO+2OH=2AlO+3H???222222
高温
+3+??Al2O3+6HCl=2AlCl3+2H2O Al2O3+6H=2Al+2H2O
?--
??Al2O3+2NaOH=2NaAlO2+H2O Al2O3+2OH=2AlO2+H2O
+3+??Al(OH)3+3HCl=AlCl3+3H2O Al(OH)3+3H=Al+3H2O
?--
Al(OH)+NaOH=NaAlO+2HO Al(OH)+OH=AlO+2HO?322322?
3+-?=Al(OH)3?+3NaCl Al+3OH=Al(OH)3??AlCl3+3NaOH(少)
?-+
NaAlO+HCl+HO=Al(OH)?+NaCl AlO+H+HO=Al(OH)??223223(少)?
?=NaAlO2+3NaCl+2H2O Al3++4OH-=AlO-?AlCl3+4NaOH2+2H2O(足)
?3++
AlCl+3NH?HO=Al(OH)?+3NHCl Al+3NH?HO=Al(OH)?+3NH?332(足)343234?
4.Al3++3H2
OAl(OH)3(胶体)+3H+ (水解方程式,明矾的净水原理)
铁、铜的获取及应用
1.H2、CO、Al、C都可以把铁从化合物(FeO、Fe3O4、Fe2O3)中还原出来
2. Fe+SFe 2Cu+SCu2S
2Fe+3Cl2点燃 2FeCl3 Cu+Cl2点燃 CuCl2 FeSO4+2NaOH=Fe(OH)2↓+Na2SO4 4Fe(OH)2+O2+2H2O=4Fe(OH)3
白色沉淀迅速变成灰绿色最后变成红褐色
3.
2+-
???FeCl2+2NaOH=Fe(OH)2?+2NaCl Fe+2OH=Fe(OH)2?????2+O2+2H2O=4Fe(OH)3?4Fe(OH)
Fe2+的检验? 2+3+-
?2FeCl2+Cl2=2FeCl3 2Fe+Cl2=2Fe+2Cl??
??FeCl+3KSCN=Fe(SCN)3+-
33+3KCl Fe+3SCN=Fe(SCN)3???
3+-??FeCl3+3NaOH=Fe(OH)3?+3NaCl Fe+3OH=Fe(OH)3?
4. Fe的检验? 3+-
FeCl+3KSCN=Fe(SCN)+3KCl Fe+3SCN=Fe(SCN)?333?
3+
?Fe+2Fe3+=3Fe2+
?2+3+-+2
?2Fe+Cl=2Fe+2ClCu+2Fe3+=2Fe2+Cu+?22+3+3+2+?5.Fe?Fe?2+ Fe?Fe? 3+2++3+-??*2Fe+H2S=2Fe+S?+2H?2Fe+Br2=2Fe+2Br
?*2Fe3++2I-=2Fe2++I?2
含硅矿物与信息材料
2-
?SiO2+2NaOH=Na2SiO3+H2O SiO2+2OH-=SiO3+H2O?2-2-??Na2SiO3+CO2+H2O=H2SiO3?+Na2CO3 SiO3+CO2+H2O=H2SiO3?+CO3
1. ? 2-+
NaSiO+2HCl=HSiO?+2NaCl SiO+2H=HSiO?323323?2
??
??H2SiO3=SiO2+H2O高温
?
?SiO2+2C=Si+2CO?高温
?高温???SiO2+Na2CO3=Na2SiO3+CO2?
2. 玻璃的生产? 硅的制取与提纯?Si+2Cl2=SiCl4 高温
??SiO+CaCO=CaSiO+CO?高温
2332??SiCl4+2H2=Si+4HCl
??
3.Si+2NaOH+H2O=Na2SiO3+2H2?(类似Al)
SiO2+4HF=SiF4↑+2H2O (用于雕刻玻璃)氢氟酸与玻璃反应因此氢氟酸保存在塑料瓶中
注意:Si不与硫酸、硝酸反应,SiO2不溶于水,不与酸(除氢氟酸)反应
含硫化合物的性质和应用
1.2Al+3S=Al2S3 Fe+S=FeS 2Cu+S=Cu2S Hg+S=HgS 2.
?
?
?
?SO2+Ca(OH)2=CaSO3+H2O
石灰石-石膏脱硫?
?2CaSO3+O2=2CaSO4
?SO2+2NH3+H2O=(NH4)2SO3
?
氨水脱硫?SO2+NH3+H2O=NH4HSO3
?2(NH)SO+O=2(NH)SO
4232424?
3.工业上制硫酸:4FeS2+11O24. SO2+H2O
高温
2Fe2O3+ 8SO2↑2SO2+O2
催化剂
2SO3 SO3+H2O=H2SO4
H2SO3 SO2+2NaOH=Na2SO3+H2O SO2+X2+2H2O=H2SO4+2HX (X=Cl、Br、I)
2H2SO3+O2=2H2SO4 (亚硫酸变质) 2Na2SO3+O2=2Na2SO4 (Na2SO3溶液变质)
5.SO2+2NaHCO3=Na2SO3+ H2O +2CO2 (除CO2中SO2用饱和的NaHCO3溶液,强酸制弱酸) 6. Cu+2H2SO4(浓)CuSO4+ SO2↑+2H2O C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
H2S + H2SO4(浓)=S↓+SO2↑+ 2H2O 2H2S +SO2=3S + 2H2O (若在溶液中进行的S打↓)
生产生活中的含氮化合物
1.
N2 + H2
NH3
(工业合成氨) N2 + O2
2NO 2NO2
N2O4
2. 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+H2O (实验室制氨气)
NH3与CaCl2、CuSO4、浓硫酸都反应,所以干燥NH3不用CaCl2、CuSO4、浓硫酸而用碱石灰
3.
工业上制硝酸:4NH3 + 5O2 4
.NH3 + H2O
NH3·H2O
2NO+O2=2NO2 (红棕色) 3NO2+H2O=2HNO3+NO
4NO + 6H2O NH4++OH-
(大量NH3已转化为一水合氨,一水合氨只有少量电离)
+HCl=NH4Cl(白烟,检验NH3)5.NH3(g) NH3·H2O+HCl=NH4Cl+H2O (g)(s)
2NH3·H2O+MgCl2=Mg(OH)2↓+2NH4Cl 3NH3·H2O+AlCl3=Al(OH)3↓+3NH4Cl (实验室制Al(OH)3)
NH3·H2ONH3↑+H2O NH4ClNH3↑+HCl↑ (NH4)2CO3
6.2NO + O2== 2NO2 4NO + 3O2 + 2H2O==4HNO3
3NO2 + H2O ==2HNO3 + NO 4NO2 + O2 + 2H2O ==4HNO3
2NH3↑+H2O+CO2↑
7.
2+
Cu+4HNO(浓)=Cu(NO3)2+2NO2?+2H2O Cu+4H++2NO-33=Cu+2NO2?+H2O2+3Cu+8HNO(稀)=3Cu(NO3)2+2NO?+4H2O 3Cu+8H++2NO-33=Cu+2NO?+H2O
8HNO3(稀)+3Fe(过量)===3Fe(NO3)2+2NO↑+4H2O 4HNO3(稀)+Fe(不足)===Fe(NO3)3+NO↑+2H2O C+4HNO3(浓)=4NO2↑+CO2↑+2H2O Fe、Al遇冷的浓硝酸、或冷的浓硫酸钝化 HNO3(常见强氧化剂)与H2S、BaSO3、HI、HBr、Fe、S、SO3、I、Br等发生氧化还原反应
2+
2-2---
8.4HNO3
光照
(了解) 4NO2↑+O2↑+2H2O 2CO+2NO=2CO2+N2 (汽车尾气处理)
催化剂
