九 年级 化学科辅导讲义(第讲)
学生姓名: 授课教师: 授课时间:

知识点一介绍:有关化学式的计算
用元素符合来表示物质组成的式子叫做化学式。本知识块的计算关键是抓住这一概念,理解概念的含义,并要深刻理解化学式中各符号及数字的意义,处理好部分与整体之间的算术关系。
1.计算相对分子质量:相对分子质量是指化学式中各原子的相对原子质量的总和。
【例】计算5CuSO4·5H2O的相对分子质量总和。
5CuSO4·5H2O=5×[64+32+16×4+5×(1×2+16)]
=5×[160+5×18]
=1250
2.计算化合物中各元素的质量比:计算的依据是所含元素的质量比,等于微观上每个分子(即化学式)中各种原子的个数与其原子量的乘积之比。
【例】计算氧化铁中铁元素和氧元素的质量比。
氧化物的化学式:Fe2O3,则
Fe∶O=56×2∶16×3=112∶48=7∶3
3.计算化合物中某元素的质量分数:宏观上化合物中某元素的质量分数等于微观上化合物的每个分子中,该元素的原子的相对原子质量总和与化合物的相对分子质量之比,
【例】计算硝酸铵(NH4NO3)中,含氮元素的质量分数。 w(N)= ×100%=35%
练习 将一定量某种铁的氧化物用足量H2还原后,得到33.6g铁,生成14.4g水,如果氧化物中铁与氧的原子个数比为最简比,试求该铁的氧化物的化学式.
知识点二介绍:有关化学方程式的计算
1.有关反应物和生成物的计算:这是化学方程式计算中最基础的题型,要深刻理解化学方程式的含义,理解反应物质和生成物质在微观上和质量上的关系。
【例如】将一氧化碳在空气中点燃后生成二氧化碳的化学反应中,它们的关系:
2CO+O2=2CO2
微粒比:2∶1∶2
质量比:2×28∶32∶88(7∶4∶11)
2.不纯物的计算:纯净物的质量=不纯物的质量×纯净物的质量分数
【例】用含Fe2O3 75%的赤 铁矿石20吨,可炼出含杂质4%的生铁多少吨?
解:20吨赤铁矿石中含纯Fe2O3的质量为:20吨×75%=15吨
设可炼出含杂质4%的生铁质量为x
Fe2O3+3CO=2Fe+3CO2
160 112
15吨(1-4%)x
x==12.5吨
3.选量(过量)计算:化学方程式计算的理论依据就是质量守恒定律。在质量守恒定律中,“参加反应的各物质的质量总和,等于反应生成的各物质的质量总和”。要着重理解“参加”两个字的含义,即没有“参加”反应的物质,就不应计算在内。
【例】今有氢气与氧气的混合气共20克,在密闭的容器中点燃,生成水18克,则下列分析正确的是()
(A)氢气10克,氧气10克(B)氢气2克,氧气18克
(C)氢气4克,氧气16克(D)氢气1克,氧气19克
4.多步反应的计算:从一个化学反应中求出的质量,用此量再进行另一个化学反应或几个化学反应的连续计算,求最后一个化学反应的量,一般称之为多步反应的计算。
【例】计算用多少克的锌跟足量稀硫酸反应生成的氢气,能跟12.25克的氯酸钾完全分解后生成的氧气恰好完全反应生成水。
本题涉及三个化学反应:
Zn+H2SO4(稀)=ZnSO4+H2↑ 2KClO3=2KCl+3O2↑ 2H2+O2=2H2O
可以用三个化学方程式中的微粒关系,找出它们的已知量与未知量的关系式:
2KClO3~3O2~6H2~6Zn即KClO3~3Zn
关于化学方程式计算的解题要领可以归纳为:
化学方程式要配平,需将纯量代方程;
量的单位可直接用,上下单位应相同;
遇到有两个已知量,应找不足来进行;
遇到多步的反应时,关系式法有捷径。
知识点三介绍:有关溶液的计算 :溶质质量+溶剂质量=溶液质量
1.溶解度的计算
固体物质溶解度的概念是:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
2.溶液中溶质质量分数的计算:溶液中溶质质量分数的计算式如下:
溶质质量分数的计算题可以有:
(1)已知溶质和溶剂的质量,求溶液的质量分数。
(2)已知溶液的质量和它的质量分数,求溶液里所含溶质和溶剂的质量。
(3)将一已知浓度的溶液加入一定量的水进行稀释,或加入固体溶质,求稀释后或加入固体后的溶液的质量分数。
【典型例题】
例1 一定质量的KClO3和MnO2的混合物中,MnO2的质量分数为20%,加热后,剩余的固体混合物中MnO2的质量分数升高至25%,则KClO3的分解率是多少?63.8%
例2 将4gH2和O2的混和气体点燃,使其充分反应,得到1.8g水蒸气,则反应前混合物中O2不少于 g,不超过 g. O2不少于1.6g,不超过3.8g.
例3 质量相同的下列金属分别和足量盐酸反应,产生H2最多的是( )
A.Mg B.Al C.Zn D.Fe
规律:在金属质量相同时产生H2质量与该金属的化合价与相对原子质量之比成正比
例4 0.92g金属Cu与CuO的混合物被H2完全还原后,得到0.752g固体剩余物.求原混合物中含CuO的质量分数?91.3%
【同步练习】
1、学习了酸和碱的知识后,小松知道了白醋的主要成分是醋酸(CH3COOH)。为了测定白醋中醋酸的质量分数,他把4%的NaOH溶液滴加到30 g白醋中,待反应恰好完全时(假定其他成分不参加反应),共用去NaOH溶液25 g。
(1)已知反应的化学方程式为:CH3COOH+NaOH=CH3COONa+H20,该反应的类型是____________。
(2)请计算白醋中醋酸的质量分数。(5%)
3、(广东汕头)某同学为探究铁合金中铁的质量分数,先后进行了三次实验,实验数据如下表:
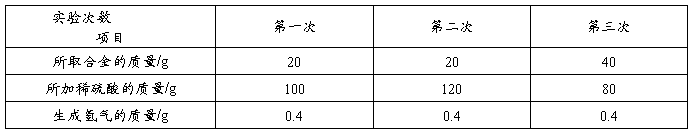
根据该同学的实验,试回答以下问题:
(1)上表三次实验中,合金里的铁恰好完全反应时,消耗稀硫酸溶液的质量是______g。
(2)该铜铁合金中铁的质量分数是多少?
(3)第三次实验所得溶液溶质质量分数为____________(结果保留至0.1%)。
((1)80g(2)56%(3)33.5%)
4、(河北)某钢铁厂检验员为了检测赤铁矿石中氧化铁的质量分数,取矿石
样品20g,加入稀盐酸,完全反应后,共用去稀盐酸219g,过滤
得到滤渣4g(假设杂质既不溶于水也不跟酸发生反应)。
请你和检验员一起完成下列计算:
(1)赤铁矿石中氧化铁的质量分数;(2)稀盐酸中溶质的质量分数。
赤铁矿石中氧化铁的质量分数为80%,稀盐酸中溶质的质量分数是10%
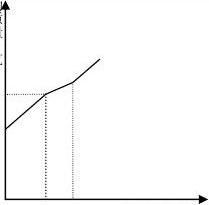
5、(济南)在一烧杯中盛有100gBaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示:
请根据题意回答问题:
(1)在实验过程中,有气体放出,还可以看到的明显实验现象是 。
(2)在实验过程中放出气体的总质量为 g。
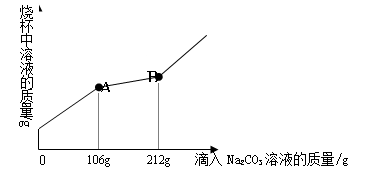 (3)当滴入Na2CO3溶液至图中B点时,通过计算求此所得不饱和溶液中溶质质量分数是多少?(计算结果精确到0.1%)
(3)当滴入Na2CO3溶液至图中B点时,通过计算求此所得不饱和溶液中溶质质量分数是多少?(计算结果精确到0.1%)
(1)生成白色沉淀 (2)4.4 (3)8.1%
6、(济宁)东方中学课外活动小组在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量未知质量分数的氯化钡溶液,实验数据见下表:

若有关的化学反应为:Na2SO4+BaCl2=BaSO4↓+2NaCl,请计算:
⑴未知氯化钡溶液的质量分数为多少。
⑵原混合物中硫酸钠的质量分数是多少。 (精确到0.01)
⑴未知氯化钡溶液的质量分数为8.32%。
⑵原混合物中硫酸钠的质量分数是28.4%
8、(荆州)镁易被空气中的氧气氧化成氧化镁。现有一卷标签上标明120 g 的镁带,称其质量为136 g(假设除镁被氧化外,没有发生其他任何变化,且氧化是均匀的)。试计算(1)被氧化的镁的质量是多少克?
(2)称取上述变质的镁带6.8 g 加入到足量的盐酸溶液中反应,试计算反应产生氢气的质量是多少克?
(24g 0.4g)
【提升练习】
一、选择题(6×10= 60分)
1.甲、乙两人各取2克锌分别与足量的稀H2SO4和稀HCl反应制得的氢气是( )
A.甲的多 B.一样多 C.乙的多 D.无法比较
2.氧化铜跟氢气反应时,如果生成36克水,则被还原的CuO的质量是( )
A.40克 B.60克 C.80克 D.160克
3.完全分解等质量的下列物质:水、KClO3、KMnO4、HgO、得到O2最多的是( )
A.KClO3 B.KMnO4 C.HgO D.H2O
4.2.4g镁、2.7g铝、5.6g铁、6.5g锌分别与足量的稀H2SO4反应,得到H2的质量比依次是( )
A. 1∶1∶1∶1 B.2∶3∶2∶2
C.3∶1∶1∶2 D.1∶2∶2∶3
5.金属X与盐酸反应能生成XCl2,已知9.6g该金属与足量盐酸反应放出0.8gH2,则金属X的相对原子质量是( )
A.24 B.40 C.56 D.65
6.有A和B两种物质,在一定条件下反应生成C和D,已知2克A能和5克B恰好完全反应,生成4克C和3克D,现有6克A和20克B经充分反应后,下列说法正确的是( )
A.生成 C和 D质量之和为26克 B.生成12克 C
C.有1克A剩余 D.生成 10克 D
二、填空题(2×10= 20分)
7.每 份质量P与 份质量O2充分反应生成 份质量的P2O5.
8.加热 克KMnO4可生成6.4克O2,完全反应后剩余固体是
和___________,其质量分别是 和 .
三、计算题(2×10=20分)
9.将109铁与509稀H2SO4反应完毕后,取出剩余的铁,洗涤、干燥后,称其质量为3g.试回答:可制得氢气多少升?(标况下ρH2 = 0.09g/L)
10.将铜和氧化铜的混合物209,用足量的H2还原,待反应完全,得到固体铜16.8g,求:
(1)反应用掉的H2质量是多少?。
(2)原混合物里CuO的质量分数?
【素质优化训练】
3.将锌和ZnSO4的混合物20.8g,放入179.6g稀H2SO4中,完全反应后得到200gZnSO4溶液.求:
(1)原混合物中Zn的质量分数?
(2)把200gZnSO4液中的水蒸干,可得到ZnSO4固体多少g?
【知识验证实验】
甲、乙两同学在实验室用氯酸钾加热制取氧气的过程中,假如没有二氧化锰,可以加少量高锰酸钾,同样可以使氨酸钾很快放出氧气.甲同学认为是高锰酸钾起了催化作用,乙同学认为是高锰酸钾分解产生的二氧化锰起了催化作用.你同意谁的观点?并用化学方程式表达你的观点.
【知识探究学习】
难题巧解:锌、铁、镁的混合物4g,与足量的稀H2SO4完全反应,蒸发水份后,得到固体物质1g,试计算生成的氢气的质量?

第二篇:初中化学精编计算题总汇
计算题
1、 将150ml稀盐酸(密度1.1g/cm3)加入到盛有53g含少量杂质的石灰石的烧杯中,恰好反应(石灰石杂质不溶于水,也不与盐酸及生成物反应),反应后烧杯中物质的总质量为196g。计算:(1)反应生成的二氧化碳的质量。
(2)石灰石中碳酸钙的质量分数。(3)生成物溶液中溶质的质量分数。
2、硝酸铵是农业生产中常用的化肥。为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取2.0g该硝酸铵样品于容器中,滴入5.0g20%的NaOH溶液。发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O.反应过程中放出
的氨气质量及加入的NaOH溶夜的质量的关系如图所示。求:(1)NH4NO3中各元素的质量比(H:N:O)(2)样品中硝酸铵的质量分数。(3)所得溶液中的NaNO3质量分数 氨 气的质量∕
克
3、 我国约在南北朝时就开始冶铸黄铜,黄铜是铜和锌的合金(Cu—Zn),它可以用来制造机器、电器零件及日用品。为了测定某黄铜样品中锌的质量分数

试求:(1)m= g
(2)此黄铜样品中锌的质量分数是多少?
(3)所用稀盐酸的溶质质量分数是多少?
4、现有氧化铜和铜的混合物,对其成分进行分析。取10g此样品,向其中分五次加入相同溶质质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量及
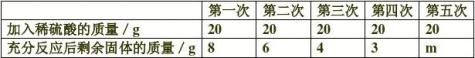

试回答下列问题:
(1)表格中m的值为 ,10g样品中CuO的质量 g
(2)计算所加入稀硫酸中溶质的质量分数?
(3)计算第三次加入稀硫酸反应后所得溶液中溶质的质量分数?
5、有两种外观类似黄金的①Cu—Zn合金和②Cu—Ag合金制品,若实验室只提供一瓶稀硫酸和必要的仪器。
(1)你认为能测出合金 (填序号)中铜的质量分数。
(2)取上述(1)中的合金粉末20g放入烧杯中,加入50g的稀硫酸,恰好完全反应,测得烧杯剩余物的质量为69.8g。求①产生氢气的质量;②该合金中铜的质量分数;③反应后所得溶液中溶质的质量分数。
6、铁是人体必需的微量元素,它是血红蛋白的成分,能帮助氧气的运输。缺少铁元素,易患缺铁性贫血。医学上常用硫酸亚铁糖衣片给这种病人补铁。现取20粒糖衣片,质量为10g,溶于40g水中。向所配溶液中滴加氯化钡溶液至略过量,过滤、洗涤、干燥,称量沉淀质量为2.33g。试计算:(1)该糖衣片中硫酸亚铁的质量分数(2)1粒糖衣片中铁元素的质量
7、为了测定某赤铁矿中氧化碳的质量分数,取矿石样品40g,加入稀盐酸,恰好完全反应时共用去盐酸219g,过滤、洗涤、干燥后得滤渣8g(矿石中的杂质既不溶于水也不与盐酸反应)。计算:(1)赤铁矿中氧化铁的质量分数;(2)盐酸的溶质质量分数。
8、水垢的主要成分是CaCO3和Mg(OH)2,为了测定其中CaCO3的含量,取100g水垢,加入过量稀盐酸,测量5min内生成的CO2的质量,绘出如图所示的曲线,请问:(1)该水垢中CaCO3的质量分数为多少?(2)假定水垢中不含其它杂质,若要计算反应消耗的稀盐酸的质量,还需知道什么信息?
CO2
的
质
量/
g 30
20
10
min
9.某研究性学习小组在协助老师清理实验室时,发现一批存放多年的氢氧化钙。为研究其变质情况,进行了如下探究:取氢氧化钙样品11.4g于锥形瓶中,加入
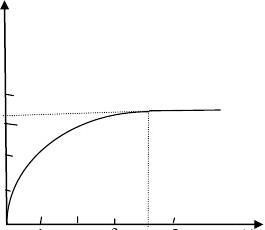
38.6g水,振荡形成悬浊液,放在电子天平上,向锥形瓶中逐滴滴入14.6℅的稀盐酸,振荡后读取质量。实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图所示。求:11.4g样品中各成分的质量。
锥形瓶中物50
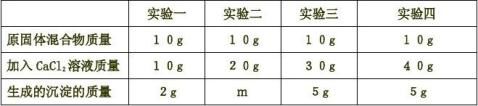
10.课外活动小组的同学在测定由NaCl和Na2CO3形成的固体混合物组成时,进行了以下实验:取40 g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表: 请分析表中数据回答并计算
(1)生成的沉淀是(填写化学式) 。
(2)10g原固体混合物配成的溶液和足量CaCl2溶液反应, 最多生成沉淀质量为 g。 (3)m= g。
(4)原固体混合物中Na2CO3的质量分数是多少?
11、某课外兴趣小组对实验室中的一瓶稀硫酸进行分析。他们分别用100g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表。
g

(1)第次实验,锌粒与稀硫酸恰好反应。
(2)计算稀硫酸中溶质的质量分数。
12、用“侯氏制碱法”制得的纯碱常含有少量的氯化钠(假定只含有氯化钠杂质)。称量某纯碱样品12g,全部溶解在100g水中,所得溶液与160g氯化钙溶液混合,恰好完全反应。过滤干燥后,称得沉淀质量为10g。请计算:
(1)纯碱样品中碳酸钠的质量分数。
(2)反应后所得滤液中溶质的质量分数。
13、长期饮用溶有较多钙、镁离子的水容易引起结石病症,加热可使水中钙、镁离子转化为沉淀——水垢,它的主要成分是CaCO3、Mg(OH)2.为确定水垢的成分,社会实践小组进行了下面实验:
①称取5g水垢样品研碎后放入100mL烧杯中,然后注入50g10℅的稀盐酸 ②反应停止后,反应混合物的质量共减少1.54g
③另取少量水垢放入实验②的混合物中,有气泡产生。
请根据以上信息回答:
(1) 实验③的目的是--------------------------------
(2) 计算水垢样品中碳酸钙的质量分数(精确到0.01)
14、 今年全国人大和政协会议使用了一种含碳酸钙的“石头纸”:为测定其
中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,
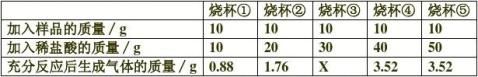
;
(2)、烧杯④中物质充分反应后所得溶液的质量为 ;
(3)、求样品中碳酸钙的质量分数。
