化学计算题
(一)化学式的计算
第一种类型:标签型化学式计算题:
(2011 甘肃兰州)在现代生活中,人们越来越注重微量元素的摄取。碘元素对人体健康有至关重要的作用。下表是某地市场销售的一种“加碘食盐”包装袋上的部分说明。

请回答下列问题:
(1)由食用方法和贮藏指南可推测碘酸钾(KIO3)的化学性质之一是____;
(2)计算碘酸钾(KIO3)中,钾元素、碘元素、氧元素的质量比______;
(3)计算碘酸钾(KIO3)中,碘元素的质量分数是多少?______;(计算结果精确到0.01,下同)
(4)计算1kg这样的食盐中,应加入____g碘酸钾(用最高含碘量计算)
第二种类型:叙述型化学式计算题:
(2010四川)蛋白质是由多种氨基酸[丙氨酸:CH3CH(NH2)COOH等]构成的极为复杂的化合物,人体通过食物获得蛋白质,在胃肠道里与水发生反应,生成氨基酸,试计算:
(1)丙氨酸分子中氮原子与氧原子的个数比__。(2)丙氨酸的相对分子质量_____。
(3)丙氨酸中碳、氢、氧、氮元素的质量比_______。
第三种类型:综合型化学式计算题:
(2011徐州市)青少年正处于生长发育时期,每天需要摄取足量的蛋白质,蛋白质的代谢产物主要是尿素[CO(NH2)2]。若从食物中摄取的蛋白质经体内新陈代谢后完全转化为尿素排出体外,每人每天相当于排出尿素30g。
(1)30g尿素中含氮元素多少克?
(2)已知蛋白质中氮元素的平均质量分数为16%,则每人每天至少应从食物里摄取的蛋白质为多少克?
(3)请你根据下表中几种常见食物的蛋白质含量,计算出每天至少应摄人多少克下列食物才能满足你对蛋白质的需求(可以只摄取一种食物,也可同时摄取几种食物)。

归纳:化学式的计算的关键是会看化学式,如丙氨酸:CH3CH(NH2)COOH,是由几种元素组成,一个分子中几个原子,各种原子的个数比,(再往细处看,一个分子中含有多少个原子核,多少个质子,多少个电子……),那么看懂化学式后,相对分子质量,原子个数比,元素质量比,纯净物(混合物)中元素质量分数,纯净物(混合物)中元素质量,不就是一个数学方程或数学表达式吗?至于题目中所给的具体问题情境,看懂题意,按图索骥,列方程或列式子即可。注意:混合物中某纯净物的质量分数等于某元素在混合物中的质量分数除以该元素在该纯净物中的质量分数乘100﹪。如,某不纯的尿素化肥含氮元素的质量分数是40﹪,试求尿素的质量分数。
(二)有关化合价的计算:
(2011成都市)据报道,“第三代”瓷珠圆珠笔问世,该圆珠笔的球珠有氧化锆陶瓷材料制成,这种材料的应用使球珠的耐腐蚀性,耐磨性得到了提高,从而填补了国内空白,氧化锆的化学式为ZrO2,在氧化锆中锆元素的化合价为:
A.+2 B.+3 C.+4 D.+5
归纳:化合物中各元素的化合价的代数和为0,特别注意:过氧化氢,过氧化钠中氧元素的化合价是―1而不是―2价。
(三)有关化学方程式的计算题:
(1)有关反应物和生成物的计算
(2011北京市)工业上使用一种“渗铬(Cr)技术”可以大大提高钢铁制品的抗腐蚀能力。其中一个主要反应的化学方程式为 。已知参加反应铁的质量28g,则生成铬的质量为多少克?
。已知参加反应铁的质量28g,则生成铬的质量为多少克?
特别注意:1、配平了吗?2、化学式写对了吗?
(2)含有杂质的反应物和生成物的计算
某炼铁厂用含氧化铁80%的赤铁矿冶炼生铁。若要炼出1120t含铁95%的生铁,需要含氧化铁80%的赤铁矿多少吨?
注意:计算时,混合物的质量要转化成纯净物的质量代入方程。
(3)标签型化学方程式的计算
(2010鄂州市)消化药片所含的物质能中和胃里过多的胃酸。某种消化药品的标签如图4所示。医生给某胃酸过多的患者开出服用此药的处方为:每日3次,每次2片。试计算,患者按此处方服用该药一天,理论上可中和HCl多少毫克?(计算结果取整数)
 归纳:看懂题意,不就是化学反应中涉及混合物的计算嘛。
归纳:看懂题意,不就是化学反应中涉及混合物的计算嘛。
(4)有关混合原料参加反应的化学方程式的计算
(2011德阳市)将26g某金属混合物投入到足量的稀硫酸中,共收集到2g氢气,该金属混合物的组成可能是( ) A、Mg和Zn B、Fe和Zn C、Zn和Cu D、Cu和Fe
归纳:一般说来,混合金属的计算,用极值法。记住一个规律:生成一克氢气,需可反应金属的质量是金属的相对原子质量除以该金属的化合价,需不反应金属的质量是无穷大。生成一克氢气,需镁12克,锌32、5克,铁28克,铝9克,铜很多很多也生不成氢气。当然,本题所给的反应金属都是二价的,相对简单一些。生成两克氢气,需镁的质量是24克,需锌的质量是65克,需铁的质量是56克,铜不反应,故生成两克氢气,需镁锌混合物的质量介于24克到65克之间,需铁锌混合物的质量介于56克到65克之间,
需锌铜混合物的混合物的质量大于65克,需铁铜混合物的混合物的质量大于56克。
(5)有关字母型化学反应方程式计算题
(2012南通市) A、B、C三种物质各15 g,它们化合时只能生成30 g新物质D。若增加10 g A,则反应停止后,原反应物中只余C。根据上述条件推断下列说法中正确的是
A.第一次反应停止后,B剩余9 g B.第二次反应后,D的质量为50 g
C.反应中A和B的质量比是3∶2 D.反应中A和C的质量比是5∶2
(6)有关表格型化学方程式计算题
(2010青岛市)在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下表:

下列说法错误的是
A该反应是分解反应 B甲可能是 该反应的催化剂
C乙、丙变化的质量比为9:8 D反应后甲的质量为0g
归纳:(5)(6)两型是考察质量守恒定律。
(四)有关溶液的计算题:
(1)直接使用公式计算:
(2011天津市)将100g10%的某固体物质M的溶液,分别进行下述操作,所得溶液中溶质的质量分数最小的是( )
A. 蒸发掉10g水,无晶体析出 B. 加入10g10%的M的溶液
C. 加入10g固体M,并使之完全溶解 D. 加入10g水
(2)溶质、溶剂的变化对质量分数的影响:
①增加溶剂(加水稀释)
(2012常州市)如要将100g溶质质量分数为20%的硝酸钾溶液稀释成溶质质量分数为10%的硝酸钾溶液,需加入水的质量为
A.50g B.90g C.100g D.200g
②溶液增浓问题:(蒸发溶剂法 增加溶质法 增加浓溶液法)
(2012 重庆市)电解水时,常常要加入少量氢氧化钠使反应容易进行。现将加有氢氧化钠的水通电一段时间后,产生lg氢气,其中氢氧化钠的质量分数也由4.8%变为5%。计算:(1)生成氧气的质量___。(2)电解后剩余水的质量____。
(3)配制溶液问题:
①计算类:
( 2009柳州市)欲配制溶质质量分数为5%的葡萄糖溶液100g。下列说法正确的是 ( )
A、只需要托盘天平和量筒两种仪器 B、配制时要用葡萄糖作溶质
C、用托盘天平称取5g葡萄糖 D、用量筒量取100ml水
②实验类:
(2011太原市)下图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图。

配制过程中使用的四种玻璃仪器,分别是广口瓶、________、_________、量筒。
请你指出图中一处错误操作,并分析该操作可能造成的后果____________________________________________________。
图②、图③表示的操作步骤分别是________________。
配制时需称量氯化钠_______g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会__________(填“偏大”或“偏小”);量取水最好选择____________的量筒(填序号①10mL②50mL③100mL)。(水的密度为1g/cm3)
归纳:涉及溶质质量分数的计算要紧扣溶质质量分数的定义式: 式中一共有三个量,把它看成一个方程式,分析或计算某些量的变化即可以求得问题的结果。
式中一共有三个量,把它看成一个方程式,分析或计算某些量的变化即可以求得问题的结果。
(五)有关溶液和化学方程式的简单综合计算:
(1)叙述型计算题:
①涉及沉淀的叙述型计算题:
(2012重庆市)家里蒸馒头用的纯碱中含有少量的氯化钠,课外探究小组的同学欲测定纯碱中碳酸钠的含量。他们取该纯碱样品11.0g,全部溶解在100.0g水中,再加入氯化钙溶液141.0g,恰好完全反应。过滤干燥后,称得沉淀质量为10.0g。请计算:(1)纯碱样品中碳酸钠的质量;(2)反应后所得滤液中溶质的质量分数。
②涉及气体的叙述型计算题:
(2009天津市)将10g不纯的锌粒(杂质不容与水也不与酸反应)投入到100g稀硫酸中,恰好完全反应,得到0.2气体,试计算:
(1)锌粒中纯锌的质量; (2)稀硫酸中溶质的质量分数。
③由溶液质量和质量分数进行计算:
(2007天津市)现有Na2CO3和Na2SO4的固体混合物共12g,将它放入98g20%的H2SO4溶液中,充分反应后溶液呈酸性;在此酸性溶液中再加入80g10%的NaOH溶液,恰好完全中和。计算:(1)恰好完全中和后,所得溶液中溶质的质量分数。(计算结果精确到0.1%)
归纳:反应后所得溶液的质量等于反应前某溶液的质量加进入溶液的质量减从溶液出去的质量。当然,也可以从分析溶质溶剂的变化来求得,不过此法一般较烦。还要注意,不要漏掉溶质,如(2007天津市)题。
(2)标签型计算题:
 (2009德阳市)某校化学实验室有一瓶标签残缺的
(2009德阳市)某校化学实验室有一瓶标签残缺的
过氧化氢溶液(如图所示)。该校化学课外兴趣小组的
同学为了测定其中溶质的质量分数,他们取出该溶液34g,
加入适量催化剂,待完全反应后,共收集到0.32g氧气。
试计算该溶液中溶质的质量分数。
(3)图像型计算题:
(2012.肇庆市)(7分)实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀
质量的关系曲线如右图所示。
回答下列问题:
 (1)从图中看出生成沉淀的最大质量是_____g。
(1)从图中看出生成沉淀的最大质量是_____g。
(2)开始加入碳酸钠溶液至10g时,还没有沉淀的原
因是____________________。
(3)计算原滤液中氯化钙的质量分数。
归纳:无论给你图像还是让你绘图像,要注意图像的起点,终点,折点,
及题目告诉的特殊点。
(4)表格型计算题:
(2012.达州市)(7分)某同学为了测定NaCl和MgCl2固体混
合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于
水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如下实验数据:

问:
1、表中m的值为____;(2分)
2、原固体混合物中MgCl2的质量分数是多少?(5分)(要求写出计算过程)
归纳:对于表格型的数据分析计算题,要善于进行数据分析。例如本题中,在固体物质相等的情况下,氢氧化钠溶液的质量依次增加20克,分析一、三知道,第一次肯定氢氧化钠完全反应,氯化镁没有完全反应,因为增加氢氧化钠溶液的质量后,反应又继续进行,及沉淀的质量增加了,每20克氢氧化钠溶液完全反应生成沉淀2.9克,那么60克氢氧化钠溶液完全反应生成沉淀应当是2.9克﹡3﹦8.7克,而第三次生成沉淀恰好是8.7克,说明第一二三实验中氢氧化钠溶液都完全反应,那么m的值是2.9克﹡2﹦5.8克。分析三、四次,尽管氢氧化钠溶液的质量增加,但沉淀的质量却没有增加,说明第三次中氯化镁就已经完全反应了,第四次实验氢氧化钠溶液过量,从而说明在第三次试验中,20克固体混合物与60克氢氧化钠溶液恰好完全反应。分析好数据,第二问求纯氯化镁的质量即可根据8.7克氢氧化镁来求。
对于质量守恒定律的数据分析题,例如(2010青岛市),先通过分析同一种物质在反应前后的质量变化,判断该物质是反应物还是生成物,质量减少的是反应物,质量增加的是生成物,然后根据质量守恒定律,求算出待求物质参加反应或生成的质量,再根据该物质在反应前的质量,求算出该物质在反应后的质量。
(五)有关质量守恒定律的计算
将3.6g的碳酸钙高温煅烧一段时间后冷却,测得固体剩余物中钙元素的质量分数为57.6%,求固体剩余物的质量。
归纳:元素守恒法,有时是解题的捷径。
第二篇:初中化学计算题型归纳
初中化学计算
(一)有关化学式的计算
用元素符合来表示物质组成的式子叫做化学式。本知识块的计算关键是抓住这一概念,理解概念的含义,并要深刻理解化学式中各符号及数字的意义,处理好部分与整体之间的算术关系。
1.计算相对分子质量。
相对分子质量是指化学式中各原子的相对原子质量的总和。通过化学式可以计算出该物质的相对分子质量,也可以通过相对分子质量,求某物质的化学式。在计算的过程中应注意化学式前面的数字(系数)与相对分子质量及元素符号右下角的数字与相对原子质量之间的关系是“相乘”不是“相加”;若计算结晶水合物的相对分子质量时,化学式中间的“·”与结晶水的相对分子质量之间是“相加”不是“相乘”。
5H2O的相对分子质量总和。 例计算5CuSO4·
2.计算化合物中各元素的质量比
宏观上物质是由元素组成的,任何纯净的化合物都有固定的组成,这样可以计算化合物中所含元素的质量比。计算的依据是所含元素的质量比,等于微观上每个分子(即化学式)中各种原子的个数与其原子量的乘积之比。
例计算氧化铁中铁元素和氧元素的质量比。
3.计算化合物中某元素的质量分数
宏观上化合物中某元素的质量分数等于微观上化合物的每个分子中,该元素的原子的相对原子质量总和与化合物的相对分子质量之比,即:
例计算硝酸铵(NH4NO3)中,含氮元素的质量分数。
(二)有关化学方程式的计算
化学方程式是用化学式表示化学反应的式子,这样,化学方程式不仅表达了物质在质的方面的变化关系,即什么是反应物质和什么是生成物质,而且还表达物质在量的方面的变
化关系,即反应物质和生成物质的质量关系,同时包括反应物质和生成物质的微粒个数关系,这是有关化学方程式计算的理论依据。
1.有关反应物和生成物的计算
这是化学方程式计算中最基础的题型,要深刻理解化学方程式的含义,理解反应物质和生成物质在微观上和质量上的关系。
例如将一氧化碳在空气中点燃后生成二氧化碳的化学反应中,它们的关系:
2CO + O2 = 2CO2
1 ∶ 2 微粒比: 2 ∶
28 ∶ 32 ∶ 88 ( 7∶4∶11) 质量比:2×
*体积比:2 ∶ 1 ∶ 2 (同温、同压)
质量守恒:56+32=88
2.不纯物的计算
化学方程式中所表示的反应物和生成物都是指纯净物,不纯物质不能代入方程式进行计算。遇到不纯物质时,需要将不纯物质换算成纯净物质的量,才能代入方程式,按质量比进行计算。计算关系为:
纯净物的质量=不纯物的质量×纯净物的质量分数
例用含Fe2O3 75%的赤 铁矿石20吨,可炼出含杂质4%的生铁多少吨?
3.选量(过量)计算
化学方程式计算的理论依据就是质量守恒定律。在质量守恒定律中,“参加反应的各物质的质量总和,等于反应生成的各物质的质量总和”。要着重理解“参加”两个字的含义,即没有“参加”反应的物质,就不应计算在内。在有些计算题中,给出了两种反应物的质量,求生成物,这时就必须考虑,给出的两种物质的质量是否都恰好参加了反应。这时思考的范围就应大一些。
例今有氢气与氧气的混合气共20克,在密闭的容器中点燃,生成水18克,则下列分析正确的是()
(A)氢气10克,氧气10克 (B)氢气2克,氧气18克
(B)(C)氢气4克,氧气16克 (D)氢气1克,氧气19克
4.多步反应的计算
从一个化学反应中求出的质量,用此量再进行另一个化学反应或几个化学反应的连续计算,求最后一个化学反应的量,一般称之为多步反应的计算。
例计算用多少克的锌跟足量稀硫酸反应生成的氢气,能跟12.25克的氯酸钾完全分解后生成的氧气恰好完全反应生成水。
(二)有关溶液的计算
溶液是一种或几种物质分散到另一种物质里形成均一、稳定的混合物,在有关溶液的计算中,要准确分析溶质、溶剂、溶液的质量,它们的最基本的质量关系是:
溶质质量+溶剂质量=溶液质量
应注意此关系中,溶质质量不包括在溶液中未溶解的溶质的质量。
1.溶解度的计算
固体物质溶解度的概念是:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
根据溶解度的概念和溶液中溶质、溶剂和溶液的量的关系,可进行如下的有关计算。
(1)根据在一定温度下,某物质饱和溶液里的溶质和溶剂的量,求这种物质的溶解度。
(2)根据某物质在某温度下的溶解度,求该温度下一定量的饱和溶液里含溶质和溶剂的质量。
(3)根据某物质在某温度下的溶解度,求如果溶剂质量减少(蒸发溶剂)时,能从饱和溶液里析出晶体的质量。
(4)根据某物质在某温度下的溶解度,求如果温度变化(降温或升温)时,能从饱和溶液里析出或需加入晶体的质量。
2.溶液中溶质质量分数的计算
溶质的质量分数是溶质质量与溶液质量之比。初中化学中常用百分数来表示。溶液中溶质质量分数的计算式如下:
溶质的质量分数= 溶质质量 / 溶液质量 × 100%
溶质质量分数的计算题可以有:
(1)已知溶质和溶剂的质量,求溶液的质量分数。
(2)已知溶液的质量和它的质量分数,求溶液里所含溶质和溶剂的质量。
(3)将一已知浓度的溶液加入一定量的水进行稀释,或加入固体溶质,求稀释后或加入固体后的溶液的质量分数。
3.溶液度与溶液质量分数之间的换算
在一定温度下,饱和溶液里溶质质量、溶剂质量、溶液质量之比,是一个固定的值,也就是说饱和溶液里溶质质量分数是恒定的。在计算中首先要明确溶液度与溶液质量分数两个概念的本质区别。其次是要注意条件,必须是在一定温度下的饱和溶液,才能进行换算。
溶解度与溶液中溶质质量分数的比较如下:
溶解度 质量分数
量的关系 表示溶质质量与溶剂质量之间的关系 表示溶质质量与溶液质量之间的关系
条件 ①与温度有关(气体还跟压强有关)
②一定是饱和溶液 ①与温度、压强无关
②不一定是饱和溶液,但溶解溶质的质量不能超过溶解度
表示方法 用克表示,即单位是克 用%表示,即是个比值,没有单位
100% 换算公式 饱和溶液中溶质质量分数= 溶解度/(溶解度+100克水 ) ×
第三篇:初中化学计算题总结训练
初中化学计算题专题
一根据化学式的计算
(一)有关化学式的计算
1、求相对分子质量,相对分子质量是指化学式中各原子的相对原子质量的总和。在计算的过程中应注意化学式前面的数字(系数)与相对分子质量及元素符号右下角的数字与相对原子质量之间的关系是“相乘”不是“相加”;若计算结晶水合物的相对分子质量时,化学式中间的“·”与结晶水的相对分子质量之间是“相加”不是“相乘”。例 计算5CuSO4·5H2O的相对分子质量总和。
5CuSO4·5H2O=5×[64+32+16×4+5×(1×2+16)] =5×[160+5×18] =1250
2、求化合物中各元素的质量比:以合物AmBn 为例。A、B元素的质量比A的相对原子质量?m。 B的相对原子质量?n
例,计算氧化铁中铁元素和氧元素的质量比。氧化物的化学式:Fe2O3,则 Fe∶O=56×2∶16×3=112∶48=7∶3
3、求化合物中某元素的质量分数:化合物中任一元素的质量分数可以用下式计算:某元素的质量分数=该元素的质量?100%。 化合物的总质量
某物质的质量?100% 混合物的质量另:混合物中某物质的质量分数=
(二)确定化学式的计算
1、根据化合物中各元素的质量比求化学式
将各元素的质量分别除以其相对原子质量,得到的商之比即为相应的原子个数之比,继而确定其化学式。
例,某硫的氧化物中S、O元素的质量比为2:3,该硫的氧化物的化学式为 解析:S、O原子个数比为23?1:3,所以化学式为SO3 3216
2、根据化合物中某元素的质量分数求化学式
已知某化合物中某元素的质量分数和相对分子质量,可确定该化合物中各原子个数之比,进而确定其化学式。
例,某铁的氧化物中ω(Fe)=70%,则设其化学式为
56x?100%
解析:可设该氧化物化学式为FexOy。则ω(Fe)=56x?16y=70%,解得x:y=2:3则其化学式为Fe2O3
根据化合价确定化学式
例,曾用作麻醉剂的“笑气”,是一种氮的氧化物,其中氮元素的化合价为+1,则“笑气”的化学式是( ) A.N2O5 B. NO2 C. NO D.N2O
根据质量守恒定律确定化学式,反应前后元素的种类,原子数目不变。
3、例,科学家通过宇宙探测仪发现金星大气层中含有物质X,X可以通过下列反应制取 CH2(COOH)2 X+2H2O。则物质X的化学式为( )
A CO B.CO2 C.C3O2 D.C2O3
二、有关化学方程式的计算
有关化学方程式计算的步骤:
(1)假设未知量,用x、y等字母表示
(2)正确完整地写出相应的化学方程式。
(3)根据化学方程式写出各物质的相对分子质量,标在化学式下面。
(4)把题中的已知条件和待求未知量写在相应的分子质量下面。
(5)列比例式、求解
(6)写出答案
注意:1、认真细心:化学式写正确;相对分子质量要准确;2、带入化学方程式中计算的相关量必须是纯净的质量。3、要注意反应中的条件,如“充分反应”、“完全反应”、“恰好反应”、“足量”、“过量”等关键性词语,以作出正确判断。
1、有关反应物和生成物的计算
化学方程式能表达出多种量的关系,这些关系都是解答有关化学方程中的已知和未知的隐含的已知条件,这些条件都可以应用于计算时的“桥梁”,是整个计算题的基础和依据。
例,发射通讯卫星的火箭用联氨(N2H4)做燃料,用四氧化二氮 (N2O4)助燃,反应的化学方程式如下:2N2H4+ N2O4=== 3N2+4H2O,生成物不会对大气造成污染。请计算:3.2Kg N2H4发生燃烧,需要助燃物N2O4的质量。
解:设需要助燃物N2O4的质量为x
2N2H4+ N2O4=== 3N2+4H2O
64 92
3.2kg x 6492? 3.2kgx
X=4.6kg
答:3.2Kg N2H4发生燃烧,需要助燃物N2O4的质量4.6kg。
2、不纯物的计算
化学方程式中所表示的反应物和生成物都是指纯净物,不纯物质不能代入方程式进行计算。遇到不纯物质时,需要将不纯物质换算成纯净物质的量,才能代入方程式,按质量比进行计算。计算关系为:纯净物的质量=不纯物的质量×纯净物的质量分数
例,用含Fe2O3 75%的赤铁矿石20吨,可炼出含杂质4%的生铁多少吨?
解:20吨赤铁矿石中含纯Fe2O3的质量为:20吨×75%=15吨
设可炼出含杂质4%的生铁质量为x
Fe2O3 + 3CO= 2Fe+3CO2
160 112
15吨 (1-4%)x x=12.5吨
3、有关无数据计算题
计算题需要数据,但有许多化学计算题缺少数据甚至无数据,这就需要假设数据。假设数据也有技巧,否则会使计算变得复杂。
【方法归纳】(1)如果题目中只有百分含量的数据,则应该假设百分数分母代表的物质为100g;(2)如果题目中什么数据都没有,则应该根据某一物质的相对分子质量来假设数据。 例1:有一瓶二氧化锰和高锰酸钾的混合物,其中二氧化锰的质量分数为21%。取一定量的混合物,放入大试管中充分加热至不再反应为止,试求剩余固体中二氧化锰的质量分数。 解:设原混合物的质量为100 g,原二氧化锰的质量是100g×21%=21 g,高锰酸钾的质量是100 g-21 g=79 g;生成二氧化锰的质量为x,生成氧气的质量为y。
2KMnO4

K2MnO4+ MnO2+ O2↑
316 87 32
79 g x y 3168732?? x=21.75 g y=8 g 79gxy
21g?21.75g =46.5% 100g-8gω(MnO2)=
答:二氧化锰的质量分数为46.5%.
例2,取一定量的高锰酸钾放入大试管中,充分加热直到不再产生气体为止。试求剩余固体中二氧化锰的质量分数。
解:设参加反应的高锰酸钾质量为316g,生成二氧化锰的质量为x,生成氧气的质量为y。
2KMnO4

K2MnO4+ MnO2+ O2↑
316 87 32
316 g x y
x=87g y=32g
ω(MnO2)=87g=30.6% 316g-32g
答:剩余固体中二氧化锰的质量分数是30.6%
4、化学图像型计算
化学计算中出现的坐标系一般都比较容易识别,正确解读坐标系中给出的相关信息是解题的关键。常见的情况是用坐标系中的纵坐标表示生成的气体或者沉淀的质量,读出并正确理解坐标系中的一些特殊“点”(如起点、拐点、终点)
第一步,理清楚题目中涉及哪几个化学反应并写出化学方程式,如果需要,还要判定它们反应的先后顺序;
第二步,结合图像分析每段图像对应的化学反应,弄清“起点”、“拐点”、“终点”的化学含义,确定相关物质质量;
第三步,将已知物质质量代入化学方程式,求出未知量。需要注意的是,溶液质量的求法一般是:进入反应容器的物质总质量减去沉淀质量、杂质质量和气体质量;求溶质质量时,要特别注意溶质包括哪几块质量,不要有遗漏。
例:在一烧杯中盛有22.3 g Na2CO3和NaCl组成的固体混合物,加足量水溶解,配成溶液。向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答问题 :
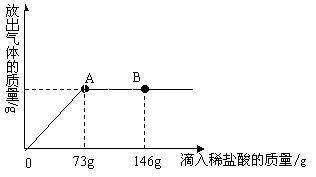
(1)当滴加了73 g稀盐酸时,放出气体的总质量为 g。
(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式) 。
(3)当滴加了73 g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。
5、多步反应的计算
从一个化学反应中求出的质量,用此量再进行另一个化学反应或几个化学反应的连续计算,求最后一个化学反应的量,一般称之为多步反应的计算。
例 ,计算用多少克的锌跟足量稀硫酸反应生成的氢气,能跟12.25克的氯酸钾完全分解后生成的氧气恰好完全反应生成水。
本题涉及三个化学反应:
Zn+H2SO4(稀)=ZnSO4+H2↑ 2KClO3=2KCl+3O2↑ 2H2+O2=2H2O 可以用三个化学方程式中的微粒关系,找出它们的已知量与未知量的关系式:
2KClO3~3O2~6H2~6Zn 即KClO3~3Zn
设需用锌的质量为x,根据上述关系式,
KClO3 ~ 3Zn
122.5 3×65
12.25g x
x=19.5g
三、有关溶液的计算
溶液是一种或几种物质分散到另一种物质里形成均一、稳定的混合物,在有关溶液的计算中,要准确分析溶质、溶剂、溶液的质量,它们的最基本的质量关系是:
溶质质量+溶剂质量=溶液质量
应注意此关系中,溶质质量不包括在溶液中未溶解的溶质的质量。
1、溶质质量分数的公式
(1)溶质质量分数=
溶质质量分数=溶液质量×溶质质量分数
溶液质量=溶质质量?100% 溶液质量溶质质量 溶质质量分数
(2)溶液质量=溶液体积×溶液密度
注意:1、只有当溶质全部溶于溶剂中,且不与溶剂发生反应时,才能直接应用以上公式;2、溶质与溶剂不发生反应,但没有全部溶解,则溶质的质量只计算溶解部分;3、若溶质带有结晶水,其结晶水应作为溶剂水的质量计算。
例,无土栽培所用的某种营养液中,含硝酸钾的质量分数为7%,某蔬菜生产基地欲配制该营养液200kg,需要硝酸钾的质量是( )
A.7kg B.14kg C.70kg D.140kg
2、有关溶液浓缩与稀释的计算
加水稀释稀释前后溶液中溶质的质量不变
溶液的稀释
加稀溶液混合后溶质质量是浓、稀溶液的溶质质量的和
加溶质
溶液的浓缩 蒸发 蒸发前后溶质质量不变
加入浓溶液 混合后溶质质量是浓、稀溶液的溶质质量的和
例,1、要将100g溶质质量分数为20%的硝酸钾溶液稀释成溶质质量分数为10%的硝酸钾溶液,需加入水的质量为( )
A.50g B.90g C.100g D.200g
2、现有8%的氯化钠溶液50g,若是其溶质质量分数增达到16%,可采用的方法是: ①需要蒸发多少克水? ②需要加入多少g 氯化钠?
③需要加入多少克40%的氯化钠溶液?
3、有关溶液与化学方程式的综合计算
在根据化学方程式进行化学计算时,各反应物、生成物之间,要以溶质的质量列比例,而不能直接用溶液的质量或体积列比例。
例,用“侯氏联合制碱法”制取的纯碱(Na2CO3)中常含有少量的氯化钠。化学实验小组同学为测定某厂生产的纯碱中碳酸钠的含量,称取12g样品放入烧杯中并滴加稀盐酸,当盐酸滴加至73g时,气泡不再冒出,此时称得烧杯内溶液的总质量为80.6g。试计算:
⑴产生二氧化碳气体的质量是 g。
⑵该厂生产的纯碱中碳酸钠的质量分数。(计算结果精确到0.1%)
(3)试通过计算求出其中含溶质的质量分数
答案(1)4.4g
(2)解:设12g纯碱试样中碳酸钠的质量为x,氯化钠为y
Na2CO3+2HCl ===2NaCl+H2O +CO2↑
106 117 44
x y 4.4g
106:44=x:4.4g
解得x=10.6g y=11.7
碳酸钠的质量分数为:10.6g/12g×100%=88.3% 答:该厂生产的纯碱中碳酸钠的质量分数88.3%。
(3)氯化钠的质量分数=(11.7+12-10.6)/80.6×100%=28.7%
