一、氯及其化合物的转化关系
1、液氯、新制的氯水和久置的氯水比较
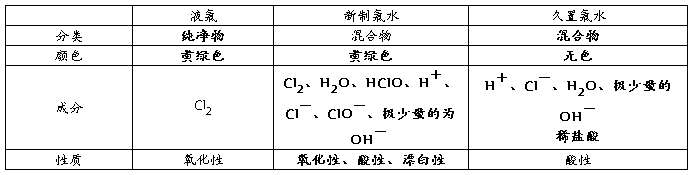
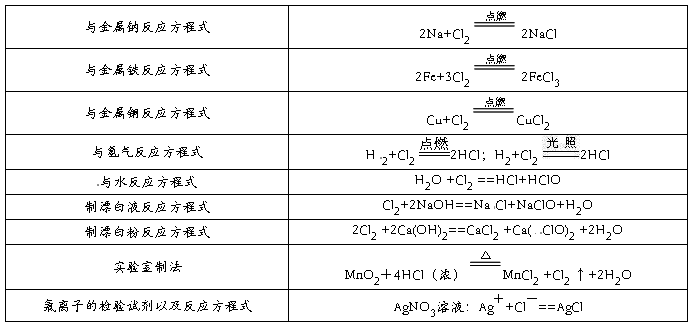
2、氯气的性质
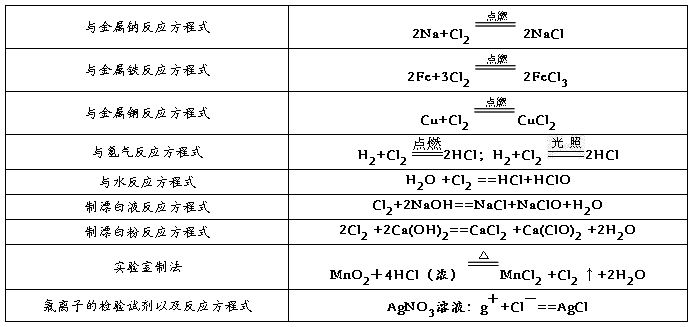
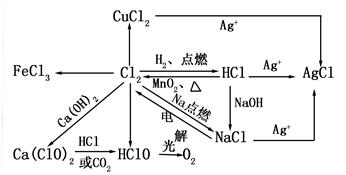
二、硅及其化合物的转化关系


①Si的还原性大于C,但C却能在高温下还原出Si。2C+SiO2Si+2CO↑;
②Si能与NaOH溶液反应放出H2,而其他非金属单质无此性质;
③非金属单质一般为非导体,但Si为半导体,石墨为良导体;
④非金属氧化物一般为分子晶体,但SiO2晶体为原子晶体。
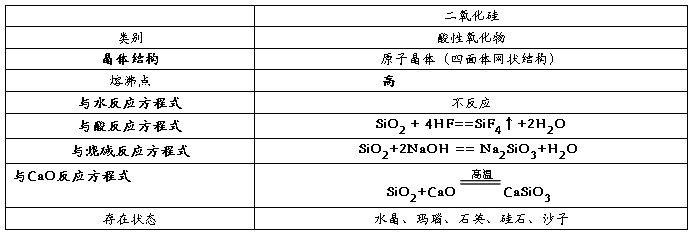
1、二氧化硅和二氧化碳比较
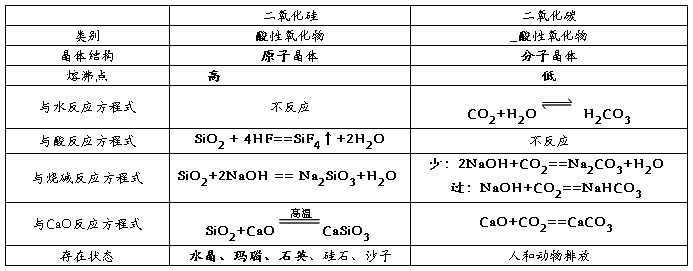
2、硅以及硅的化合物的用途

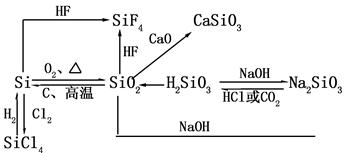
1、玻璃的主要成分之一是二氧化硅。能在玻璃上蚀刻,将其制成毛玻璃和雕花玻璃的物质是( )
A.烧碱 B.纯碱 C.氢氟酸 D.盐酸
三、硫及其化合物的转化关系

1、二氧化硫的性质

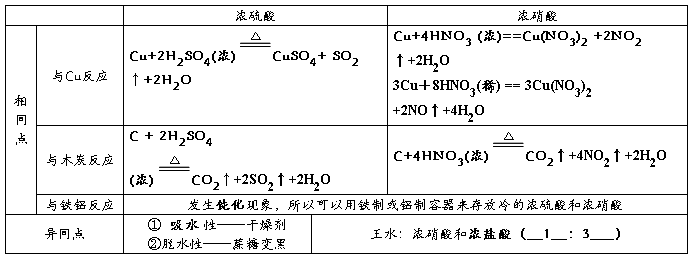
2、浓硫酸和浓硝酸的性质
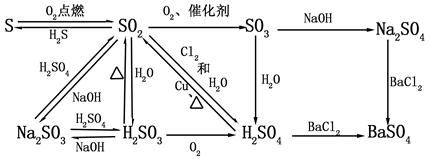
硫在空气中燃烧生成气体A。把A溶于水得溶液B。向B中滴加溴水,溴水褪色,B变成C。在C里加Na2S产生气体D。把D通入B溶液得浅黄色沉淀E。按A、B、C、D、E顺序排列的是 ( )
A.SO2,H2SO4,H2SO3,H2S,S
B.SO2,H2SO3,H2SO4,H2S,S
C.SO2,H2SO3,H2SO4,SO3,Na2S2O3
D.SO3,H2SO4,H2SO3,SO2,Na2S2O3
四、氮及其化合物的转化关系

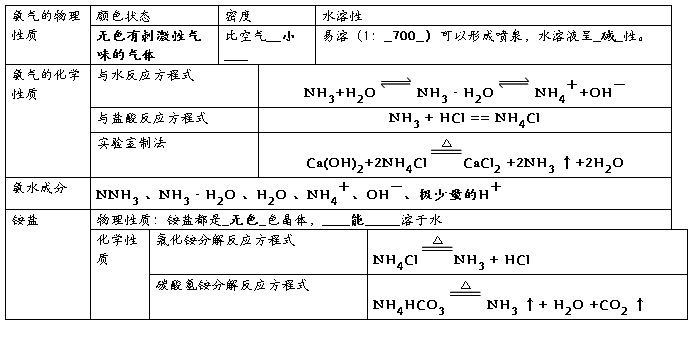
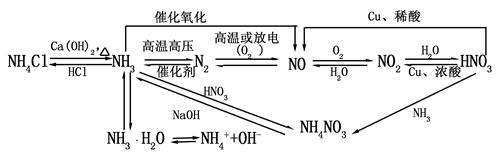
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mL B.45mL C.30mL D.15m
漂白剂
1.强氧化剂型
这类漂白剂主要包括次氯酸、Na2O2、H2O2、HNO3、臭氧等强氧化剂。这类漂白剂的漂白原理就是利用其强氧化性将有色物质氧化成无色物质,适用于漂白纺织品。但要注意不能漂白还原性物质,还要注意有关酸或碱对漂白的物质有无腐蚀性。
2.加合反应型
这里主要指的是SO2,SO2溶于水生成亚硫酸,亚硫酸跟有色物质结合,即生成不稳定的无色物质。这种作用化学上称之为“加合反应”,常用SO2漂白纸张、编织品等。这种漂白方法的缺点,一是污染环境,二是效果不持久。
3.吸附作用型
把一块木炭放入盛有品红的烧杯中振荡,会发现溶液的红色变浅,甚至完全消失,这是品红分子被吸附在木炭上的缘故。吸附作用是一种物理过程。将木炭加工制成活性炭,吸附能力会更强,用于漂白效果极佳,制糖工业中就是用活性炭作脱色剂的,除了吸附色素外,活性炭也可以吸附一些有毒气体或微粒。
【例8】 SO2通入紫色石蕊试液中,有什么现象?
【解析】 因为SO2的漂白性是有选择的,SO2不能使石蕊试液褪色,在此只表现酸性。
【答案】 紫色石蕊试液变红。
【点拔】 如果认为SO2能使所有有色物质褪色,就会认为SO2能使石蕊试液褪色。
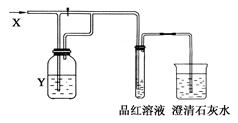
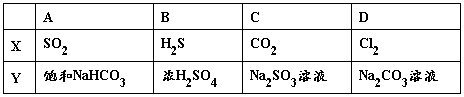
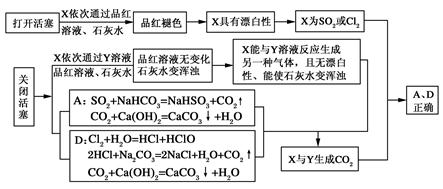
【例9】 如图所示是一套检验气体性质的实验装置,向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化,而能使澄清石灰水变浑浊;若打开活塞,则品红溶液褪色。据此判断气体X和洗气瓶内溶液Y可能是( )
第二篇:高一化学必修一第四章 非金属及其化合物(硅、氯)知识点总结
非金属及其化合物(一)
一、硅Si
1、硅单质
 存在结构:化合态(自然界),在地壳中的含量第二(仅次于氧)
存在结构:化合态(自然界),在地壳中的含量第二(仅次于氧)
物理性质:灰黑色,金属光泽,硬度大,有脆性,熔沸点高的固体,
是良好的半导体材料(硅芯片、光电池)
性质
化学性质(常温下化学性质稳定)
下列关于硅的说法不正确的是 ( )
A.硅是非金属元素,它的单质是灰黑色有金属光泽的固体
B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质反应
D.加热到一定温度时硅能与H2、O2等非金属反应
答案: C
2、二氧化硅
其化学性质很不活泼,氢氟酸HF是唯一能与之反应的酸!!!
天然二氧化硅的存在形式:结晶形和无定形
应用:石英光导纤维,石英坩埚,玛瑙饰品
1.下列物质的主要成分不是SiO2的是( )
A.石英 B.水晶 C.金刚砂 D.玛瑙
答案:C
2.下列说法正确的是( )
A.SiO2溶于水显酸性 B.CO2通入水玻璃可得硅酸
C.SiO2是酸性氧化物,它不溶于任何酸 D.SiO2晶体中不存在单个SiO2分子
答案:BD
3、硅酸
1、特点:溶解度很小,酸性很弱 (比碳酸弱)
2、什么是“硅胶”?
硅胶的用途:多孔、吸水能力强,故可做干燥剂;也做催化剂的载体

1、将足量的CO2通入下列溶液中,能产生沉淀的是 ( )
A.硅酸钠溶液 B.石灰水
C.氯化钡溶液 D.氯化钙溶液
答案:A
2、碳化钛(TiC)、碳化硼(B4C3)、氮化硅(Si3N4)等非氧化物陶瓷是新型无机非金属材料,合成这些物质需在高温条件下进行,在合成它们的过程中必须注意 ( )
答案:B
A.通入足量氧气 B.避免与氧气接触
C.通入少量氯气 D.通入少量氧气
3、下列物质属于酸性氧化物但不溶于水的是
A、二氧化碳 B、 二氧化硅 C、 二氧化硫 D、 氧化铁
答案:B
4、下列说法正确 的是( )
的是( )
A.硅是良好的半导体材料,能与盐酸或氢氧化钠溶液反应
B.二氧化硅不导电,能与盐酸或氢氧化钠溶液反应
C.硅酸具有多孔性结构,可用作吸附剂或催化剂的载体
D.二氧化硅是酸性氧化物,能与氢氟酸反应,也能与氢氧化钠溶液反应
答案:D
4、硅酸盐
1、大多硅酸盐不溶于水,化学性质稳定
 2、硅酸钠 Na2SiO3
2、硅酸钠 Na2SiO3
性质:可溶于水,其水溶液俗称水玻璃
用途:制备硅胶和木材防火剂的原料
Na2SiO3 + H2O + CO2=Na2CO3 + H2SiO3
或 Na2SiO3 + 2HCl = H2SiO3 + 2NaCl
产品:陶瓷、玻璃、水泥
小练:写出以SiO2为原料制备H2SiO3的化学方程式
答案:SiO2+2NaOH====Na2SiO3+H2O
Na2SiO3+2HCl====2NaCl+H2SiO3↓
或Na2SiO3+CO2+H2O====Na2CO3+H2SiO3↓
Na2SiO3+2CO2+2H2O====2NaHCO3+H2SiO3↓
二、氯Cl
1、氯气 很强的氧化性!!!
有毒气体!!!
重要性质
1、下列气体,被当作化学武器首次使用于战争的是( )
A.氯气  B.一氧化碳
B.一氧化碳
C.芥子气 D.沙林
答案:A
2、检验Na2SO4 溶液中含有Cl―的方法是 ( )
A.先加BaCl2溶液,再加AgNO3溶液
B.先加AgNO3溶液,再加稀HNO3
C.先加足量的Ba(NO3)2溶液,再加AgNO3溶液
D.先加足量Ba(OH)2 溶液,再加AgNO3溶液
答案:C
3、下列气体,既有颜色又有毒性的是( )
A.N2 B.CO
C.Cl2 D.CO2
D.CO2
答案:C
4、下列说法正确的是( )
A.用鼻子对着盛有氯气的瓶口,就可以嗅到氯气的气味[来源:Z#xx#k.Com]
B.用排水集气法便可以收集到纯净的氯气
C.氯气有漂白性
D.自来水常用氯气来杀菌、消毒
答案:D
5、欲除去Cl2中的少量HCl气体,可选用( )
A.NaOH溶液 B.AgNO3溶液[来源:学科网ZXXK]
C.饱和食盐水 D.石灰水
答案:C
2、氯水(混合物)
(1)溶液中含H+ :具有酸性
(2)溶液中含Cl2、HClO :具有强氧化性
(3) 溶液中含Cl ― :具有Cl
― :具有Cl ―的性质
―的性质
(4)溶液中含HClO: 具有漂白性
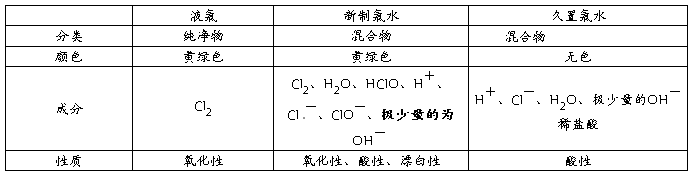
氯水在保存是要密封,避光保存。因为氯水不稳定,见光易分解。
3、次氯酸
(1)弱酸性:比碳酸弱
(2)见光容易分解:2HClO==2HCl + O2↑
(3)强氧化性:杀菌消毒,漂白
漂白性的思考:起漂白作用的物质有哪些?
干燥氯气能否漂白物质???
1、氯气可用来杀菌消毒,又可作漂白剂,其中起作用的是 ( )
A.Cl2 B.HClO C.HCl D.O2
答案:B
2、下列物质不能作漂白剂的是
A 、SO2 B、Ca(ClO)2 C、 NaClO D、 H2SO4(浓)
答案:D
3、下列物质中,既含有氯分子,又含有氯离子的是( )
A.氯化钠溶液 B.新制氯水
C.漂白粉 D.液氯
答案:B
4、下列物质能使干燥的有色布条褪色的是( )
A.氯水 B.液氯
C.氯气 D.次氯酸
答案:AD
5、下列叙述能证明次氯酸是一种弱酸的是( )
A.次氯酸不稳定,易分解 B.次氯酸是一种强氧化剂
C.次氯酸钙能与碳酸作用生成碳酸钙和次氯酸 D.次氯酸能使染料和有机色质褪色
答案:C
6、有一包白色固体,它可能是KCl、K2CO3、KNO3中的一种或几种,进行下列实验:
①溶于水,得无色溶液;[来源:学科网]
②在所得溶液中滴入AgNO3溶液,生成白色沉淀(说明:Ag2CO3为白色沉淀);
③再滴加稀硝酸,沉淀量减少但不完全消失,同 时有气泡生成。
时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是_______________,可能含有的成分是_______________。
(2)请写出上述实验中有关反应的离子方程式______________________________________。
思路解析:由②产生白色沉淀知,可能含有K2CO3和KCl中的一种或两种;由③沉淀量减少且有气泡生成知,一定含有K2CO3;又由沉淀不完全消失可知 ,一定含有KCl。
,一定含有KCl。
答案:(1)KCl和 K2CO3 KNO3
K2CO3 KNO3
(2)Ag++Cl-====AgCl↓,2Ag++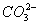 ====Ag2CO3↓,
====Ag2CO3↓,
Ag2CO3+2H+====2Ag++H2O+CO2↑
