第七章
1. 法拉第定律:Q=zFξ
2. 迁移数计算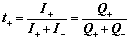
【例】用铜电极电解CuSO4溶液,通电一定时间后测得银电量计中析出0.7512g银,并测得阳极区溶液中CuSO4质量增加0.3948g。试求CuSO4溶液中离子的迁移数t(Cu2+)和t(SO42-)。(已知摩尔质量M (Ag) = 107.868 g·mol-1,M (CuSO4) =159.604 g·mol-1。)
解:电量计中析出银的物质的量即为通过总电量:n (电) =0.7512g/M(Ag)= 6.964×10-3 mol
阳极区对Cu2+ 进行物料衡算:n (原) + n (电)-n (迁出) = n (后)
n (迁出) = n (原) -n (后) + n (电)
n (迁出) =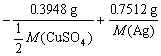
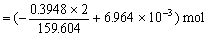 =2.017×10-3 mol
=2.017×10-3 mol
t (Cu2+) = 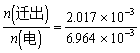 =0.2896
=0.2896
t (SO42-) =1-t (Cu2+) = 0.7164
3. 电导(G):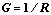 ,电导率
,电导率 ,摩尔电导率:
,摩尔电导率:
【例】已知25℃时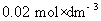 KCl溶液的电导率为0.2768 S·m-1。一电导池中充以此溶液,在25 ℃时测得其电阻为453Ω。在同一电导池中装入同样体积的质量浓度为0.555g.dm-3的CaCl2溶液,测得电阻为1050Ω。计算(1)电导池系数;(2)CaCl2溶液的电导率;(3)CaCl2溶液的摩尔电导率。
KCl溶液的电导率为0.2768 S·m-1。一电导池中充以此溶液,在25 ℃时测得其电阻为453Ω。在同一电导池中装入同样体积的质量浓度为0.555g.dm-3的CaCl2溶液,测得电阻为1050Ω。计算(1)电导池系数;(2)CaCl2溶液的电导率;(3)CaCl2溶液的摩尔电导率。
解:(1)电导池系数为
(2)CaCl2溶液的电导率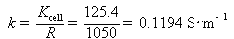
(3)CaCl2溶液的摩尔电导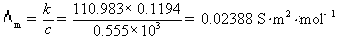
4. 离子独立运动定律
【例】已知25℃时0.05mol.dm-3CH3COOH溶液的电导率为3.8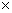 10-2S.m-1。计算CH3COOH的解离度α及解离常数Kθ。
10-2S.m-1。计算CH3COOH的解离度α及解离常数Kθ。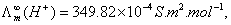
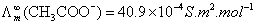
解:设CH3COOH的解离度α
CH3COOH = CH3COO-1 + H+
开始时 C 0 0
平衡时 C(1-α) Cα Cα
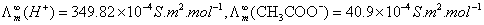

因此,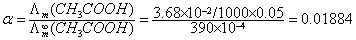
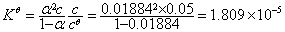
5. 平均离子活度,平均离子活度因子,平均质量摩尔浓度:
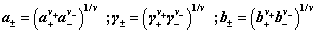
离子强度: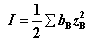
6. 原电池热力学
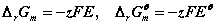
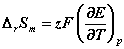
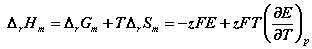
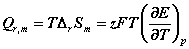
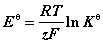
【例】在25 °C时,电池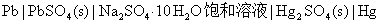 的电动势E = 0.9647 V ,电动势的温度系数
的电动势E = 0.9647 V ,电动势的温度系数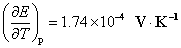 。①写出电池反应;②计算该反应的DrGm 、DrSm 、DrHm 及电池恒温可逆放电时过程的可逆热 Qr,m 。
。①写出电池反应;②计算该反应的DrGm 、DrSm 、DrHm 及电池恒温可逆放电时过程的可逆热 Qr,m 。
解:①电池反应为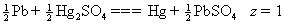
该反应的各热力学函数变化为
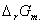 = -zFE = -1
= -zFE = -1 96485.309
96485.309 0.9647= -93.08 KJ.mol-1
0.9647= -93.08 KJ.mol-1
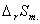 =zF
=zF =1
=1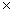 96485.309
96485.309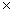 1.74
1.74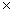 10-4=16.79 J.mol-1.K-1
10-4=16.79 J.mol-1.K-1
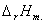 =
= 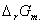 +T
+T 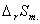 =-93.08
=-93.08 103+298.15
103+298.15 16.79=88.07KJ.mol-1
16.79=88.07KJ.mol-1
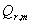 = T
= T 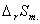 =298.15
=298.15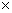 16.79 =5.006kJ.mol-1
16.79 =5.006kJ.mol-1
7. 能斯特(Nernst)方程
电池: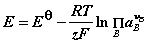
电极: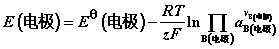
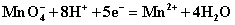
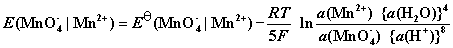
8. 电池电动势计算
E=E(右)– E(左) ; EΘ=EΘ(右)– EΘ(左)
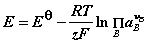 ,其中EΘ=EΘ(右)– EΘ(左)
,其中EΘ=EΘ(右)– EΘ(左)
【例】有一原电池Ag | AgCl(s) | Cl-(a=1)¦¦Cu2+(a=0.01)| Cu。
(1)写出上述原电池的反应式;
(2)计算该原电池在25℃时的电动势E;
(3)25℃时,原电池反应的 吉布斯函数变(DrG m)和平衡常数K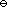 各为多少?
各为多少?
已知:E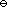 (Cu2+|Cu) = 0.3402V,E
(Cu2+|Cu) = 0.3402V,E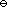 (Cl-|AgCl|Ag) =0.2223 V。
(Cl-|AgCl|Ag) =0.2223 V。
解:(1)2Ag+2Cl-(a=1) + Cu2+(a=0.01) ==== 2AgCl(s) + Cu
(2)E=[0.3402-0.2223-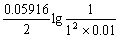 ] V = 0.05875 V
] V = 0.05875 V
(3)DrG m=-zFE=[-2×96485×0.05875] J·mol-1=-11.337 kJ·mol-1
DrG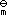 =-zFE
=-zFE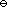 =-RTlnK
=-RTlnK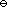
lnK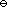 =-zFE
=-zFE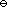 /RT=
/RT= =9.1782
=9.1782
K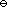 =9.68×103
=9.68×103
【例】已知 25 ℃时,下列电池的电动势 E =0.6095 V ,
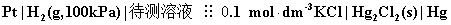
试计算待测溶液的 pH 。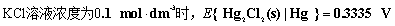
解: 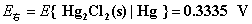
左方为氢电极
所以
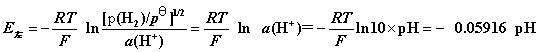
因为 E = E右 – E左 ,所以:
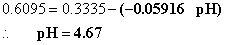
9. 原电池设计
【例】求25 ℃ AgCl(s) 在水中的溶度积Ksp 。25 ℃ 时
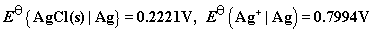
解: 溶解过程为: AgCl(s) = Ag+ + Cl–
分解成电极反应 阳极: Ag= Ag+ + e–
阴极:AgCl(s) + e–= Ag + Cl–
总反应: AgCl(s) = Ag+ + Cl– (符合题意)
所以可设计电池如右:
这个电池的电动势是: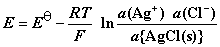
因AgCl为纯固体,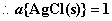
在电池达到平衡时,E = 0 ,所以:
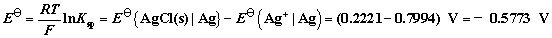

【例】已知25 ºC时AgBr的溶度积Ksp=4.88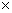 10-13,
10-13,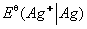 =0.7994V,
=0.7994V,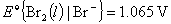 。试计算25 ºC时
。试计算25 ºC时
(1)银-溴化银电极的标准电极电势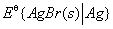 ;
;
(2) 的标准生成吉布斯函数。
的标准生成吉布斯函数。
解:(1)根据 溶度积写出的电池反应:AgBr(s)= Ag+ + Br-
其阴极反应(+): AgBr(s) + e- Ag + Br-
Ag + Br-
阳应极反应(-): Ag  Ag++ e-
Ag++ e-
设计成电池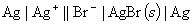

 根据Nernst方程
根据Nernst方程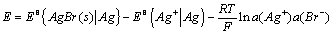
沉淀反应平衡时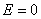 ,所以,Eθ{AgBr(s)∣Ag}=Eθ(Ag+∣Ag)+
,所以,Eθ{AgBr(s)∣Ag}=Eθ(Ag+∣Ag)+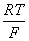 lnKsp=0.7994+
lnKsp=0.7994+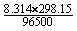 ln(4.88
ln(4.88 10-13)=0.0711V
10-13)=0.0711V
(2)根据生成反应的概念有:Ag +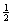 Br2=AgBr(s)
Br2=AgBr(s)
阳极反应: Ag + Br- AgBr(s) + e-
AgBr(s) + e-
阴极反应: 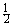 Br2+ e-
Br2+ e- Br-
Br-
设计电池,Ag∣AgBr(s)∣Br-‖Br-∣Br2(l)∣Pt
电池反应为该反应为AgBr(s)的生成反应,
ΔrGmθ=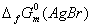 = -zFEθ= -zF[Eθ{Br-∣Br2(l)}- Eθ{AgBr(s)∣Ag}]
= -zFEθ= -zF[Eθ{Br-∣Br2(l)}- Eθ{AgBr(s)∣Ag}]
= -96485.309(1.065-0.0711)= -95.88kJ.mol-1
第九章 统计热力学初步
1. 定域子系统能级分布微态数的计算
离域子系统能级分布微态数的计算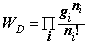
2. 玻耳兹曼分布


任何两个能级 i、k上分布数 ni 、nk 之比为: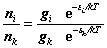
在任何一个能级i上,分布粒子数ni 与系统总粒子数N之比为: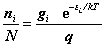
3. 配分函数计算
(1)平动配分函数: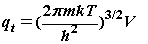
【例】求 T =300 K ,V =10 – 6 m3 时,氩气分子的平动配分函数 qt 及各平动自由度的配分函数 ft 。
解:Ar 的相对原子质量为 39.948 ,故Ar 分子质量为:
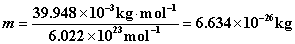
将此值及 T = 300K , V =10–6 m3 代入(9.5.11) qt计算式得:

所以一个平动自由度的配分函数为: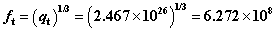
(2)转动配分函数的计算 ,其中
,其中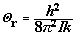 ——转动特征温度
——转动特征温度
(3)振动配分函数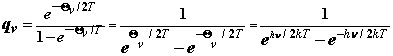
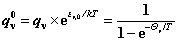
4. 热力学性质与配分函数间的关系
热力学能: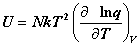
熵:定域子系统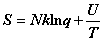 ,离域子系统
,离域子系统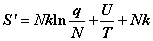
第十章 界面现象
1、液体的表面张力、表面功和表面吉布斯函数。
表面张力: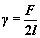 ;表面功:
;表面功: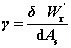 ;表面吉布斯函数:
;表面吉布斯函数:
2. 弯曲液面的附加压力—Laplace方程
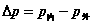
小液滴或液体中小气泡: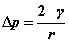 ;空气中的肥皂泡:
;空气中的肥皂泡: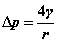
3. 毛细现象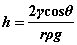
4. 微小液滴的饱和蒸气压— Kelvin公式: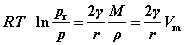
【例】已知CaCO3在773.15k时的密度为 3900kg·m-3,表面张力为1210×10-3N·m-1 ,分解压力为101.325Pa,若将CaCO3研磨成半径为 30nm(1nm=10-9m)的粉末,求其在773.15k时的分解压力。
解:一定温度下CaCO3的分解压力是指CaCO3分解产物CO2的平衡压力。此分解压力与反应物CaCO3的分散度即颗粒半径之间关系可用开尔文公式表示,即
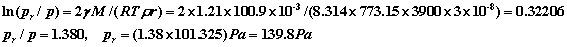 5. 朗缪尔吸附等温式
5. 朗缪尔吸附等温式
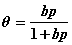 ;
;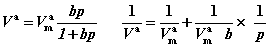

【例】已知273.15K时,用活性炭吸附CHC13,其饱和吸附量为93.8dm3·kg-1,若CHC13的分压力为13.375kPa,其平衡吸附量为82.5dm3·kg-1。求
(1) 朗缪尔吸附等温式中的b值;
(2) CHC13的分压为6.6672kPa时,平衡吸附量为若干?
解:(1)Va=Vam bp /(1+bp)
将Vam=93.8dm3·kg-1, 及 p=13.375kPa时Va=82.5dm3·kg-1 代入上式得
b =〔82.5/{13.375×(93.8-82.5)}〕kPa-1=0.5459kPa-1
(2)当p=6.6672kPa时
Va=Vam bp /(1+bp)={93.8×0.5459×6.6672/(1+0.5459×6.6672)}(dm3·kg-1)=73.58 dm3·kg-1
6. 杨氏方程(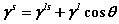
7. 表面过剩与吉布斯吸附等温式: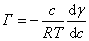
【例10.5.1】292.15k时,丁酸水溶液的表面张力可以表示为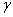 =
=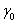 -aln(1+bc)
-aln(1+bc)
式中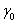 为纯净水的表面张力,a和b皆为常数。
为纯净水的表面张力,a和b皆为常数。
(1)试求该溶液中丁酸的表面过剩量Г和浓度c的关系。
(2)若已知α=13.1×10-3N·m-1,b=19.62dm3·mol-1试计算当c=0.200mol·dm-3时的吸附量Г为多少?
(3)当丁酸浓度足够大,达到b c>>1时,表面过剩Гm为若干?设此时表面上丁酸成单分子层吸附,试计算在液面上每个丁酸分子所占的截面积为若干?
解:(1)以表面张力表达式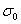 =-aln(1+b c)对c的求导:
=-aln(1+b c)对c的求导:
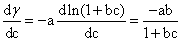
把上式代入吉布斯(Gibbs)吸附等温式,得
Г=
(2)当c=0.200mol·dm-3时,表面过剩量为
Г=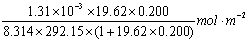 =4.298×10-6mol·m-2
=4.298×10-6mol·m-2
(3)bc>>1时
Г=
此时吸附量Г与浓度c无关,达到饱和状态,即
Г=Г =
=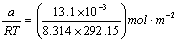 =5.393×10-6mol·m-2
=5.393×10-6mol·m-2
每个丁酸分子在液面上所占的截面积为
Am=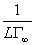 ={1/(6.022×1023×5.396×10-6)}m2 =30.79×10-20 m2
={1/(6.022×1023×5.396×10-6)}m2 =30.79×10-20 m2
第十一章 化学动力学
第二篇:物化总结
第一章 热力学第一定律
一、基本概念
系统与环境,状态与状态函数,广度性质与强度性质,过程与途径,热与功,内能与焓。
二、基本定律
热力学第一定律:ΔU=Q+W。
焦耳实验:ΔU=f(T) ; ΔH=f(T)
三、基本关系式
1、体积功的计算 δW= -pedV
恒外压过程:W= -peΔV
可逆过程: W=nRT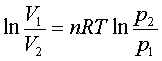
2、热效应、焓
等容热:QV =ΔU(封闭系统不作其他功)
等压热:Qp =ΔH(封闭系统不作其他功)
焓的定义:H=U+pV ; dH=dU+d(pV)
焓与温度的关系:ΔH=
3、等压热容与等容热容
热容定义: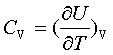 ;
;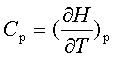
定压热容与定容热容的关系:
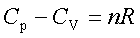
热容与温度的关系:Cp=a+bT+c’T2
四、第一定律的应用
1、理想气体状态变化
等温过程:ΔU=0 ; ΔH=0 ; W=-Q= pedV
pedV
等容过程:W=0 ; Q=ΔU=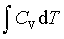 ; ΔH=
; ΔH=
等压过程:W=-peΔV ; Q=ΔH= ; ΔU=
; ΔU=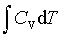
可逆绝热过程:
Q=0 ; 利用p1V1γ=p2V2γ求出T2,
W=ΔU=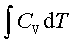 ;ΔH=
;ΔH=
不可逆绝热过程:Q=0 ;
利用CV(T2-T1)=-pe(V2-V1)求出T2,
W=ΔU=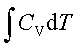 ;ΔH=
;ΔH=
2、相变化
可逆相变化:ΔH=Q=nΔ_H;
W=-p(V2-V1)=-pVg=-nRT ; ΔU=Q+W
3、热化学
物质的标准态;热化学方程式;盖斯定律;标准摩尔生成焓。
摩尔反应热的求算: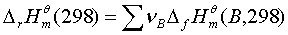
反应热与温度的关系—基尔霍夫定律:
 。
。
第二章 热力学第二定律
一、基本概念
自发过程与非自发过程
二、热力学第二定律
1、热力学第二定律的经典表述
克劳修斯,开尔文,奥斯瓦尔德。实质:热功转换的不可逆性。
2、热力学第二定律的数学表达式(克劳修斯不等式)
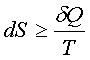 “=”可逆;“>”不可逆
“=”可逆;“>”不可逆
三、熵
1、熵的导出:卡若循环与卡诺定理
2、熵的定义: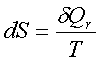
3、熵的物理意义:系统混乱度的量度。
4、绝对熵:热力学第三定律
5、熵变的计算
(1) 理想气体等温过程:

(2)理想气体等压过程: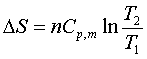
(3)理想气体等容过程: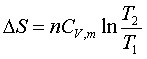
(4)理想气体pTV都改变的过程:
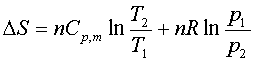
(5)可逆相变化过程: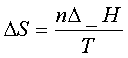
(6)化学反应过程:
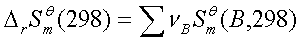
四、赫姆霍兹函数和吉布斯函数
1、定义:A=U-TS;G=H-TS
等温变化:ΔA=ΔU-TΔS;ΔG=ΔH-TΔS
2、应用:不做其他功时,ΔAT,V≤0 ;自发、平衡
ΔGT,V≤0 ;自发、平衡
3、热力学基本关系式
dA=-SdT-Vdp;dG=-SdT+pdV
4、ΔA和ΔG的求算
(1)理想气体等温过程
用公式:ΔA=ΔU-TΔS;ΔG=ΔH-TΔS
用基本关系式:dA=-SdT-Vdp;dG=-SdT+pdV
(2)可逆相变过程
ΔA=ΔU-TΔS=W=-nRT;ΔG=0
(3)化学反应过程的ΔG
标准熵法:ΔG=ΔH-TΔS
标准生成吉布斯函数法:
(4)ΔG与温度的关系
ΔG=ΔH-TΔS ,设ΔH、ΔS不遂温度变化。
五、化学势
1、化学式的定义和物理意义
 ;在T、p及其他物质的量保持不变的情况下,增加1molB物质引起系统吉布斯函数的增量。
;在T、p及其他物质的量保持不变的情况下,增加1molB物质引起系统吉布斯函数的增量。
2、化学势的应用
在等温等压不作其他功时,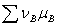 <0自发;=0平衡;>逆向自发
<0自发;=0平衡;>逆向自发
3、化学时表示式
理想气体: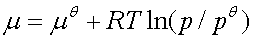
纯固体和纯液体: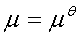
第三章 化学平衡
一、化学平衡常数与平衡常数表达式
如:Zn+2HCl(aq)=H2+ZnCl2(aq);
二、 标准平衡常数的求算
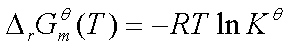
三、 范特荷夫等温方程
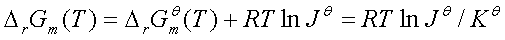
四、平衡常数与温度的关系
 ;
;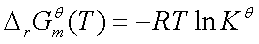
五、各种因素对平衡的影响
分压、总压、惰性气体、温度。
第四章 液态混合物和溶液
一、拉乌尔定律和亨利定律
1、拉乌尔定律
pA=p*xA ;pA=p*ax,A 适用于液态混合物和溶液中的溶剂。
2、亨利定律
pB=kx,BxB=kb,BbB=k%,B[%B] ; pB=kx,Bax,B=kb,Bab,B=k%,Ba%,B 适用于溶液中的溶质。
二、液态混合物和溶液中各组分的化学势
1、理想液态混合物
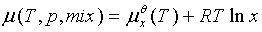 标准态为:同温下的液态纯溶剂。
标准态为:同温下的液态纯溶剂。
2、真实液态混合物
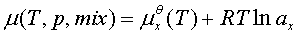 标准态为:同温下的液态纯溶剂。
标准态为:同温下的液态纯溶剂。
3、理想稀溶液
溶剂: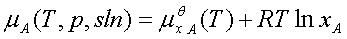 标准态为:同温下的液态纯溶剂。
标准态为:同温下的液态纯溶剂。
溶质: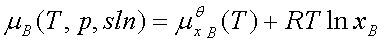 标准态为:同温下xB=1且符合亨利定律的溶质(假想状态)。
标准态为:同温下xB=1且符合亨利定律的溶质(假想状态)。
4、真实溶液
溶剂: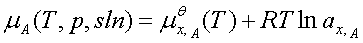 ;ax,A=fx,A x; 标准态为:同温下的液态纯溶剂。
;ax,A=fx,A x; 标准态为:同温下的液态纯溶剂。
溶质: ; ax,B=γx,B xB; 标准态为:同温下xB=1且符合亨利定律的溶质(假想状态)。
; ax,B=γx,B xB; 标准态为:同温下xB=1且符合亨利定律的溶质(假想状态)。
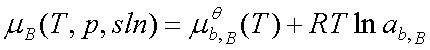 ; ab,B=γb,B bB; 标准态为:同温下bB=1且符合亨利定律的溶质(假想状态)。
; ab,B=γb,B bB; 标准态为:同温下bB=1且符合亨利定律的溶质(假想状态)。
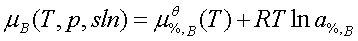 ; a%,B=γ%,B[%B]; 标准态为:同温下[B%]=1且符合亨利定律的溶质(一般为假想状态)。
; a%,B=γ%,B[%B]; 标准态为:同温下[B%]=1且符合亨利定律的溶质(一般为假想状态)。
三、各种平衡规律
1、液态混合物的气液平衡
pA=p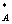 ax,A ; pA=p
ax,A ; pA=p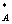 ax,A ; p=pA+pB
ax,A ; p=pA+pB
2、溶液的气液平衡
pA=p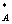 ax,A;pB=kx,Bax,B=kb,Bab,B=k%,Ba%,B;p=pA+pB
ax,A;pB=kx,Bax,B=kb,Bab,B=k%,Ba%,B;p=pA+pB
3、理想稀溶液的凝固点降低
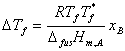
4、分配定律
5、化学平衡
6、西弗特定律
第五章相平衡
一、相律
1、物种数、独立组分数、相数、自由度数
2、相律公式
f=C-φ+2
二、单组分系统
1、克-克方程
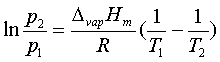
2、水的相图
三面、三线、一点。
三、双组分系统
1、相律分析
根据f=C-φ+1(一般固定压力),φ=2,f=1;φ=3,f=0
2、杠杆规则
3、步冷曲线
四、典型相图
1、Mg-Ge相图
2、Na-K相图
3、Ag-Cu相图
第六章电解质溶液
一、电解质溶液的电导
1、电导
G=1/R ; 单位:S(西门子)
2、电导率
G=κA/l 或κ=G l/A ; 单位:S/m
3、摩尔电导率
Λm=κ/c
4、无限稀释摩尔电导率
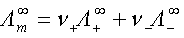
5、离子的电迁移
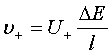 ;
;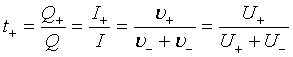 ;
;
二、电解质溶液的活度
1、电解质的化学势(电解质溶液的浓度用mB或bB表示)
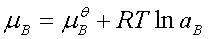
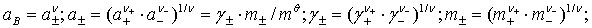
2、离子强度

3、德拜—休克尔极限公式
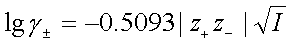 ;适用于25℃时的极稀水溶液。
;适用于25℃时的极稀水溶液。
第七章电化学
一、可逆电池的构成
电池反应互为逆反应;充放电时电流无穷小。
二、可逆电池热力学
1、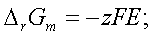
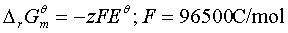
2、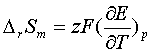
3、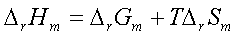
4、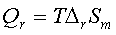 ;电池反应做了其他功。
;电池反应做了其他功。
三、能斯特方程
1、电池反应的能斯特方程
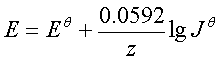 ;常用
;常用
2、电极反应的能斯特方程
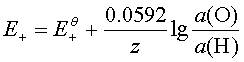 ;不常用
;不常用
四、可逆电极的种类
1、第一类电极
金属电极;气体电极
2、第二类电极
难溶盐电极;难溶氧化物电极
3、氧化还原电极
五、电极电势的应用
1、测定电池反应的热力学函数
2、测定电解质的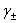
3、测定溶液的pH值
4、浓差定氧
六、极化现象和超电势
1、浓差极化
电极反应速度比离子迁移速度快造成的。
2、电化学极化
电极反应速度比电子移动速度慢造成的。
3、极化结果
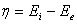 ;对阳极η总为正;对阴极η总为负。
;对阳极η总为正;对阴极η总为负。
七、金属腐蚀与防护
1、金属腐蚀
电化学腐蚀:析氢腐蚀,吸氧腐蚀
2、金属防护
阴极保护法:牺牲阳极法,外加电流法。
阳极保护法:钝化。
涂层保护法:热镀、电镀、有机涂层。
第八章 表面现象
一、表面吉布斯函数
1、产生
表面分子与内部分子的差别。
2、定义及单位
 ;J/m2或N/m;因此又称表面张力。
;J/m2或N/m;因此又称表面张力。
3、影响因素
物质本性、温度、相邻相、溶质的种类。
4、表面热力学
在温度、压力、组成不变的情况下,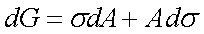
缩小表面积和降低表面张力为自发方向。
二、弯曲液面的表面现象
1、附加压力
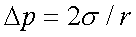
2、饱和蒸气压
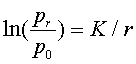
3、毛细管现象

三、新相生成与介安状态
1、过饱和蒸汽与人工降雨
2、过冷现象与晶种
3、过饱和溶液与种盐
4、过热现象与沸石
5、淬火与回火
四、固体表面的吸附作用
1、物理吸附与化学吸附
范德华力与化学键力;又无选择性;单分子层与多分子层。
2、吸附曲线
等温线(判断单多层);等压线(判断吸附类型)、等量线(求吸附热)
3、吸附等温式
弗伦德里希: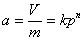
朗格谬尔: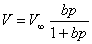
五、溶液表面的吸附
1、溶液的表面张力
各类溶质对表面张力的影响。
2、吉布斯吸附公式
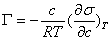
六、润湿现象
1、接触角θ
θ=0°,完全润湿;θ<90°,润湿;θ>90°,不润湿;
θ=180°,完全不润湿。
2、杨氏方程

七、表面活性剂
1、定义
溶于水后能显著降低水的表面张力的物质。
2、分类
离子型、非离子型。
3、结构特点
一端亲水基一端亲油基。
4、应用
乳化、去污(增溶)、浮选、改变润湿角。
第九章 化学动力学基础
一、关于反应速率的基本概念
1、反应速率的表示
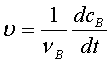
2、反应速率的测定
测定不同时刻的浓度(化学法、物理法),作c~t曲线,t时刻切线的斜率即为t时的反应速率。
3、基元反应和非基元反应
一步完成的反应为基元反应,基元反应遵守质量作用定律。是否基元反应只能通过实验确定。
4、速率方程与速率常数
质量作用定律是速率方程的特殊形式,对于非基元反应也有类似的式子。
速率常数仅与温度和催化剂有关,而与浓度无关。
5、反应级数
速率方程中浓度幂之和称之。基元反应一定为正整数,非基元反应可为0或小数。
二、浓度对反应速率的影响
1、一级反应
微分式: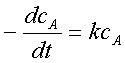 ——反应速率与浓度的一次方成正比;k的单位为时间-1;
——反应速率与浓度的一次方成正比;k的单位为时间-1;
积分式: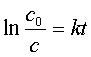 ——以lnc~t作图得一直线;
——以lnc~t作图得一直线;
半衰期: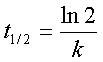 ——与起始浓度无关。
——与起始浓度无关。
2、二级反应与准一级反应
微分式: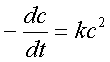 ——反应速率与浓度的二次方成正比;k的单位为浓度-1时间-1;
——反应速率与浓度的二次方成正比;k的单位为浓度-1时间-1;
积分式: ——以1/c~t作图得一直线;
——以1/c~t作图得一直线;
半衰期: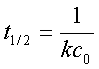 ——与起始浓度的一次方成反比。
——与起始浓度的一次方成反比。
准一级反应:对于A+B==Y+Z,当A大大过量或B大大过量时,可按一级反应处理。
3、反应级数的测定
尝试法:将一组c~t数据代入不同积分公式求k,若k为常数则所代公式正确;
作图法:将一组c~t数据按lnc~t、1/c~t等作图,若得直线可判定反应级数;
半衰期法:根据 得
得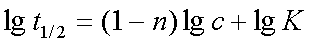 ,以
,以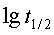 ~
~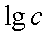 作图可得直线,从斜率可求n。
作图可得直线,从斜率可求n。
微分法:根据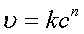 得
得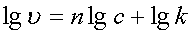 ,以
,以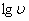 ~
~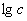 作图可得直线,斜率即为n。
作图可得直线,斜率即为n。
四、温度对反应速率的影响
1、阿仑尼乌斯公式
微分式: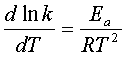
积分式: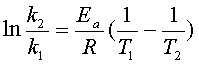
2、活化能
活化分子的平均能量与反应物分子的平均能量之差。
第十章 复合反应动力学
一、复合反应基本类型
1、平行反应
 ;
;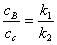
2、对行反应
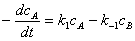 ;
;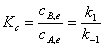
3、连串反应
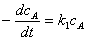 ;
;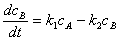 ;
;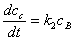
二、复合反应机理近似处理方法
1、平衡态法
对于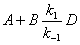
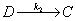 ;若
;若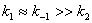 ,则反应物与中间物达成平衡。
,则反应物与中间物达成平衡。
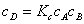 ;
;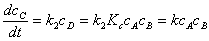
2、稳态法
对于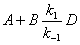
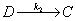 ;若
;若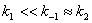 ,则中间物的浓度维持微小量不变。
,则中间物的浓度维持微小量不变。
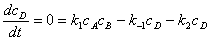 ;
;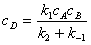
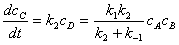
三、链反应与爆炸半岛
1、链反应
分为直链反应和支链反应;链引发、链传递、链终止。
2、爆炸半岛
常见可燃气体在空气中的爆炸限。
