实验室制乙烯的原理、装置及注意事项:
1.药品:乙醇和浓硫酸(体积比:1∶3)
2.装置:圆底烧瓶。温度在170℃左右,温度计水银球
浸入液面以下,不能与烧瓶底部接触。在烧瓶中加入沸石
(碎瓷片)防止暴沸。
3.反应原理:
浓H2SO4作用:既是催化剂又是脱水剂
4.收集:乙烯难溶于水,乙烯的相对分子质量比空气略小,采用排水取气法收集。
5.气体净化:由于在反应过程中有一定的浓硫酸在加热条件下与有机物发生氧化-还原反应使生成的气体中混有SO2、CO2,收集前应用NaOH溶液吸收SO2、CO2。
6.注意事项:要严格控制温度,应设法使温度迅速上升到170℃。因为温度过低,在140℃时分子间脱水而生成过多的副产物乙醚(CH3-CH2-O-CH2-CH3)。温度过高,浓H2SO4使乙醇炭化,并与生成的炭发生氧化-还原反应生成CO2、SO2等气体。
乙炔实验室制法:
(1)药品:电石(CaC2碳化钙)和水
(2)装置:固+液→气(不加热)
(3)反应原理:
(4)收集:乙炔的相对分子质量略小于空气;乙炔微溶于水,可用排水取气法收集。 (5)注意事项:
a.一般情况下用电石得的乙炔气中夹杂着H2S、PH3、AsH3等特殊臭味的气体,可用CuSO4溶液或NaOH溶液除去杂质气体。
b.为得到平稳乙炔气流,控制反应速率,可用饱和食盐水代替水,用分液漏斗控制流速,并加棉花,防止泡沫喷出。
苯的硝化
药品:浓HNO3、浓H2SO4、苯。
反应原理:
装置特点:水浴加热,使用温度计控制温度在50~60℃,橡胶塞上加一段玻璃导管起导气和冷凝回流作用。
操作顺序:试管中先加入1.5mL浓HNO3,再加2mL浓H2SO4,振荡冷却到50~60℃以下,再加入1mL苯振荡在50~60℃的水浴中加热10分钟,倒入盛水的烧杯中。
分离提纯:将烧杯中的液体用玻璃棒搅拌,反复水洗,再分液,得到有苦杏仁味的无色油状液体—硝基苯。
苯的卤化
药品:苯、液溴、铁钉。
反应原理:
装置特点:反应器烧瓶上面连一长导管,起导气和冷凝回流作用,收集器锥形瓶中盛有少量水,导气管口应接近水面,但不能伸进去以利于吸收HBr。
操作顺序:先将约2mL苯加入烧瓶中,再放入5~10颗无锈铁钉,最后加入1滴管液溴,立即塞好瓶塞,在锥形瓶中的水里,滴入AgNO3溶液有淡黄色沉淀生成,证明卤化反应有HBr生成。 分离提纯:将锥形瓶中的液体倒入烧杯中,用大量水或稀NaOH溶液搅拌洗涤,再分液,得到无色液体——溴苯。
酯化反应:
化学方程式为:CH3COOH + HOCH2CH3
说明:
①生成乙酸乙酯反应的条件及其意义:
加热:加热的主要目的是提高反应速率;其次是使生成的乙酸乙酯挥发,有利于收集,提高乙醇、乙酸的转化率。
浓硫酸作催化剂,提高反应速率。
浓硫酸作吸水剂,使平衡右移,提高乙醇、乙酸的转化率。
②实验室里制乙酸乙酯实验的注意事项:
化学药品加入大试管中时,不能先加浓硫酸;加热要
先小火加热,后大火加热;导气管末端不要浸入液体内,
以防液体倒吸。
③饱和Na2CO3溶液的作用:
中和乙酸;溶解乙醇;减少乙酸乙酯的溶解。
被银氨溶液氧化:
实验步骤:在洁净的试管里加入1 mL 2%的AgNO3溶液,然后边滴人2%的稀氨水,边振荡试管,至产生沉淀恰好溶解为止,然后加入3滴乙醛,振荡后,将试管在热水中加热。不能搅拌
CH3COOCH2CH3 + H2O
实验现象:不久就可以看到试管内壁上附着一层光亮如镜的金属银。
有关方程式:AgNO3+NH3·H2O=AgOH↓+NH4NO3
AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O
CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag↓+3NH3+H2O
实验结论:化合态的银被还原,乙醛被氧化。
应用:银镜反应常用来检验醛基的存在。在工业上也用银镜反应来制镜或保温瓶胆 被新制氢氧化铜悬浊液氧化
实验步骤:在试管里加入10%的NaOH 的溶液2mL,滴人2%的CuSO4溶液4滴~6滴,振荡后加乙醛溶液0.5mL,振荡后加热至沸腾。
实验现象:试管内有红色沉淀产生。
有关方程式:Cu+2OH=Cu(OH)2↓
CH3CHO+2Cu(OH)22+- CH3COOH+Cu2O↓+2H2O
说明:实验中的Cu(OH)2必须是新制的,制取Cu(OH)2时,是在NaOH溶液中滴入少量CuSO4溶液,NaOH是明显过量的。该实验必须在碱性环境中才能发生。该反应是实验室常用检验醛基的方法。
溴乙烷水解反应
化学方程式:CH3CH2—Br + H—OH CH3—CH2—OH + HBr
注意:(1)溴乙烷的水解反应是可逆反应,为了使正反应进行的比较完全,水解一定要在碱性条件下进行;
(2)溴乙烷分子不能电离出Br-,所以它不与AgNO3反应。但在碱性条件下水解之后,由于溶液中存在Br-,所以再加酸化的AgNO3溶液可以产生浅黄色的AgBr沉淀。
(3)冷却至室温再加入溴乙烷,防止挥发。长导管作用:冷凝,导气,回流。检验乙烯气体时,通入高锰酸钾溶液之前先通水,除杂。
石油的分馏
a原理:利用石油中各组成成分沸点的不同进行蒸馏,所以是物理方法;由于进行多次蒸馏,故称分馏;得到的不同沸点范围的产物称馏分,但仍是多种烃的混合物。
b实验室装置如图:所需仪器有:酒精灯、蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶
需注意的是:温度计的水银球的位置在略低于蒸馏烧瓶支管口处;冷凝管的冷却水的流向为从下到上;牛角管与锥形瓶间不需加胶塞。
第二篇:化学有机实验总结
一、复习要点
1.反应原理(方程式); 2.反应装置特点及仪器的作用; 3.有关试剂及作用;
4.反应条件; 5.实验现象的观察分析与记录; 6.操作注意事项;
7.安全与可能事故的模拟处理;
8.其他(如气密性检验,产物的鉴别与分离提纯,仪器的使用要领).
二、主要有机制备实验
1.乙烯、乙炔的制取


2.溴苯的实验室制法(如图所示)
①反应原料:苯、液溴、铁粉
②反应原理:
 +
+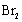
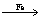
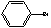 +
+
③制取装置:圆底烧瓶、长玻璃导管(锥形瓶)(如图所示)
④注意事项:
a.反应原料不能用溴水。苯与溴水混合振荡后,苯将溴
从溴水中萃取出来,而并不发生溴代反应。
b.反应过程中铁粉(严格地说是溴化铁)起催化剂作用。
c.苯的溴代反应较剧烈,反应放出的热使苯和液溴汽化,使用长玻璃导管除导气外,还兼起使苯和液溴冷凝回流的作用,使反应充分进行。
d.长玻璃导管口应接近锥形瓶(内装少量水)液面,而不能插入液面以下,否则会产生倒吸现象。实验过程中会观察到锥形瓶面上方有白雾生成,若取锥形瓶中的溶液加入经硝酸酸化的硝酸银溶液会产生淡黄色沉淀,证明反应过程中产生了 ,从而也说明了在铁粉存在下苯与液溴发生的是取代反应而不是加成反应。
,从而也说明了在铁粉存在下苯与液溴发生的是取代反应而不是加成反应。
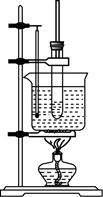 e.反应完毕可以观察到:在烧瓶底部有褐色不溶于水的液体生成,这是溶解了液溴的粗溴苯,将粗溴苯倒入稀
e.反应完毕可以观察到:在烧瓶底部有褐色不溶于水的液体生成,这是溶解了液溴的粗溴苯,将粗溴苯倒入稀 溶液中振荡洗涤,可除去溶解在溴苯中的液溴,得到无色,不溶于水,密度比水大的液态纯溴苯。
溶液中振荡洗涤,可除去溶解在溴苯中的液溴,得到无色,不溶于水,密度比水大的液态纯溴苯。
3.硝基苯的实验室制法(如图所示)
①反应原料:苯、浓硝酸、浓硫酸
②反应原理: +
+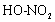
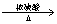
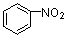 +
+
③制取装置:大试管、长玻管、水浴加热装置和温度计
④注意事项:
a.反应过程中浓硫酸起催化和脱水作用。
b.配制一定比例的浓硝酸和浓硫酸的混合酸时,应先将浓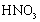
注入容器中,再慢慢注入浓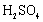 ,同时不断搅拌和冷却。
,同时不断搅拌和冷却。
c.混合酸必须冷却至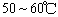 以下才能滴入苯是为了防止苯的挥发;在滴入苯的过程中要不断振荡是因为反应放热。若不振荡会因为温度升高加快了硝酸的分解和苯的挥发及副反应的发生。
以下才能滴入苯是为了防止苯的挥发;在滴入苯的过程中要不断振荡是因为反应放热。若不振荡会因为温度升高加快了硝酸的分解和苯的挥发及副反应的发生。
d.为了使反应在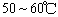 下进行,通常将反应器放在
下进行,通常将反应器放在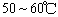 的水
的水
浴中加热,水浴加热的好处是保持恒温,受热均匀、易于控温( )。
)。
e.将反应后的混合液倒入冷水中,多余的苯浮在水面,多余的硝酸和硫酸溶于水中,而反应生成的硝基苯则沉在容器底部,由于其中溶有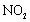 而呈淡黄色,将所得的粗硝基苯用稀
而呈淡黄色,将所得的粗硝基苯用稀 溶液洗涤除去其中溶有的残留酸后,可观察到纯硝基苯是一种无色,有苦杏仁味,比水重的油状液体。
溶液洗涤除去其中溶有的残留酸后,可观察到纯硝基苯是一种无色,有苦杏仁味,比水重的油状液体。
f.硝基苯有毒,万一溅在皮肤上,应立即用酒精清洗。
4.乙酸乙酯的制备
①实验原理:
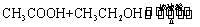
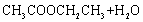
②实验装置

③反应特点
a.通常反应速率较小。
b.反应是可逆的、乙酸乙酯的产率较低。
④反应的条件及其意义
a.加热。加热的主要目的是提高反应速率,其次是使生成的乙酸乙酯挥发而收集,使平衡向正方向移动,提高乙醇、乙酸的转化率。
b.以浓硫酸作催化剂,提高反应速率。
c.以浓硫酸作吸水剂,提高乙醇、乙酸的转化率。
⑤实验需注意的问题
a.加入试剂的顺序为
b.用盛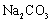 饱和溶液的试管收集生成的乙酸乙酯,一方面中和蒸发出来的
饱和溶液的试管收集生成的乙酸乙酯,一方面中和蒸发出来的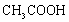 、溶解蒸发出来的乙醇;另一方面降低乙酸乙酯的溶解度,有利于酯的分离。
、溶解蒸发出来的乙醇;另一方面降低乙酸乙酯的溶解度,有利于酯的分离。
c.导管不能插入到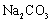 溶液中,以防止倒吸回流现象的发生。
溶液中,以防止倒吸回流现象的发生。
d.加热时要用小火均匀加热,防止乙醇和乙酸大量挥发,液体剧烈沸腾。
e.装置中的长导管起导气兼冷凝作用。
f.充分振荡试管、然后静置,待液体分层后,分液得到的上层液体即为乙酸乙酯。
点拨:①苯的硝化反应,②实验室制乙烯,③实验室制乙酸乙酯。实验中浓 H2SO4所起的作用不完全相同,实验①和③中浓H2SO4均起催化剂和吸水剂作用,实验②中浓H2SO4作催化剂和脱水剂。
⑥能与醇发生酯化反应的酸除羧酸外,还有无机含氧酸,如
C2H5OH+HO-NO2 C2H5ONO2+H2O
C2H5ONO2+H2O
硝酸乙酯
无氧酸则不行,如C2H5OH+HBr C2H5Br+H2O
C2H5Br+H2O
5.石油的分馏实验(图所示)
①反应原料:原油
②反应原理:利用加热和冷凝,把石油分成不同沸点范围的馏分
③反应装置:酒精灯、圆底烧瓶、温度计、冷凝器、锥形瓶等
④注意事项:
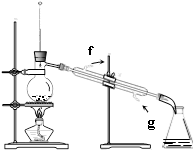
a.实验前应认真检查装置的气密性。
b.温度计水银球应位于蒸馏烧瓶支管口略低处,以测定生成物的沸点。
c.冷凝器中冷凝水的流向与气流方向相反,上口出水。
d.为防止液体暴沸,在反应混合液中需加入少许碎瓷片。
e.实验过程中收集沸点60~150℃的馏分是汽油,沸点为150~300℃的馏分是柴油。
三、官能团的特征反应
1.遇溴水或溴的CCl4溶液褪色:C═C、C≡C、-CHO(甲酸、甲酸酯、甲酸盐、葡萄糖)或酚;
2.遇KMnO4酸性溶液褪色:烯烃、炔烃、苯的同系物、醇、酚、醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等
3.遇FeCl3溶液显紫色, 遇浓溴水产生白色浑浊:酚;
4.遇石蕊试液显红色:羧酸;
5.与Na反应产生H2:含羟基化合物(醇、酚或羧酸);
6.与Na2CO3或NaHCO3溶液反应产生CO2:羧酸;
7.与Na2CO3溶液反应但无CO2气体放出:酚;
8.与NaOH溶液反应:酚、羧酸、酯或卤代烃;
9.发生银镜反应或与新制的Cu(OH)2悬浊液共热产生红色沉淀:含有-CHO(甲酸、甲酸酯、甲酸盐、葡萄糖、麦芽糖);
10.常温下能溶解Cu(OH)2:羧酸;
11.能氧化成羧酸的醇:含“─CH2OH”的结构(能氧化的醇,羟基相“连”的碳原子上含有氢原子;能发生消去反应的醇,羟基相“邻”的碳原子上含有氢原子);
12.能水解:酯、卤代烃、二糖和多糖、酰胺和蛋白质;
13.既能氧化成羧酸又能还原成醇:醛;
14.卤代烃的水解,条件:NaOH, 水,取代;②NaOH, 醇溶液,消去。
15.蛋白质(分子中含苯环)与浓HNO3反应后显黄色。
四、有机物的分离,提纯
1.甲烷气体中有乙烯或乙炔(除杂)(溴水)
2.己烷中有己烯(除杂) (酸性KMnO4)
3.醋酸钠固体中有萘(除杂和分离)(升华)
4.苯有甲苯(除杂) (先酸性KMnO4、再NaOH)
5.苯中有苯酚(除杂和分离)(NaOH、分液)
6.乙醇中有水(分离和提纯)(CaO、蒸馏)
7.乙酸乙酯中有乙醇和乙酸(除杂)(饱和Na2CO3)
8.溴苯中有溴(除杂) (NaOH、分液)
9.硝基苯中有硝酸或NO2(除杂)(NaOH、分液)
10.硝基苯中有苯磺酸(除杂和分离)(NaOH、蒸馏)
11.蛋白质溶液中有少量食盐(除杂)(清水、渗析)
12.硬脂酸钠溶液中有甘油(提纯)(NaCl)
13.蛋白质中有淀粉(除杂) (淀粉酶、水)
14.己烷中有乙醇(除杂和分离)(水洗、分液)
15.乙醇中有乙酸(除杂)(NaOH或CaO、蒸馏)
16.乙酸乙酯中有水(除杂)(无水Na2SO4)
17.苯酚中有苯甲酸(除杂)(NaHCO3、蒸馏)
18.肥皂中有甘油(除杂和分离)(NaCl、盐析)
19.淀粉中有NaCl(除杂)(渗析)
五、常见有机物的鉴别(要注意试剂的选择)
1.甲烷、乙烯与乙炔的鉴别 (燃烧)
2.烷烃与烯烃的鉴别 (溴水或酸性KMnO4)
3.烷烃与苯的同系物的鉴别(酸性KMnO4)
4.卤代烃中卤素元素的鉴别(NaOH、HNO3、AgNO3)
5.醇与羧酸的鉴别 (指示剂)
6.羧酸与酯的鉴别
(1)乙酸与乙酸乙酯的鉴别(水)
(2)乙酸与甲酸甲酯的鉴别(水)
(3)甲酸与乙酸的鉴别(新制的Cu(OH) 2)
(4)甲酸与甲醛的鉴别(新制的Cu(OH) 2)
7.醛与酮的鉴别(新制的Cu(OH) 2或银氨溶液)
8.酚与芳香醇的鉴别(浓溴水)
9.淀粉与纤维素的鉴别(淀粉酶)
10.蛋白质的鉴别,与浓HNO3反应后显黄色。
11.甘油与乙醛鉴别 (银氨溶液、Cu(OH) 2)
