照度自检报告
工程名称及编号: 检测时间 年 月 日
室内温度检测报告
工程名称及编号: 检测时间 年 月 日
室内湿度检测报告
工程名称及编号: 检测时间 年 月 日
室内外压差检测报告
工程名称及编号: 检测时间 年 月 日
…… …… 余下全文
照度自检报告
工程名称及编号: 检测时间 年 月 日

室内温度检测报告
工程名称及编号: 检测时间 年 月 日

室内湿度检测报告
工程名称及编号: 检测时间 年 月 日

室内外压差检测报告
工程名称及编号: 检测时间 年 月 日
…… …… 余下全文
苏州市黄浦空调净化设备有限公司
洁净室检验报告
检测单位:上海秋实机械设备有限公司

苏州市黄浦空调净化设备有限公司
洁净室检验报告
检测单位:上海秋实机械设备有限公司
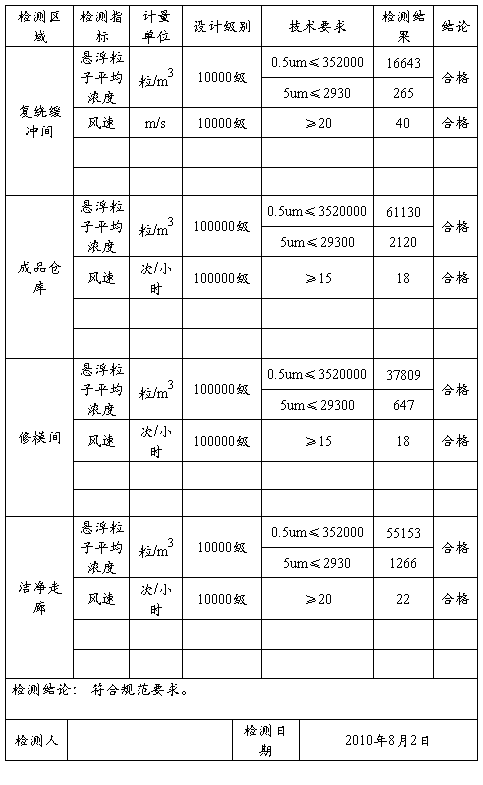
苏州市黄浦空调净化设备有限公司
洁净室检验报告
检测单位:上海秋实机械设备有限公司

…… …… 余下全文
陇南市食品药品检验检测中心
洁净室(区)性能检测凭证
检测编号:甘陇药/( ) 号 受理日期 年 月 日
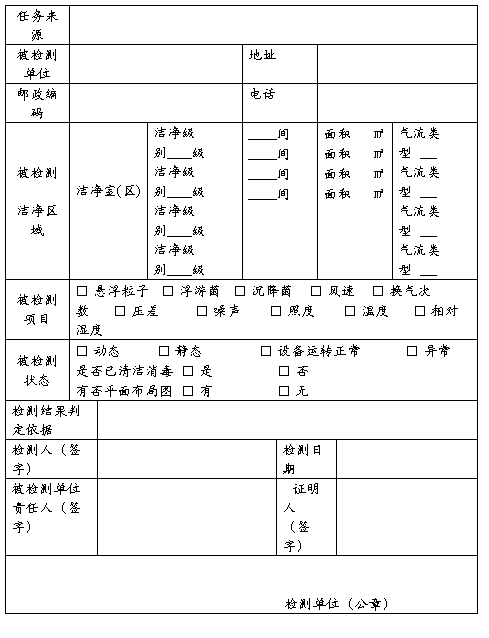
注:1、检测编号填写原则:检测药品生产企业和医疗机构制剂室填“甘陇药”,括号内填年份,括号外为四位流水号。
2、检测报告仅对检测当时的现场负责。对检测报告有异议,应于接到报告15日内向检测单位提出申诉,或向上一级检测单位申请复检,逾期不予受理。
3、检测单位地址: 邮编:
…… …… 余下全文
商丘市龙兴制药有限公司
生产厂房洁净度检测报告书
(□季度、□产前)

商丘市龙兴制药有限公司
检验报告附页
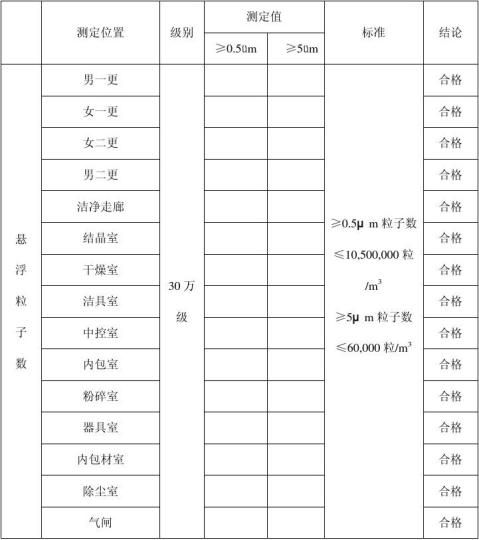
检验人:
商丘市龙兴制药有限公司
检验报告附页
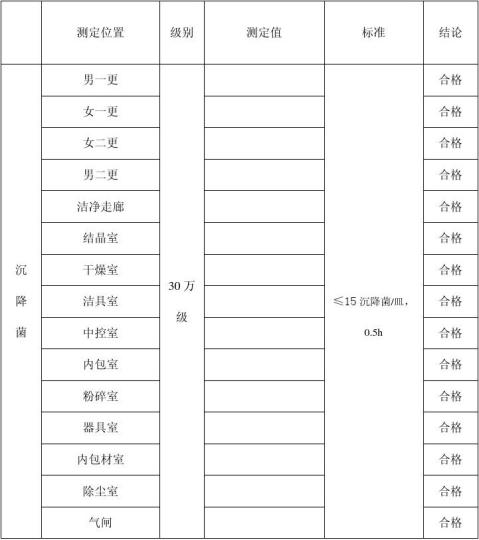
检验人:
商丘市龙兴制药有限公司
检验报告附页
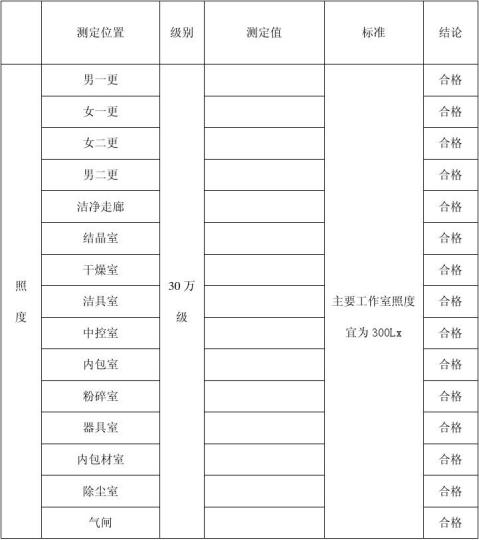
检验人:
商丘市龙兴制药有限公司
检验报告附页
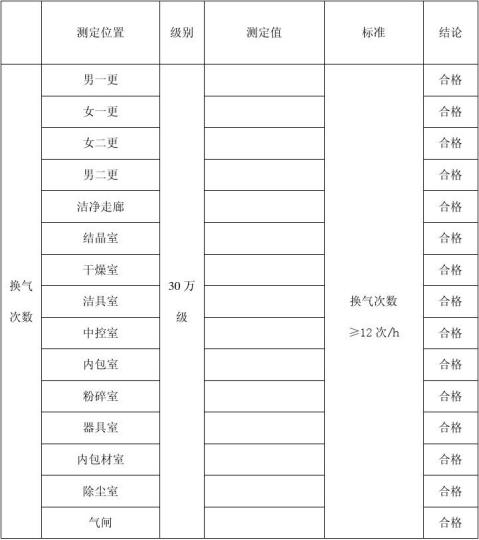
检验人:
商丘市龙兴制药有限公司
检验报告附页
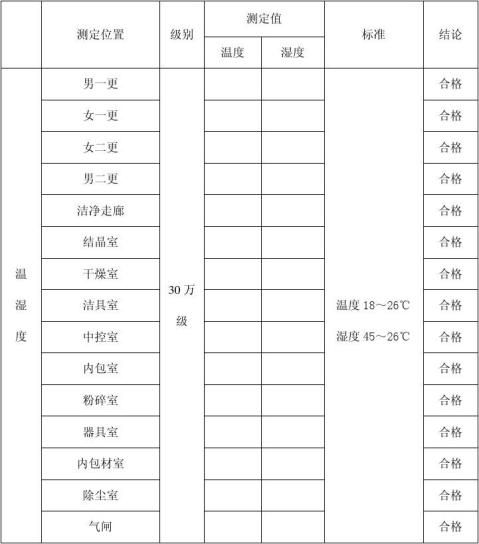
检验人:
商丘市龙兴制药有限公司
检验报告附页
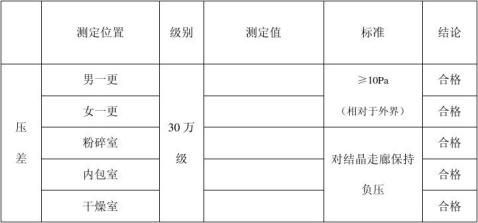
检验人:
…… …… 余下全文
洁净区空气净化空调系统验证文件
一、 验证小组的组成
验证项目名称:洁净区空气净化空调系统的验证
验证小组组长:
验证小组成员:
二、 验证方案
(一)验证目的:确认该系统运转情况及性能达到设计要求。
(二)质量标准:系统各项功能均能达到厂家使用手册和设计规定的要求。
(三)安装验证
1.资料档案
(1)系统设计和施工图纸
(2)施工合同
(3)图纸设计单位资质证明
(4)装修用料及施工说明
(5)通风空调设计施工总说明
(6)空调通风设备表
2.检测和检测结果记录
(1)过滤器安装记录
(2)系统检漏测试记录
(3)风量及压差测试记录
(4)中效过滤器及排风箱高效过滤器压差记录
(5)主要设备安装记录
(6)公共工程安装记录
(7)空运转测试
(四)运行验证
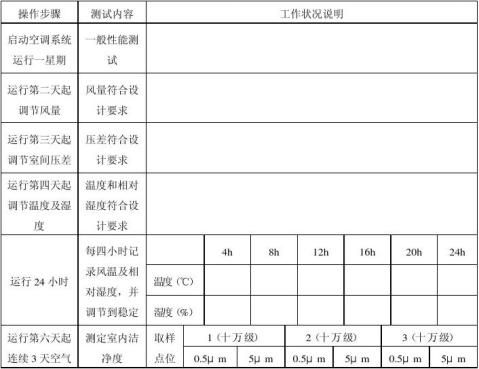
1.空运转测试
(1)一般性能测试,包括:各种管道连接是否符合标准,空机连续一周运转的情况记录。
(2)连续三天清洁后,测试系统有无泄漏,风量调节是否符合设计要求。
2.负载测试
测试风量、压差、温度和相对湿度、洁净度(尘埃粒子数)、菌落数是否符合设计要求。
(五)验证方案的起草和审批
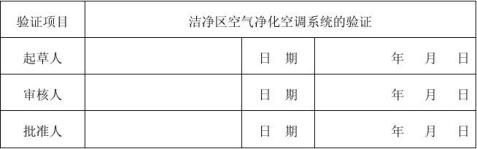
洁净区空气净化空调系统验证报告
201*年7月27日至201*年7月 30日,洁净区空气净化空调系统验证小组根据批准的洁净区空气净化空调系统验证方案,对洁净区空气净化空调系统进行了验证,验证结果如下:
(一)资料档案的审核和归档
(二)检测结果 1、过滤器安装记录
2、系统检漏结果记录
3、风量及压差记录
4、中效过滤器及排风箱高效过滤器压差记录
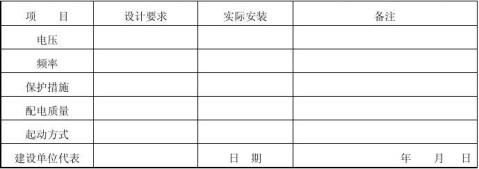
5、主要设备安装记录
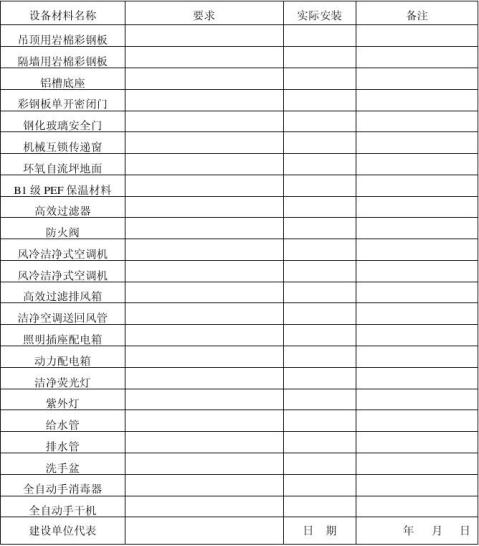
6、公共工程安装记录
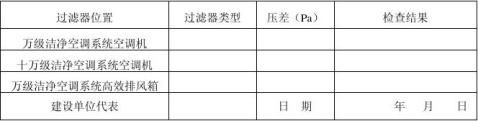

7、空运转测试
8、负载测试
9.………………检验中心检验报告
(三)结论和说明
1.验证方案合理,在实施过程未作变动。 2.各项性能指标的误差在允许范围内。 3.验证记录完整属实。
…… …… 余下全文
洁净室检测参照标准以及相关细则
第三方洁净室检测验收单位需要通过国家实验室认可委(CNAS)认证和计量认证(CMA),其出具的洁净室检测报告方能真实反映洁净厂房实际情况,可作为第三方公正评价的依据,同时可用于QS认证的洁净环境检测报告和GMP认证的生产环境洁净检测报告。
检测范围:洁净室环境等级评定、工程验收检测,包括食品洁净室、保健品净化车间、化妆品洁净工程、桶装水百级灌装车间、电子产品洁净生产车间、GMP净化车间、医院手术室、动物实验室、生物安全实验室、生物安全柜、超净工作台、无尘车间、无菌车间等。
检测项目:洁净间的尘埃粒子数、沉降菌、浮游菌、压差、换气次数,风速、新风量、照度、噪声、温度、相对湿度等。
参照检测标准:
1 《洁净厂房设计规范》GB50073-2001
2 《医院洁净手术部建筑技术规范》 GB 50333-2002
3 《生物安全实验室建筑技术规范》GB 50346-2004
4 《洁净室施工及验收规范》GB 50591-2010
5 《医药工业洁净室(区)悬浮粒子的测试方法》GB/T 16292-2010 6 《医药工业洁净室(区)浮游菌的测试方法》GB/T 16293-2010 7 《医药工业洁净室(区)沉降菌的测试方法》GB/T 16294-2010
注:
(1)在静态条件下洁净室(区)监测的悬浮粒子数、浮游菌数或沉降菌数必须符合规定。测试方法应符合现行国家标准《医药工业洁净室(区)悬浮粒子的测试方法》GB/T 16292 、《医药工业洁净室(区)浮游菌的测试方法》GB/T 16293 和《医药工业洁净室(区)沉降菌的测试方法》GB/T16294 的有关规定;
(2)空气洁净度100 级的洁净室(区)应对大于等于5μm 尘粒的计数多次采样,当大于等于5μm 尘粒多次出现时,可认为该测试数值是可靠的。
(3)洁净室(区)的温度和湿度,应符合下列规定:生产工艺对温度和湿度无特殊要求时,洁净室(区)温度应为18~26℃,相对湿度应为45%~65 %
…… …… 余下全文
