EDQM:(PA/PH/OMCL (05) 47 DEF) 2005.6
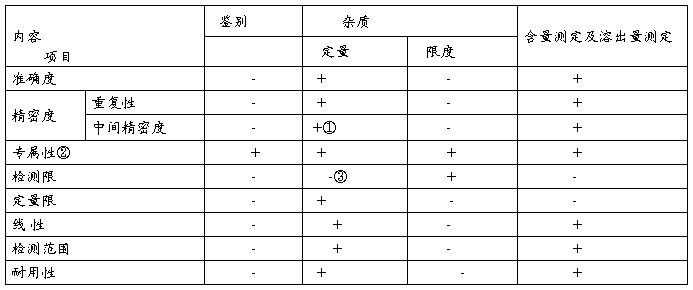
分析方法验证
官方药品检验所(OMCL)的指导性原则
介绍
ICH指导原则中的Q2A和Q2B这两个篇章分别描述了“分析方法的验证:定义/术语和方法学”,同时明确了在分析方法验证中必须考虑的验证项目等一系列讨论,这两个指导原则也同时适用于兽药。这主要适用于制药行业的注册文件中需要提供的验证数据。而这些验证数据能证明提议的检验方法和可接受的质量标准是可控的,是能保证产品放行时的质量重现性和货架寿命期内的质量充分可控(稳定性)。
由于官方药品检验所和制药公司工作的环境是不一样的,制药公司在大多数情况下没有分析程序,而经常在很短的一段时间内反映说做过了,因此我们需要重新考虑在完成一个分析方法前所要求的分析验证的程度。另一方面,也是为了保证递交的结果在任何情况下都是可信的。在这里必须强调:在进行验证研究和检验产品时适当的标准物质也是一个重要的因素。使用普遍接受的标准物质,在一定环境下可以免除一些验证项目的考虑,主要是一些生物产品,这些随后被证明是可行的。
这篇文档的适用范围(特指从事于OMCLs):根据以下不同的环境情况,给验证所需的程度提供指导性原则:分析的目的(如不依从性筛选),一定数量的验证数据是可用的(如方法转移情形),在个别OMCL实验室中已经使用经验性的或历史性的数据(如从复杂的矩阵中得到的;标准滴定的常规使用甚至是不同物质的滴定)等。这篇文档也同样适用于合成产品和生物制品。这不适用于普通的实验室操作:如设备的特殊使用,校准等。
…… …… 余下全文

 方法名称:
方法名称: 

 验证单位: 测试日期:
验证单位: 测试日期: 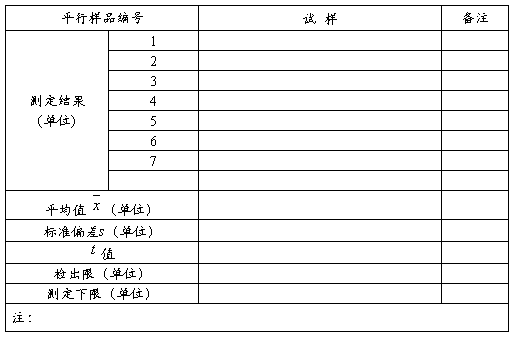
 验证单位: 测试日期:
验证单位: 测试日期: 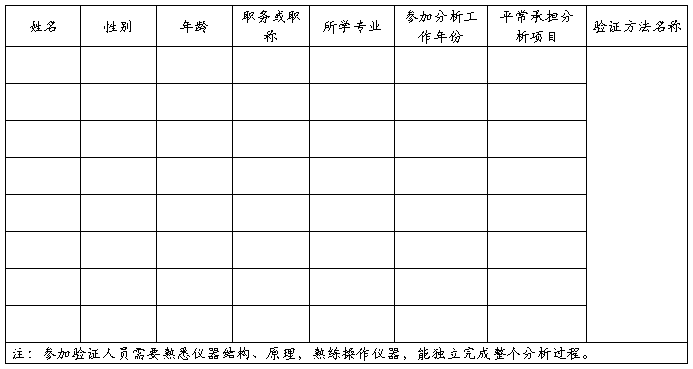
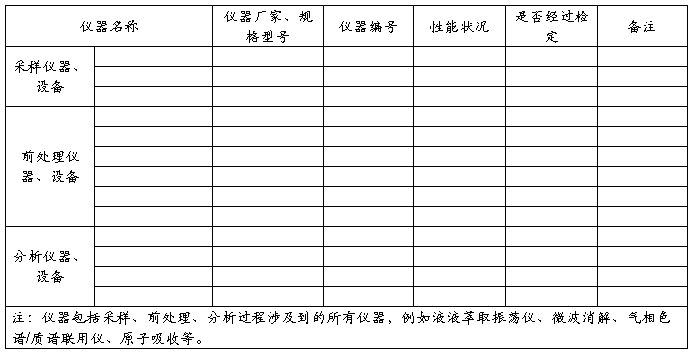
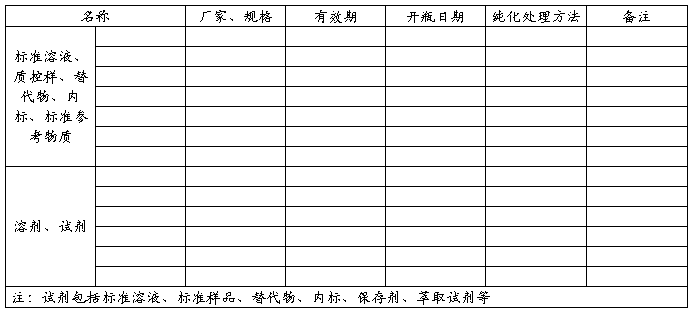
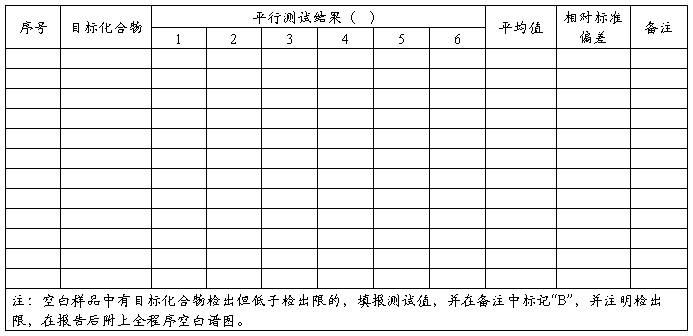
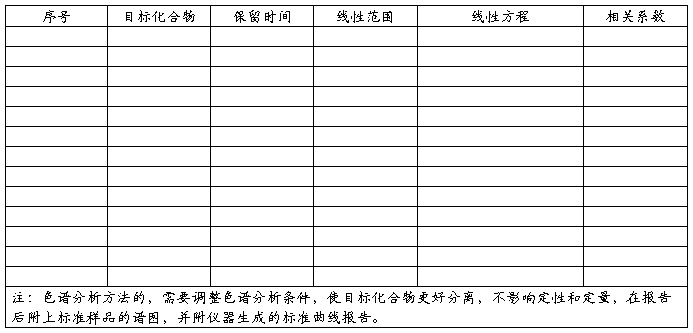
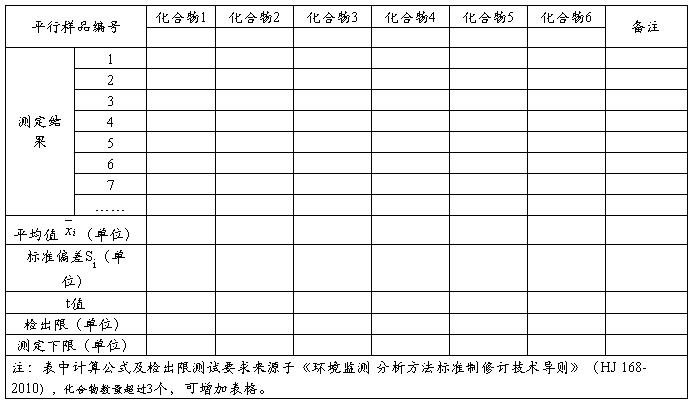
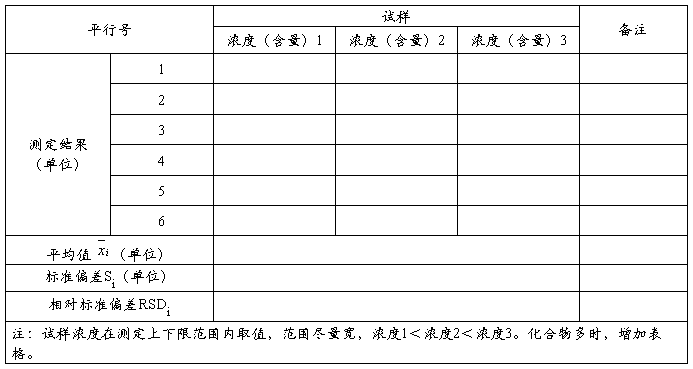
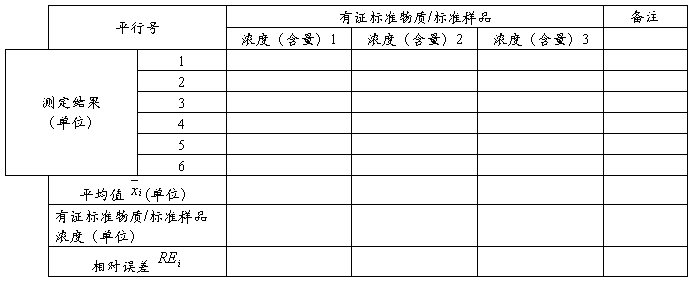
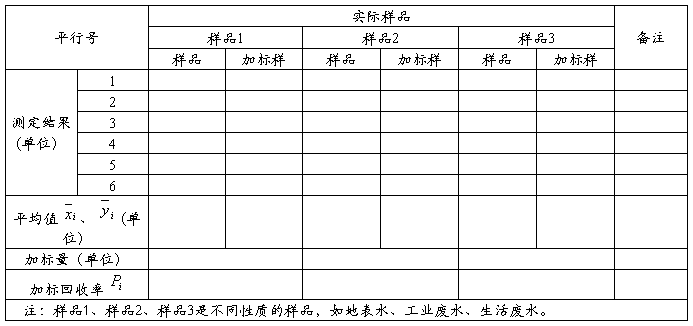
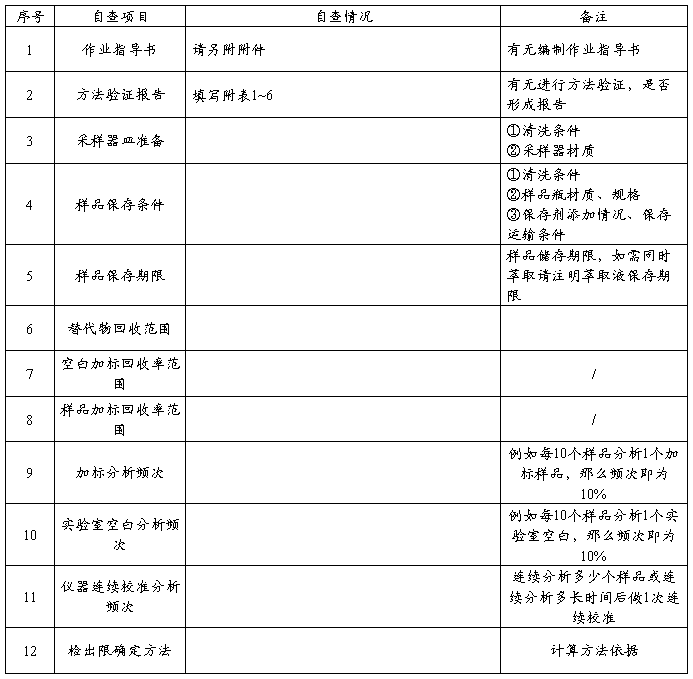
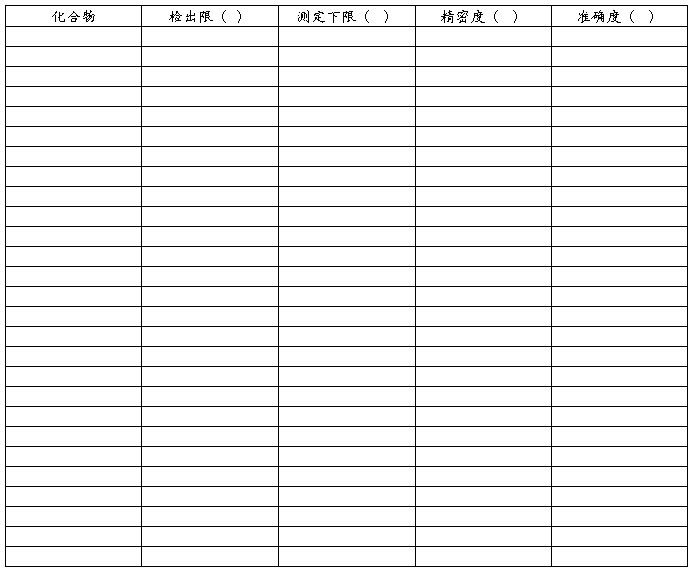


 分析方法验证报告
分析方法验证报告