明矾的制备、组分含量测定及其晶体的培养
一. 实验目的
1. 熟练掌握无机物的提取、提纯、制备、分析等方法的操作及方案设计。
2. 学习设计综合利用废旧物的化学方法。
3. 学习从溶液中培养晶体的原理和方法。
4. 自行设计鉴定产品的组成、纯度和产率的方法,并鉴定之。
仪器和试剂
( 1 )仪器
100cm3 烧杯,布氏漏斗,抽滤瓶,表面皿,玻璃棒,试管,电子天平,容量瓶(250 mL、100mL),移液管,锥形瓶(两个),电炉,温度计。
( 2 )试剂
废铝(易拉罐), KOH (1.5mol·dm-3),NH3 · H2O (6mol·dm-3),H2SO4(9mol·dm -3),HAc (6mol·dm-3),KAl(SO4)2·12H2O 晶种, BaCl2 (1mol·dm-3), pH 试纸,涤纶线EDTA溶液(0.02205 mol·L-1),二甲酚橙(XO,2g·L-1)水溶液,
NaOH溶液(200 g·L-1,贮于塑料瓶中),HCl(6mol·L-1,3mol·L-1),NH3·H2O(1+1),
六次甲基四胺溶液(200g·L-1),Zn2+(0.01089 mol·L-1);
NH4F溶液(200 g·L-1,贮于塑料瓶中),
KOH溶液:(1.5mol/L 取42.08g KOH溶于500ml蒸馏水中),
氯化钡溶液:0.25g/mL ;取25.45克氯化钡溶于100mL蒸馏水中
硫酸根标准贮备溶液(550ug/mL):准确称取0.2210g(称准至0.0001g)已烘干的基准硫酸钾溶于100mL 水中,全量转入250mL 容量瓶中,加水定容,摇匀。
二. 实验提要
目前使用的铝制品的包装和用具较多,因此废旧饮料罐、盒,铝质导线等废铝很多,设计简便的方法由铝制的易拉罐制备明矾(KAl(SO4)2-·12H2O),并培养明矾的单晶,计算产率和鉴定产品的质量。
1、实验原理
( 1 )明矾的制备
将铝溶于稀氢氧化钾溶液制得偏铝酸钾:
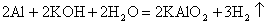
往偏铝酸钾溶液中加入一定量的硫酸,能生成溶解度较小的复盐明矾 [KAl(SO4)2·12H2O] 反应式为:
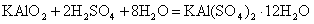
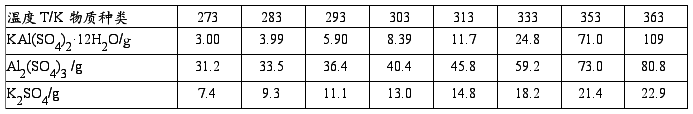
不同温度下明矾、硫酸铝、硫酸钾的溶解度( 100gH2O 中)如下表所示:
单晶的培养
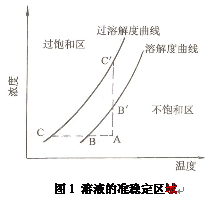 要使晶体从溶液中析出,从原理上来说有两种方法。以图1的溶解度曲线的过溶解度曲线为例,
要使晶体从溶液中析出,从原理上来说有两种方法。以图1的溶解度曲线的过溶解度曲线为例,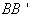 为溶解度曲线,在曲线的下方为不饱和区域。若从处于不饱和区域的 A 点状态的溶液出发,要使晶体析出,其中一种方法是采用
为溶解度曲线,在曲线的下方为不饱和区域。若从处于不饱和区域的 A 点状态的溶液出发,要使晶体析出,其中一种方法是采用 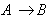 的过程,即保持浓度一定,降低温度的冷却法;另一种办法是采用
的过程,即保持浓度一定,降低温度的冷却法;另一种办法是采用 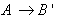 的过程,即保持温度一定,增加浓度的蒸发法。用这样的方法使溶液的状态进入到
的过程,即保持温度一定,增加浓度的蒸发法。用这样的方法使溶液的状态进入到 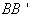 线上方区域。一进到这个区域一般就有晶核产生和成长。但有些物质,在一定条件下,虽处于这个区域,溶液中并不析出晶体,成为过饱和溶液。可是过饱和度是有界限的,一旦达到某种界限时,稍加震动就会有新的,较多的晶体析出(在图中,
线上方区域。一进到这个区域一般就有晶核产生和成长。但有些物质,在一定条件下,虽处于这个区域,溶液中并不析出晶体,成为过饱和溶液。可是过饱和度是有界限的,一旦达到某种界限时,稍加震动就会有新的,较多的晶体析出(在图中,  表示过饱和的界限,此曲线称为过溶解度曲线)。在
表示过饱和的界限,此曲线称为过溶解度曲线)。在  和
和 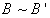 之间的区域为准稳定区域。要使晶体能较大地成长起来,就应当使溶液处于准稳定区域,让它慢慢地成长,而不使细小的晶体析出。
之间的区域为准稳定区域。要使晶体能较大地成长起来,就应当使溶液处于准稳定区域,让它慢慢地成长,而不使细小的晶体析出。
根据溶解与结晶原理,在饱和溶液中采用加入人工晶种方法培养硫酸铝钾的单晶。
KAl(SO4)2·12H2O 为正八面体晶形。为获得棱角完整、透明的单晶,应让籽晶(晶种)有足够的时间长大,而晶籽能够成长的前提是溶液的浓度处于适当过饱和的准稳定区(图 11 的 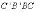 区)。
区)。
本实验通过将室温下的饱和溶液在室温下静置,靠溶剂的自然挥发来创造溶液的准稳定状态,人工投放晶种让之逐渐长成单晶。
2、制备:
制备工艺路线大致如下:

步骤及现象:
2.1.1 清除废铝表层的污染物,洗净,干燥。
2.1.2 称取1.80g 废铝,加入KOH 50ml,加热溶解。有大量的气泡产生,随着产品的溶解,溶液瞬间变成黑色,溶解到无气泡再产生,固体几乎消失时停止。
2.1.3 抽滤,取下清液。滤液显微黄色。
2.1.4 往清液中滴加0.3/LH2SO4(1.2),直至沉淀溶解。往溶液中滴加H2SO4 时产生絮状沉淀,继续滴加H2SO4 时产生白色沉淀,继续滴加H2SO4 溶液变浑浊,加热,溶液变澄清。
2.1.5 浓缩,分成两份,用两种方法结晶。
晶体的生长:
1 )然后放在不易振动的地方,烧杯口上架一玻棒,在烧杯口上盖一块滤纸,以免灰尘落下。放置一天,杯底会有小晶体析出。
2 )以缝纫用的涤纶线把0.15g 、0.10g晶种系好,剪去余头,缠在玻棒上悬吊在已过滤的饱和溶液中,观察晶体的缓慢生长。一天后,可得到棱角完整齐全、晶莹透明的大块晶体。
抽滤以上两份溶液,吹干,所得结果如下:

三. 产品鉴定
准确称取0.3642g(7.68×10-4mol)产品,加入3—5ml 1:3HCl,微热,冷却后,定容于100ml容量瓶中。(待用)
1、铝离子鉴定:
实验原理
由于Al3+易水解而形成一系列多核氢氧基络合物,且与EDTA反应慢,络合比不恒定,常用返滴定法测定铝含量。
加入定量过量的EDTA标准溶液,加热煮沸几分钟,使络合完全,继在pH为5~6,以二甲酚橙为指示剂,用Zn2+标准溶液滴定过量的EDTA。然后,加入过量的NH4F,加热至沸,使AlY-与F-之间发生置换反应,释放出与Al3+等物质的量的EDTA,再用Zn2+盐标液滴定释放出来的EDTA而得到铝的含量.有关反应如下:
pH = 3.5时,
Al3+(试液)+ Y4-(过量)=AlY- , Y4-(剩)
pH = 5~6时,加XO指示剂,用Zn2+盐标液滴定剩余的 Y4-
Zn2+ + Y4-(剩) = ZnY2-
终点: Zn2+(过量)+ XO= Zn-XO
黄色 → 紫红色
置换反应: AlY-+6F-=AlF63-+Y4-(置换)
滴定反应: Y4-(置换)+ Zn2+= ZnY2-
终点: Zn2+(过量)+ XO= Zn-XO
黄色 → 紫红色
步骤与现象:
吸取所配试液25.00ml于250ml锥形瓶中,加入10ml 0.02mol/L EDTA溶液,二甲酚橙指示剂2滴,用1:1氨水调至溶液恰成紫红色,然后滴加1:3HCl 3滴,将溶液煮沸3min左右,冷却,加入20%六次甲基四胺溶液20ml,此时溶液应成黄色,如不成黄色,可用HCl调节,再补加二甲酚橙指示剂2滴,用锌标准溶液滴定至溶液从黄色变为红紫色(此时,不计体积)。加入20%NH4F溶液10ml,将溶液加热至微沸,流水冷却,再补加二甲酚橙指示剂2滴,此时溶液应呈黄色,若溶液呈红色,应滴加1:3HCl使溶液呈黄色,再用锌标准溶液滴定至溶液由黄色变为紫红色时,即为终点。根据消耗的锌盐溶液的体积,计算Al3+的百分含量。
实验数据:
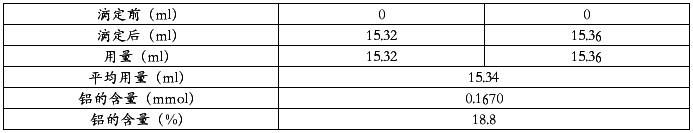
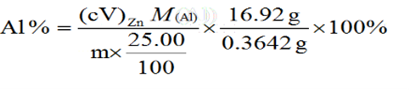
Al%=46.5%
2、硫酸根鉴定:
2.2.1 标准曲线的绘制:
精确吸取硫酸根标准溶液1、2、3、4、5mL 于5 个25mL 比色管中。同时加入0.25g/mL 氯化钡溶液直至没沉淀产生, 用蒸馏水稀释至刻度,匀速搅拌1分钟,将浑浊液倒入1 厘米比色皿中,静置4 分钟,在420nm 处,以蒸馏水作空白,分别测其吸光度。以吸取硫酸根标准溶液ml数为横坐标, 以吸光度为纵坐标绘制标准曲线。
2.2.2 样品的测定:吸取上述待用溶液1.00mL 于25mL 容量瓶中,同时加入0.25g/mL 氯化钡溶液直至没沉淀产生, 用蒸馏水稀释至刻度,匀速搅拌1分钟。将浑浊液倒入1 厘米比色皿中,静置4 分钟,在波长420nm处,以蒸馏水作空白,测其吸光度。
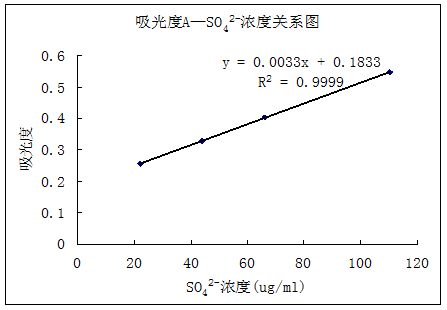
SO42-浓度与吸光度的关系

舍弃SO42-浓度为88ug/ml的一组数据。
将样品的吸光度带入y = 0.0033x + 0.1833中,得到SO42-浓度为103.5ug/ml。
Al%=
[C(SO42- )V(100ml/1ml)×M(Al)×(16.92g/0.3642g)/(M(SO42-)×2)]/m总
=[103.5ug/ml×25ml×100 ×27×(16.92/0.3642) /(96×2)]/1.80g=93.9%
对两种鉴定方法的分析:
上述两种鉴定方法得知用硫酸根离子鉴定铝的百分含量远远大于用铝离子鉴定的方法。主要原因如下:
结晶过程中用到大量的硫酸根离子,因此晶体中附着有较多的硫酸根离子。虽然在洗涤晶体时洗涤些硫酸根离子,但是还是残存大量的硫酸根离子。
该实验中比浊法的精确度比较小,但却是测定硫酸根离子浓度最简单的方法。
实验中存在的一些问题:
在晶体的培养中,由于溶液为得到饱和就加入晶种,结果晶种溶解消失。
此次实验中,由于分光光度计应用存在失误,没有调零,但是,我认为并不影响实验的结果,所以没要求做重复实验。
在该实验中,我主要负责一些理论上的计算,如硫酸根标准曲线的配制以及设计如何两种鉴定方法只使用一种溶液,实验中主要负责铝离子的鉴定。
第二篇:明矾的制备2
明矾的制备2
一、实验目的
1.了解明矾的制备方法; 2.认识铝和氢氧化铝的两性;
3.练习和掌握溶解、过滤、结晶以及沉淀的转移和洗涤等无机制备中常用的基本操作和测量产品熔点的方法。 二、实验原理
铝屑溶于浓氢氧化钠溶液,可生成可溶性的四羟基合铝(Ⅲ)酸钠Na[Al(OH)4],再用稀H2SO4调节溶液的pH值,将其转化为氢氧化铝,使氢氧化铝溶于硫酸生成硫酸铝。硫酸铝能同碱金属硫酸盐如硫酸钾在水溶液中结合成一类在水中溶解度较小的同晶的复盐,此复盐称为明矾[KAl(SO4)2·12H2O]。当冷却溶液时,明矾则以大块晶体结晶出来。
制备中的化学反应如下:
2Al + 2NaOH + 6H2O ===2Na[Al(OH)4] + 3H2↑ 2Na[Al(OH)4] + H2SO4 ===2Al(OH)3↓+ Na2SO4 + 2H2O 2Al(OH)3 + 3H2SO4 === Al2(SO4)3 + 6 H2O Al2(SO4)3 + K2SO4 + 24H2O ===2KAl(SO4)2·12H2O 三、实验仪器与试剂
烧杯,量筒,普通漏斗,布氏漏斗,抽滤瓶,表面皿,蒸发皿,酒精灯,台秤,毛细管,提勒管等。
H2SO4(3mol·L-1),NaOH(s),K2SO4(s),铝屑,pH试纸(1~14)。
四、实验步骤
1.制备Na[Al(OH)4] 在台秤上用表面皿快速称取固体氢氧化钠
2g,迅速将其转移至250mL的烧杯中,加40mL水温热溶解。称量1g铝屑,切碎,分次放入溶液中。将烧杯置于热水浴中加热(反应激烈,防止溅出!)。反应完毕后,趁热用普通漏斗过滤。
2.氢氧化铝的生成和洗涤 在上述四羟基合铝酸钠溶液中加入8mL左右的3mol·L-1 H2SO4 溶液,使溶液的pH值为8~9为止(应充
分搅拌后再检验溶液的酸碱性)。此时溶液中生成大量的白色氢氧化铝沉淀,用布氏漏斗抽滤,并用热水洗涤沉淀,洗至溶液pH值为7~8时为止。
3.明矾的制备 将抽滤后所得的氢氧化铝沉淀转入蒸发皿中,加10mL 1:1 H2SO4,再加15mL水,小火加热使其溶解,加入4g硫酸钾继续
加热至溶解,将所得溶液在空气中自然冷却,待结晶完全后,减压过滤,用10mL 1:1的水-酒精混合溶液洗涤晶体两次;将晶体用滤纸吸干,称重,计算产率。
4.产品熔点的测定及性质试验 将产品干燥,装入毛细管中。把毛细管放入提勒管中,控制一定升温速度,测量产品的熔点。测量两次,取平均值。
另取少量产品配成溶液,设法证实溶液中存在Al3+, K+和
五、注意事项
1.第(2)步用热水洗涤氢氧化铝沉淀一定要彻底,以免后面产品不离子。
纯。
2.制得的明矾溶液一定要自然冷却得到结晶,而不能骤冷。
六、思考题与参考答案
1.本实验是在哪一步中除掉铝中的铁杂质的?
答:第(1)步。因为铁与氢氧化钠不反应。
2.用热水洗涤氢氧化铝沉淀时,是除去什么离子?
答:除去Na+和离子。
3.制得的明矾溶液为何采用自然冷却得到结晶,而不采用骤冷的办法?
答:否则单盐组分可能会析出。
