水中化学耗氧量(COD)的测定(高锰酸钾法)
一、实验目的
1、对水样中耗氧量COD与水体污染的关系有所了解
2、掌握高锰酸钾法测定水中COD的原理及方法
二、实验原理
化学需氧量(COD)是反映水质受有机物污染情况的一个重大指标,本实验通过用酸性高锰酸钾煮沸消解法,对武汉东湖内的水样进行化学耗氧量的测定。测定时,在水样中加入H2SO4及一定量的KMnO4溶液,置沸水浴中加热使其中的还原性物质氧化,剩余的KMnO4用一定量过量的NaC2O4还原,再以KMnO4标准溶液返滴定NaC2O4的过量部分。 在煮沸过程中,KMnO4和还原性物质作用:
4MnO4- + 5C + 12H+ = 4Mn2+ + 5CO2 + 6H2O
剩余的KMnO4用NaC2O4还原:
2MnO4- + 5C2O42- + 16H+ = 2Mn2+ + 10CO2 + 8H2O
再以KMnO4返滴NaC2O4过量部分,通过实际消耗KMnO4的量来计算水中还原性物质的量。
三、主要试剂
0.01mol/LKMnO4 0.01mol/LNa2C2O4 1:3H2SO4
四、实验步骤
1、Na2C2O4 0.01mol/L标准溶液的配制
将Na2C2O4于100-105℃干燥2h, 准确称取6.701g于烧杯中,加水溶解后定量转移至1000ml容量瓶中,以水稀释至刻度线。取上液100ml稀至1升,得到0.01mol/L标准溶液。
2、KMnO4 0.01mol/L溶液的配制
称取3.3g KMnO4溶于1.05升水中,煮沸15min,静置2天,以“4”号砂芯漏斗过滤,保存于棕色瓶中(此溶液约0.1mol/L KMnO4溶液)。取上液100ml稀至1升,摇匀。
3、水中耗氧量的测定
用移液管准确移取100ml的水样,置于250ml锥形瓶中。加入5ml 1:3H2SO4,再加入10ml 0.01mol/L KMnO4溶液,若此时紫红色消失,应补加KMnO4溶液,记录KMnO4总体积用量V1(若紫红色不消失,则V1=10ml),置沸水浴锅30min(或加热煮沸10min),取出趁热加10ml 0.01mol/L Na2C2O4溶液,充分振荡,此时溶液应由红色转为无色(若仍为红色,可再补加5ml)。趁热用0.01mol/L KMnO4标准溶液滴定至稳定的淡红色即为终点(若滴定温度低于60℃,应加热至60-80℃间进行滴定),记录V2,平行滴定三次,记录数据。 4、求KMnO4的校正系数K值
用一份滴至终点的水样,趁热(70~80℃)加10ml Na2C2O4,立即用KMnO4滴至微红,30s不褪色,记录V2(ml)。
校正系数 K=10 / V2 (每毫升高锰酸钾标准溶液相当于草酸钠标准溶液的毫升数)
5、化学需氧量COD的计算
高锰酸钾指数(O2, mg/L)
= [(V1+V3)*K—10]*M*8*1000 / 100
式中:M—草酸钠标准溶液(Na2C2O4)浓度,mol/L;
8—氧(O)的摩尔质量,g/mol;
100—取水样体积, mL。
五、实验结果:
第一次 V1=10 V2=5.8 V3=7.4
高锰酸钾指数(O2, mg/L) = [(V1+V3)*K—10]*M*8*1000 / 100
=(17.4*10/5.8-10)*0.01*8*1000/10=160(O2, mg/L)
第二次 V1=10 V2=7.4 V3=7.4
高锰酸钾指数(O2, mg/L) = [(V1+V3)*K—10]*M*8*1000 / 100
=(17.4*10/7.4-10)*0.01*8*100=108(O2, mg/L)
第三次
V1=10 V2=6.7
V3=7.5 高锰酸钾指数(O2, mg/L) = [(V1+V3)*K—10]*M*8*1000 / 100
=(17.5*10/6.7-10)*0.01*8*100=128(O2, mg/L)
六 思考:
1、水样的采集与保存应当注意哪些事项?
2、水样加入KMnO4煮沸后,若红色消失说明什么?应采取什么措施?
1、答:水样的采集要注意具有代表性,在水的表层、中层和下层分别采样。水样保存在塑料瓶中,带回实验室,立即放入4~5℃的冰箱避光储藏。
2、答:说明水样浓度过高,还原物质很多,导致高锰酸钾被还原,红色消失。此时应该继续添加高锰酸钾,或者稀释水样后重新试验。
第二篇:化学耗氧量的测定
化学耗氧量的测定
1主题内容与适用范围
本标准规定了测定化学耗氧量的重铬酸钾快速法
本标准适用于天然水、炉水、冷却水和除盐水等水样的化学耗氧量的测定。化学耗氧量(以氧计)的测定范围为Omg/L~50mg/L,浓度大于50 mg/L时应稀释后测定。
3 方法概要
本方法基于在适当提高硫酸浓度的条件下,以提高重铬酸钾的氧化率和缩短回流时间,达到快速测定化学耗氧量的目的。测定中加入适量硝酸银和硝酸铋,以消除氯离子的干扰。
4 试剂
4.1硫酸银-硫酸溶液:
称取10g硫酸银(Ag2SO4)溶于1L硫酸(密度1.84g/mL),贮存于棕色瓶中。
4.2试亚铁灵指示剂:
称取1.48g邻菲啰啉(即1-,10-二氮杂菲)和0.70g硫酸亚铁(FeSO4·7H20),溶于200mL二次蒸溜水,
贮存于棕色瓶中。
4.3重铬酸钾标准溶液,0.004000mol/L:
准确称取1.177g优级纯重铬酸钾(预先在105℃~110℃烘箱中干燥2h并在干燥器中冷却至室温)溶于试剂水,定量转移至1L容量瓶中,稀释至刻度,摇匀。
4.4硫酸亚铁铵溶液,0.012mol/L:
称取4.70g硫酸亚铁铵〔FeS04·(NH4)2 SO4·6H20〕溶于试剂水,加10mL硫酸(密度1.84g/mL),冷却
后转移至1L容量瓶中,稀释至刻度,摇匀。此溶液在使用前按下法标定:
用移液管吸取5.OOmL重铬酸钾标准溶液(见4.3)注入于锥形瓶中,加入45mL二次蒸溜水稀释,再加5mL硫酸银-硫酸溶液(见4.1)。充分冷却后加入1滴试亚铁灵指示剂,用硫酸亚铁铵溶液滴定至颜色从蓝绿色刚变至红色为终点。记下硫酸亚铁铵溶液消耗的体积α(mL)。按下式计算硫酸亚铁铵溶液的浓度C(mol/L): C=0.004000×6×5.00/α
4.5硝酸银溶液,10%(m/V):
称取10g硝酸银溶于100mL除盐水,贮存于棕色瓶中。
4.6硝酸铋溶液:
称取1g硝酸铋〔Bi(NO3)3·5H20〕溶于100mL硫酸溶液(1+2)。
4.7二次蒸溜水:
为使空白试验和稀释用的水不含有机物,应以每升普通蒸溜水中加入约5mL硫酸(密度1.84g/mL)和0.2g纯高锰酸钾(使水保持紫红色),再蒸溜一次以制得二次水。凝汽式电厂高压炉无污染的过热蒸汽凝结水,一般也可作为二次水用。
5仪器
5.1球形冷凝器(长30m)。
5.2锥形瓶(磨口,150或250mL)O
5.3电炉(600W~800W)及石棉网。
5.4微量滴定管(10mL)。
5.5容量瓶(1000mL)。
5.6移液管(5mL,10mL)和吸液管(2mL)。
5.7秒表或计时器。
6分析步骤
6.1用移液管吸取10.OOmL水样置于回流的磨口锥形瓶中,加1mL硝酸银溶液〔10%(m/V)〕,摇匀,再加1mL硝酸铋溶液,摇匀(当氯离子含量在500~3000mg/L时,应各加2mL)。
6.2用移液管加入5.OomL0.004000mol/L重铬酸钾溶液,再加入几颗碎瓷块或沸石(预先用硫酸和重铬酸钾煮沸,洗净),装上球形冷凝器和通人冷却水。
6.3从冷凝器顶端管口慢慢加入20mL硫酸银-硫酸溶液,摇匀,用电炉加热,回流10min(从沸腾算起),停止加热。
6.4稍冷后从冷凝器顶端管口慢慢加入50mL二次蒸溜水洗涤管壁。取下锥瓶置于冷水浴中冷却至室温。
6.5加1滴试亚铁灵指示剂,过剩的重铬酸钾用硫酸亚铁铵溶液(见4.4)滴定至颜色从蓝绿色变至红棕色即为终点。
6.6另取10.OOmL二次蒸溜水按6.1~6.5条步骤进行空白试验。 7分析结果的计算
用重铬酸钾快速法测定的耗氧量按下式计算:
(CODCr)=(b-a)×C
4V
式中:(CODCr)一一用重铬酸钾快速法测定的耗氧量(以O2计),mg/L;
b一一空白试验消耗的硫酸亚铁铵溶液的体积,mL; a一一滴定水样消耗的硫酸亚铁铵溶液的体积,mL; C一一硫酸亚铁铵溶液的浓度(以Fe2+计),mol/L; 32一-1mmo1O2的质量,mg/mmoL; 1
一1mmol Fe2+所需氧(O2)的mmol数,按下式反应: 4
1 1
Fe2++2+H+=Fe3+2O
22
V一一所取水样的体积,mL;
10OO--1L的mL数,ml/L。
8允许差
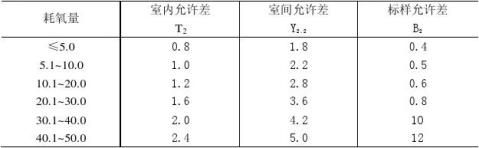
水样中耗氧量在不同范围时的允许差如表1所示。
表1
注:①取水样后要迅速测定耗氧量,如不能及时测定,应将水样加人硫酸调节pH至2以下保存,但仍不能
存放过久。 ②加硝酸银和硝酸铋时,必须按先后顺序加人,不能二者同时加人,否则氯离子的干扰不能完全消除,
使测定结果偏高。 ③所用浓硫酸必须纯净,不应含有黑色悬浮物。 ④若回流时颜色出现绿色,表示耗氧量过高,应用二次蒸溜水稀释后测定。
