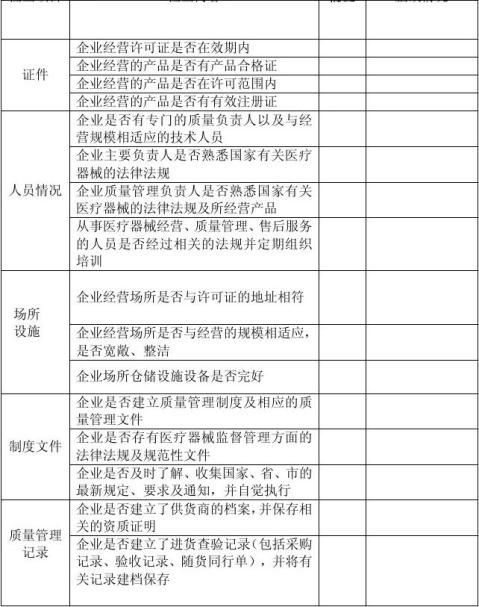
20xx年度医疗器械经营企业自查报告
企业名称: 企业负责人: 主要经营产品种类或名称: 企业地址: 联系人: 联系电话:

…… …… 余下全文
无菌医疗器械生产质量管理规范自查报告
自查企业名称:无锡市宇寿医疗器械股份有限公司 企业负责人(签名):
自查产品名称:肠道增菌片培养基
自查日期:
自查人员(内审员):
管理者代表(签名): 备案号:
…… …… 余下全文
三原县药材公司第二经营部 《医疗器械经营企业许可证》自查报告
三原县药材公司第二经营部成立于19xx年,20xx年7月换取《医疗器械经营企业许可证》;无变更情况。企业负责人桑康:注册资金5万元。企业办公经营场所注册地址为:三原县西什字,经营面积40平方米;现有员工3人;药学或相关专业人员1人。
我企业于20xx年7月换取《医疗器械经营企业许可证》,按照《陕西省医疗器械经营企业检查验收标准》的要求进行了严格的自查。现将自查情况汇报如下: (一)机构与人员
(1)、企业设置有合理的组织机构。
(2)、企业负责人为:桑康,熟悉国家有关医疗器械监督管理法规、规章。
(3)、企业设置有质量管理机构,对企业所经营产品具有质量裁决权。 质量负责人、质量管理员:柳福孝,有几十年质量管理工作经验。验收员:梁妮,中专学历。
上述质量管理人员均都熟悉国家及医疗器械相关管理法规、规章、规范性文件要求及相关专业知识,且在职在岗,无兼职现象。
20xx年2月安装了药械实时监控系统,并将器械的购进、
-1-
储存、销售数据定期上传。
(二)医药器械经营质量管理情况
(1) 企业具有与经营规模和经营范围相适应的相对独立的经营场所。
(2)经营场所面积40平方米,环境整洁、明亮、卫生。
(3)企业的营业场所集中,与生活区域分开,设置有与企业组织机构相符合的标识门牌。经营场所配备有办公桌椅、固定电话、文件柜、电脑等办公设备。
(四)技术培训与售后服务
(1)企业对从事质量管理、产品采购、质量验收、储存保管、业务销售及售后服务等岗位的人员进行了有关法规规章、专业技术、质量管理和职业道德等知识的培训,有培训计划、培训记录并建立了培训档案。
(2)企业定期收集产品的质量信息,及时上报、处理和反馈。对已销售产品如发现有质量问题,及时召回。属于国家重点监管的产品向市食品药品监督管理局报告,并及时做好记录。
…… …… 余下全文
医疗器械经营企业自查报告
企业名称:宁夏源丰医药有限公司 (盖章)
企业地址:银川市兴庆区丽景街东侧宁夏新世纪冷链物流中心6号楼04号商业房 企业法人代表:梁宪刚
企业负责人: 梁宪刚
主要经营产品种类或名称:医疗器械第Ⅱ、Ⅲ类
变更内容:20xx年12月28日
注册地址变更为:银川市德胜工业园区穆园路唐徕渠东岸
仓库地址变更为:银川市德胜工业园区穆园路唐徕渠东岸
经营范围增加 :Ⅱ、Ⅲ类:植入材料和人工器官、介入器材;注射 穿刺器械、医用高分子材料及制品、体外循环及血 液处理设备、临床检验分析仪器、口腔科材料、医 用激光仪器设备、医用电子仪器设备
质量负责人变更为:漆淑华
20xx年07月24日
注册地址变更为: 银川市兴庆区民族北街高尔夫商务楼B座25幢1101 室
20xx年05月26日
注册地址变更为: 银川市兴庆区丽景街东侧宁夏新世纪冷链物流中6 号楼04号商业房
20xx年11月20日
经营范围中增加Ⅲ类:医用光学器具、仪器及内窥镜设备
库房地址变更为: 银川市德胜工业园区奥莱路唐徕渠东岸
质量管理人员:6人 售后服务人员:2人 专业技术人员:3人
联系人: 陈丽 联系电话:181xxxxxxxx
1
医疗器械经营企业自查报告
我公司遵照国家食品药品监督管理总局关于施行医疗器械经营质量管理规范的公告(20xx年第58号)文件精神,组织相关人员重点就我公司经营的所有医疗器械进行了全面检查,现将具体情况汇报如下:
…… …… 余下全文
医疗器械经营许可证换证自查报告
一、企业概况
天津############################大药房成立于 ####年##月##日,经营地址为########,法人代表:###,企业负责人:##,质量负责人:##。
经营面积## 、仓库面积## ,公司拥有员工#人,其中验收员#人、养护员#
人、采购员#人、营业员##人。
公司经营范围包括:Ⅲ类:一次性注射器、输液器; ***
二、医疗器械经营许可证换证自查总结
自发证以来,我企业对照“医疗器械监督管理条例”各条款,认真检
查企业许可证管理的执行情况,现将发证以来的自查情况从6方面进行简要
阐述。
1、管理职责:
为全面开展、实施许可证换证工作,我公司首先结合企业实际和许可
证换证要求,修订和完善了4项质量管理制度和岗位质量职责,并及时对全
体员工进行了学习和传达。为确保各项制度能够严格执行.
2、人员:
我公司目前共有人员#人,企业负责人##为本科学历,执业药师、高级
工程师,熟悉有关器械的法律法规。质量负责人##为本科学历,执业药师、
主管中药师。营业员都具有相关专业的学历资质。
3、设施设备:
营业面积 ##、仓库面积##,营业环境与布局符合换证要求(具体见
布局图);主要设施设备有货架、陈列柜、电脑等。设备设施能够满足经营
活动的需要,并定期有专人进行检查和维护。
4、进货与验收:
购进器械严格按照器械购进制度的规定进行。对供货单位及供货单位销售人员的合法性严格审核。与供货单位每年签订质量保证协议,并明确质量条款。购进器械均有合法票据,并建立了购进记录,票、帐、货相符。
对购进的器械,首先进行购货确认,验收人员根据原始凭证对照器械逐批验收,并建立验收记录。验收中,按照要求对器械的外观性状以及内外包装、标签、说明书、标识等内容进行详细检查,
5、陈列与养护
器械按用途摆放整齐美观,类别标签放置准确,字迹清晰。对陈列器械进行养护,至今未发现质量问题。
…… …… 余下全文

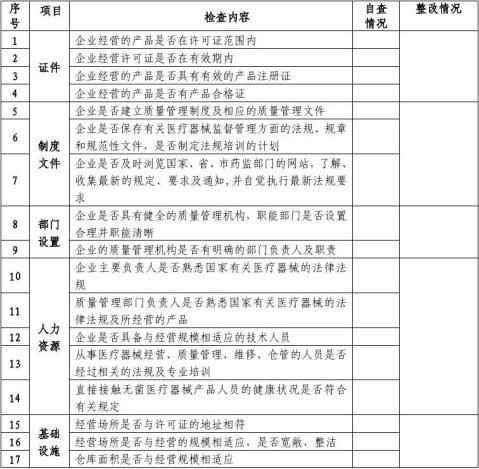
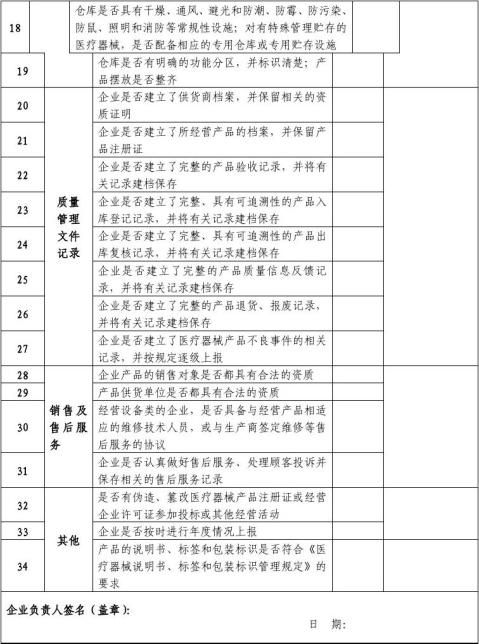
说明
按照《医疗器械生产企业质量体系考核办法》(局令22号)的要求,为了提高企业对质量管理体系自我检查的能力,统一检查标准,制定本自查报告以供参考。企业在申请质量管理体系考核之前,应按照本报告要求进行全面自查,并按要求逐项填写。
1.三类产品其中重点考核项目(条款前加“*#”)21项;二类产品其中重点考核项目(条款后加“*”)12项;重点考核项目有一项不合格,则考核不予通过。
2.企业可以根据申请考核产品的特点,对“不适用条款”应当说明“不适用的理由”。检查组予以确认。
3.对自查结果的填写,要求描写可核查的事实。对于只填写“是”“符合”的,可以作为资料不全退回补充。
4.企业承诺对自查情况的真实性负责,并愿意承担任何由于失实而引起的法律后果。
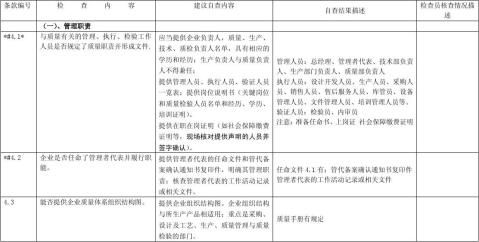
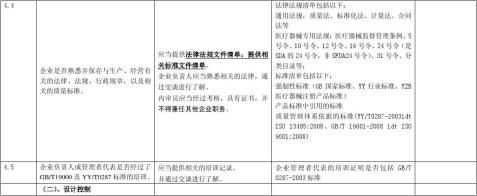
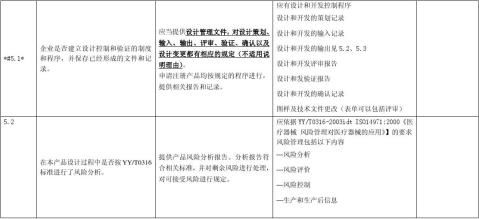
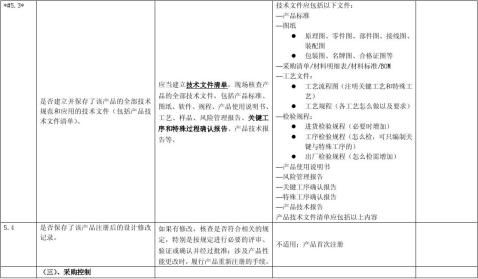
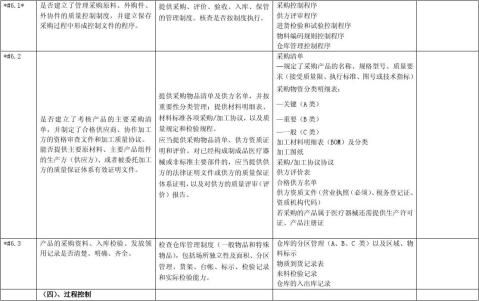
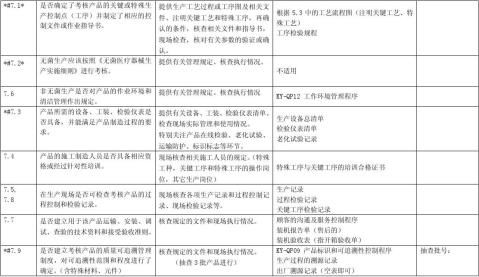
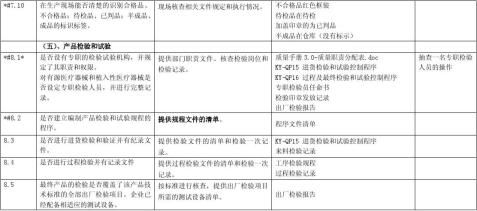

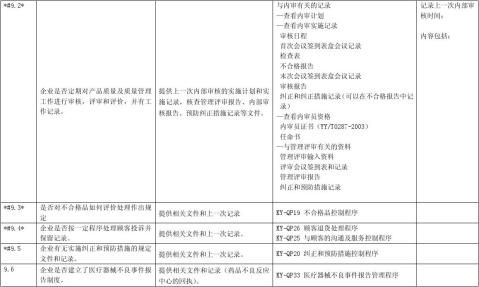
备注:条款前有*#为三类产品的重点检查项目,条款后有*为二类产品的重点检查项目,其它为一般检查项目。
自查结论:重点检查项目合格 项,不合格 项;一般检查项目合格 项,不合格
项。不合格的写出具体内容,并提交整改措施。
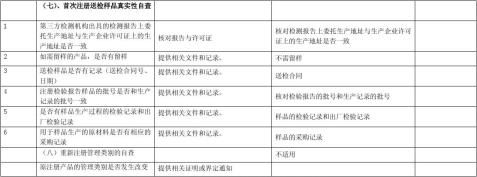
…… …… 余下全文
附件1
第三类医疗器械批发企业
企业名称: (盖章) 企业地址:隶属区局: 企业负责人:手机: 联 系 人: 电话: 手机:
年度基本情况表
填报单位: 填报时间:
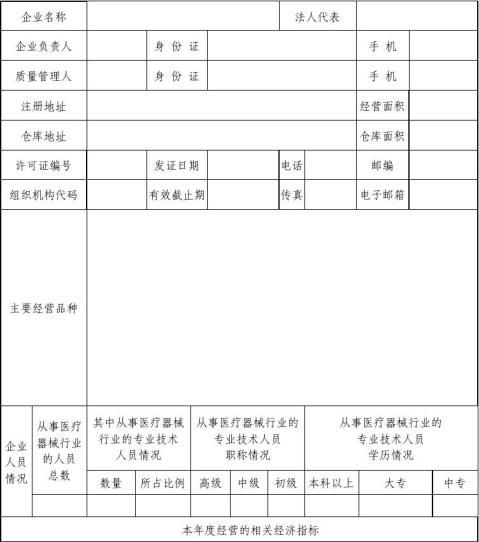
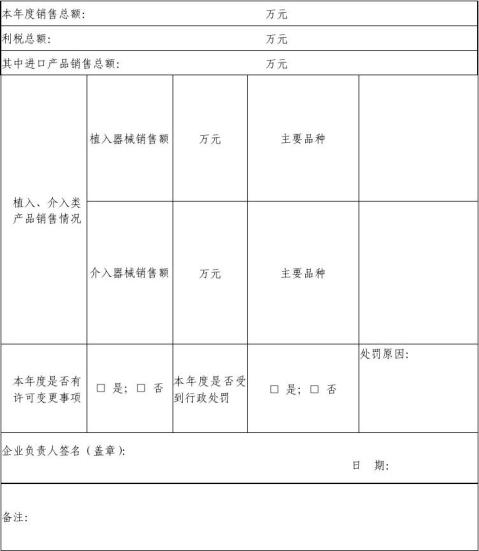
年度自查情况表
填报单位: 填报时间:

医疗器械经营企业自查承诺书
武汉市 区食品药品监督管理局:
为加强医疗器械经营管理,确保经营的医疗器械质量符合要求,我公司于 年 月 日对医疗器械经营管理进行了自查,现将《武汉市医疗器械经营企业自查报告》(以下简称《自查报告》)报送区局,为此我们保证:
一、我们按照医疗器械监督管理法规、规章的要求,对我公司医疗器械经营全过程进行了自查,并对发现的问题进行了整改(或制定了整改方案)。
二、《自查报告》反映的情况真实。
三、我们承担报送不真实《自查报告》所产生的相关责任。
企业名称:
企业负责人(签名):
年 月 日(公章)
…… …… 余下全文
医疗器械经营企业年度自查报告
(20xx年度)
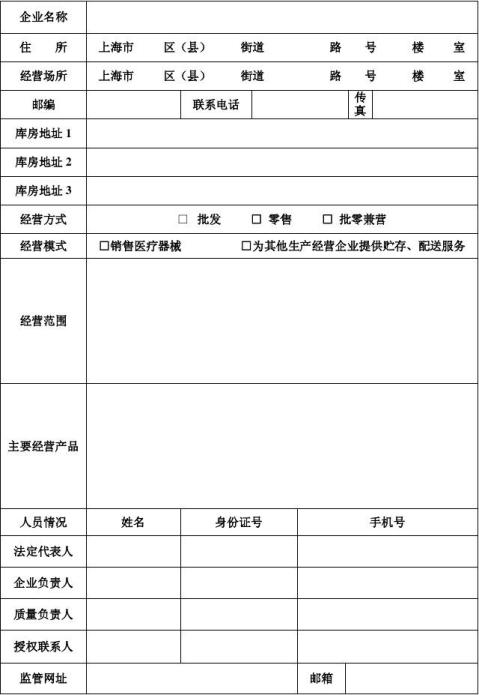

填表说明:1.本表按照实际内容填写,不涉及的可缺项。其中,企业名称、住所、法定代表
人、等按照营业执照内容填写。
2.本表经营范围应当按照国家食品药品监督管理部门发布的医疗器械分类目录
中规定的管理类别、分类编码及名称填写。
…… …… 余下全文
