玻璃综合性设计实验
实验方案设计报告
玉石玻璃材料的制备及性能测定
班 级:无非0802
姓 名:
指导老师:
日 期:20##年11月10日
沈阳化工大学材料科学与工程学院
一、文献综述
普通的玻璃是用石英砂、纯碱和石灰石一起熔炼而成的。它是一种组成不固定的硅酸盐的混和物。人们最先制造出来的玻璃是一些透明度差,带有一些颜色的小玻璃片。它的颜色并不是人们有意识地加进去的,而是所用的原料不纯,混进了杂质的结果。那时的颜色玻璃只是用来做装饰品,要求不高,人们只是偶然生产出了颜色玻璃。
经过研究,人们发现如果在普通玻璃的配料中加入0.4~0.7%的着色剂,就能使玻璃带上了颜色。着色剂大多是金属的氧化物。每种金属元素都有它独特的“光谱特征”,所以不同的金属氧化物都能呈现出不同的颜色。如果在玻璃配料中加入这些氧化物就给玻璃着上了色。其实,玻璃的颜色不仅取决于加入的着色剂,人们还通过熔炼的温度及炉焰的性质来调节元素的化合价,使玻璃呈现不同的颜色。例如玻璃中的铜,如果以高价的氧化铜存在时玻璃显现蓝绿色;以低价的氧化亚铜存在时,玻璃呈红色。有时,烧熔一次还不能使玻璃显示出色来,再要进行第二次加热才能使玻璃显出颜色。名贵的金红玻璃就是这样,它是在普通的玻璃配料中加入微量的金子烧制成的。第一次烧熔后,金以原子形式分布在玻璃中,此时玻璃并不显颜色;当再次加热到接近软化的温度时,其中的金原子聚合成胶状颗粒,此时玻璃就显现出了美丽的红色。
目前,人们又用稀土元素的氧化物为着色剂制成了各种高级的颜色玻璃。掺有稀土元素的颜色玻璃,色调明净,有光亮的色泽,甚至还会在不同的光线下改变颜色。例如氧化钕玻璃中就有这种特性,它在日光下显紫红色,在荧光下显蓝紫色,十分美丽。有一种玻璃会随着光线的强弱而改变颜色,人们用它作眼镜的镜片和房屋的窗户玻璃。用这种玻璃作窗玻璃,室内可以保持一定的光亮度,再也用不着用窗帘子来遮阳,所以有人称它为“自动窗帘”。它又能阻挡阳光中的紫外线通过,图书馆藏书室和博物馆装上这种玻璃以后,可以保护书籍和文物不受紫外线的破坏。
除稀土元素外,在玻璃中直接添加钨和铂,也可以做成变色玻璃。
向玻璃原料中添加能够形成着色离子、化合物胶体及金属胶体粒子的物质,使之呈现不同颜色的工艺,按照着色机理可分四种类型:离子着色、化合物胶体粒子着色、金属胶体粒子着色、半导体着色。
颜色玻璃也被用于制成人工玉石。人工宝石包括合成宝石、人造玉石、拼合宝石和再造宝石。可见人造宝石只是人工宝石的一部分,故不能将人工宝石称为人造宝石。合成宝石与人造宝石的主要区分是:如果在自然界中有对应的天然宝石,且其物理和化学性质、矿物内部结构与对应的天然宝石相同,则称“合成宝石”,如合成水晶、合成祖母绿、合成立方氧化锆、合成红、蓝宝石、合成金红石等等;若在自然界中没有对应的天然宝石,只是外表的颜色、透明度、硬度等像某种天然宝石,但其物理和化学性质、矿物内部结构等都与这种天然宝石不一样,甚至它不像任何天然宝石,仅可作为宝石用,这些人工合成的宝石统称为人造宝石(有时人们把某些人造宝石叫仿宝石),如人造钇铝榴石(YAG)、人造钆镓榴石(GGG)、人造钛酸锶、人造夜光宝石、人造玻璃猫眼、仿金星石、仿绿松石、仿珊瑚、仿珍珠等等。
本次实验的研究对象是离子着色的玉石玻璃,实验目的是研究不同着色剂对玻璃颜色的影响。
本次实验的意义是:通过本次实验了解玻璃中得各氧化物在玻璃中得作用,各氧化物由何种原料引入,玻璃成分设计的依据,玻璃配方调整的方法,理解玻璃的熔制过程,以及颜色玻璃的着色机理,了解和掌握相关仪器设备的使用。
二、化学组成设计
(1)设计题目:离子着色的玉石玻璃组成
(2)性能要求:由于实验条件的限制,在满足玻璃所设计的玻璃组成能够形成玻璃的基础上,要求玻璃的熔制温度在1350℃以下,因此要引入能够降低玻璃熔点的物质,如钡化合物、氟化物等。为了缩短料性,使玻璃易于成型,还要适度减少钙的含量。因此,玻璃设计组成为:
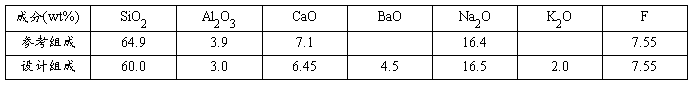
(3)玻璃性能:
①玻璃的熔制温度:
Ledererova计算式:
式中: —常数
—常数  —计算系数
—计算系数  —玻璃成分百分含量
—玻璃成分百分含量
因此,由上式知
玻璃的退火温度:

式中:x—Na2O% y—CaO% z—Al2O3% A=-7.32 B=3.49 C=5.37 D=603.4
因此,由上式知

②玻璃的密度
Knapp法
③玻璃的折射率
Huggins法 
式中: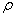 —玻璃密度
—玻璃密度  —折射率加和系数
—折射率加和系数  —玻璃成分质量分数
—玻璃成分质量分数
其中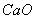 的
的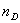 系数=
系数=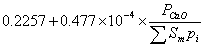
=0.2258
 的
的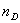 系数=
系数=
=0.1294
因此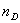 =1.45
=1.45
④玻璃的热膨胀系数
高桥法:


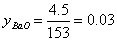
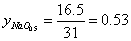




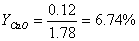
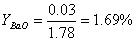

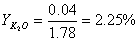
0~400℃时
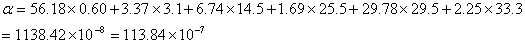
⑤玻璃的化学稳定性

 :
:

式中:B—玻璃耐水性,将2g玻璃粉末加入50ml蒸馏水中,加热到98℃并保持60mi以析出Na O mg数表示
O mg数表示
P ,P
,P ,P
,P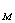 ,P
,P ,P
,P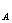 ,P
,P —分别代表Na
—分别代表Na O,K
O,K O,MgO,CaO,Al
O,MgO,CaO,Al O
O ,Fe
,Fe O
O
含量
因此
三、玻璃的原料
本实验所选用的原料是:石英粉、 (32~35%水分)、碳酸钙、
(32~35%水分)、碳酸钙、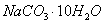 、
、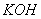 (
( )、
)、
四、配方计算:100g玻璃为基准
①需Na SiF
SiF 的量:
的量: ,引入Na:3.05g Si:1.85g
,引入Na:3.05g Si:1.85g
②需SiO 的量:
的量: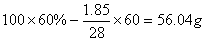
③需CaCO 的量:
的量:
④需BaCO 的量:
的量: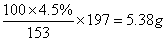
⑤需KOH的量:
⑥需Na CO
CO 的量:
的量: ,补充0.47g,共需14.68g
,补充0.47g,共需14.68g
需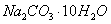 的量:
的量: g
g
⑦需Al 的量:
的量: ,又Al
,又Al 含32%~35%的水分,取33%得Al
含32%~35%的水分,取33%得Al 的量:
的量:
100g玻璃所需配料

五、实验方案设计
玻璃的熔制过程是将配合料经过高温加热,配合料发生一系列物理的,化学的,物理化学的现象和反应,最后使之成为符合要求的玻璃。这一过程是一个非常复杂的过程,一般把玻璃熔制过程分为五个阶段,即硅酸盐形成、玻璃形成、澄清、均化和冷却。
由前面计算得:加料1000℃左右,澄清1339℃,成型1000℃左右。
本次实验共制作2种颜色玻璃,分别加入MnO 和CuO+Cr2O3为着色剂,然后比较2种玻璃的差异。
和CuO+Cr2O3为着色剂,然后比较2种玻璃的差异。
六、实验仪器设备
①箱式电阻炉;
②茂福炉(型号:SM-2.8-12);
③瓷坩埚若干、研钵;
④其他物品,如坩埚钳、石棉手套、氧化铝粉、坩埚套、炉铲、加料勺、搅拌棒、墨镜、石棉板、成型模具等。
七、实验步骤
①烘烤电炉
②预热坩埚:将坩埚放入马弗炉内预热。
③加料:将温度升到1000℃左右,向坩埚内加入配料1/3左右。炉温将有所下降。待温度升到加料温度保温15min左右,再根据融化情况分次加料,直至加完为止。
④融化和澄清:电炉在1000℃保温15min后,以5~10℃/min的升温速率至澄清温度1340℃,保温2h。
⑤搅拌和观察:在高温炉保温期间,可用不锈钢棒或包有白金的棒搅拌玻璃1~2次,同时取样观察,若已无密集小气泡仅仅有少量大气泡时,玻璃熔制结束,否则需适当延长澄清事件或提高澄清温度。
⑥玻璃的成型
⑦玻璃的退火
八、性能测试
本次实验所测试的玻璃性能为玻璃的密度和化学稳定性。
