10.2 结晶水合物中结晶水含量的测定
[考纲要求] 1. 结晶水合物中结水含量的测定原理;2瓷坩埚、研钵、干燥器等仪器的正确使用;
3.恒重等基本操作技能;4.按操作程序分析操作不当引起实验误差的技能。
分点清理 查漏补缺
考点一:结晶水合物中结晶水含量的测定
【基础再现】
一.硫酸铜晶体的组成、性质及用途
五水硫酸铜俗称胆矾、蓝矾。是一种结晶水和物其化学式为:CuSO4·5H2O,是一种蓝色固体,其水溶液为蓝色,固体受热时变为白色粉末,硫酸铜水溶液能杀菌消毒,游泳池里水变蓝是放了硫酸铜的缘故。用作纺织品媒染剂、农业杀虫剂、水的杀菌剂,饲料添加剂,并用于镀铜。
我国劳动人民很早就认识了铜盐,在汉代许多著作里有记载“石胆能化铁为铜”,晋葛洪《抱朴子内篇·黄白》中也有“以曾青涂铁,铁赤色如铜”的记载。这是我国劳动人民发明的水法炼铜,即用铁把铜盐溶液里的铜置换出来,它成为湿法冶金术的先驱,在世界化学史上占有光辉的一页。
在欧洲,湿法炼铜出现比较晚。15世纪50年代,欧洲人把铁片浸入硫酸铜溶液,偶尔看出铜出现在铁表面,感到十分惊讶,更谈不上应用这个原理来炼铜了。
二.结晶水含量测定的原理
?? CuSO4 + xH2O 化学反应CuSO4· xH2O?
所测数据:硫酸铜晶体质量m1 ,无水硫酸铜质量m2
??CuSO4+xH2O CuSO4·xH2O?
160+18x 160 18x
m1g m2g (m1-m2)g
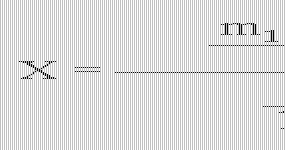
(160+18x) :160 = m1 : m2 或 160 :18x = m2 :( m1-m2 )
计算公式
三、测定硫酸铜结晶水含量的实验方案设计
请完成下列设计:1.实验设计思路
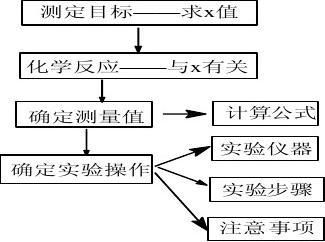
2.实验步骤
(1)研磨:在研钵中将硫酸铜晶体研碎。
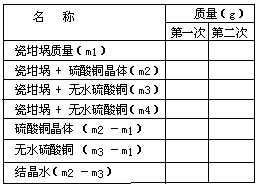
(2)称量:准确称量一干燥洁净的瓷坩锅质量(m1)。
(3)再称:称量瓷坩埚+硫酸铜晶体的质量(m2)。
(4)加热:加热至蓝色晶体全部变为白色粉末,并放入干燥器中冷却。
(5)再称:在干燥器内冷却后,称量瓷坩埚+硫酸铜粉末的质量(m3)。
(6)再加热:把盛有硫酸铜的瓷坩埚再加热,再冷却。
(7)再称重:将冷却后的盛有硫酸铜的瓷坩埚再次称量(两次称量误差不得超过0.001 g)。
(8)计算:根据实验测得的结果计算硫酸铜晶体中结晶水的质量分数。
数据记录表,再实验平均值
【深度思考】
1、测得硫酸铜晶体中结晶水的质量分数实验所用的主要仪器有_____________________________________.
2、这是一个较精确的定量实验,为了减小误差,实验操作中应注意那些事项?确保测定准确的关键操作有那些?
3、无水硫酸铜易吸收空气中的水,能否放在空气中冷却?__________________________________________
第二篇:胆矾结晶水测定误差分析
胆矾结晶水测定误差分析
1、加热前,称量时容器未完全干燥。
2、晶体未研细。
3、加热过程中有少量晶体溅出
4、晶体不纯,含有不挥发杂质。
5、坩埚内附有不挥发杂质。
6、粉末未完全变白就停止加热。
7、加热时间过长,部分变灰。
8、加热后在空气中冷却称量。
9、在称量坩埚时由于是上一班的同学刚做过实验,坩埚内壁上有少量的无水硫酸铜。
10、在称量坩埚时由于是上一班的同学做过实验,坩埚内壁上有少量的已略变蓝色硫酸铜。
11、加热后硫酸铜晶体仍有蓝色。
12、坩埚内壁有少量的NH4Cl。
13、硫酸铜晶体中有少量的CuCl2·5H2O 。
14、硫酸铜晶体中有少量的NH4Cl。
15、硫酸铜晶体中有少量的NaCl。
【实验关键】1. 能不能用称量纸先称出晶体的质量,再倒入瓷坩埚中?
不可以,多次称量会扩大误差值。
2.在硫酸铜晶体加热过程中何时停止加热?如果出现灰色物质,说明什么?
当坩埚中物质变为白色后停止加热。变灰说明有CuO产生。
3、加热过程中为何要不断搅拌?如何加热?
搅拌防止局部过热使晶体发生飞溅,小火慢慢加热
4、如何判断晶体已经完全失去结晶水。
“恒重操作”,两次称量相差小于0.001g。
5、实验中至少要称量几次?
称量4次
高 低 高 低 不变 低 高 低 不变 高 低 高 高 高 不变
