硫代硫酸钠的制备
摘 要:用亚硫酸纳法制备硫代硫酸纳,在制备过程中要注意控制反应过程中的温度,以及在减压热过滤、冷却、结晶、过滤过程中要认真操作每一个过程以便提高产量。
关键词:硫代硫酸纳 制备
前 言:硫代硫酸纳俗称海波、大苏打为无色透明单斜晶体,无臭、味咸,相对密度1.729(170度),33度以上干燥在空气中易风化56度熔于结晶水,100度失去结晶水。易溶于水,难溶于醇,水溶液加酸会导致其分解。硫代硫酸纳有较强的还原性和配位能力可作为定量分析中的还原剂。
实验原理
 制备反应: Na2SO3 + S + 5H2O === Na2S2O3 ·5H2O
制备反应: Na2SO3 + S + 5H2O === Na2S2O3 ·5H2O
定性检验: S2O32- + 2 H+ = SO2↑+ S↓ + H2O
定量分析: 2S2O32- +I2= S4O62-+ 2I-
SO32- + I2+ H2O= SO42-+ 2I- +2 H+
仪器及试剂
仪 器: 抽滤瓶、布氏漏斗、烧杯、玻璃棒、蒸发皿、表面皿、量筒、试管、电热套。
固体药品:硫粉、亚硫酸钠(无水)。
液体药品:乙醇(95%)、HCl (6 mol/L)、I2标准溶液(0.05000 mol/L)、淀粉溶液(0.2%)、硝酸银溶液(1 mol/L)、溴化钾溶液(1 mol/L)、酚酞、。
材 料:pH试纸、滤纸。
实验步骤
1.5g硫粉、3ml乙醇置于烧杯中→5.1g Na2SO3 、40ml H2O置于小烧杯中→将小烧杯中的溶液移至烧杯中→加热近沸,反应约一个小时至少许硫粉悬浮于溶液中(不少于20ml)→趁热减压过滤→ 滤液(有色则用活性炭脱色)→蒸发、浓缩(至3-4ml)→冷却→结晶(必要时加少量晶种)→抽滤→少量乙醇洗涤→晶体→抽干→称量、回收、计算产率。
产品检验的定性检验
(1)取适量产品溶于试管中,往其中逐步滴加入硝酸银溶液,得到黄色沉淀,然后沉淀变棕色,最后变黑色,证明硫代硫酸根离子存在。
(2)取适量产品溶于试管中,再滴加数滴6 mol/L HCl,并迅速将湿润的蓝色石蕊试纸置于试管口,试纸变红且溶液变浑浊,证明硫代硫酸纳遇酸不稳定。
(3)取适量产品溶于试管中,往其中滴入少量碘液并振荡,再往其中滴加淀粉溶液,溶液无色澄清透明,证明硫代硫酸钠具有还原性。
(4)往试管中滴加5滴硝酸银溶液和6滴溴化钾溶液,得到溴化银淡黄色沉淀,再往试管中滴入由产品所配得的溶液,沉淀溶解、溶液澄清透明,证明硫代硫酸钠具有配位能力。【M】
产率的计算
理论Na2SO3的产量为m=10g
实际产量 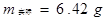
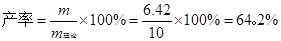
实验心得及分析
(1)实验结果产率比较低,原因可能有二:其一,过分干燥,产品结晶水少;其二:操作过程抽滤过程造成产品流失。
(2)产品中混有微量褐色杂质,源于抽滤瓶在预热过程中被污染。
(3)蒸发浓缩的温度控制不好,完成实验所用的时间过长。
【参考文献】
【1】古风才、肖衍繁.基础化学实验教程【M】北京:科学出版社.2000
【2】高华寿、陈恒武,罗崇建.分析化学实验【M】3版.北京:高等教育出版社
第二篇:硫代硫酸钠标准液配制与标定
实验八 硫代硫酸钠标准溶液的配制与标定
一、试验目的
1)掌握硫代硫酸钠标准溶液的配制与标定方法;
2)掌握碘量法的原理及测定条件。
二、原理
硫代硫酸钠(Na2S2O3·5H2O)一般都有含有少量杂质,如S、Na2SO3、Na2SO4、Na2CO3及NaCl等,同时还容易风化和潮解,因此不能直接配制准区浓度的溶液。
Na2S2O3溶液易受空气及水中CO2、微生物等的作用而分解,为了减少溶液在水中的CO2和杀死水中的微生物,应用新煮沸后冷却的蒸馏水配制溶液并加入少量Na2CO3(浓度为0.02%),以防止Na2S2O3分解。
日光能促进Na2S2O3溶液分解,所以Na2S2O3溶液应贮存在棕色瓶中,放置暗处,经8~14天在标定。长期使用的溶液,应定期标定。 通常用K2Cr2O7作基准物进行标定Na2S2O3溶液的浓度。K2Cr2O7先与KI反应析出I2:
K2Cr2O7+6KI+14HCl=2CrCl3+8KCl+3I2+7H2O
析出的I2再用Na2S2O3标准溶液滴定:
I2+2Na2S2O3=2NaI+ Na2S4O6
这个测定方法是间接碘法的应用。
三、试剂
Na2S2O3·5H2O(固体)
Na2CO3(固体);
K2Cr2O7(G.R或A.R);
0%KI溶液;
6mol·L-1HCl溶液;
0.2%淀粉指示?。
四、实验步骤
1)Na2S2O3溶液的配制
将12.5gNa2S2O3·5H2O与0.1gNa2CO3放入小烧杯中,加入?煮沸并已冷却的蒸馏水使溶解,稀释至500mL,贮于棕色瓶中,在?处放置8~14天后在标定。
2)标定
精确称取适量在130~110℃烘干的(G.R)K2Cr2O7,放入250mL碘量瓶中,加?25mL使溶解。加入6mol·L-1HCl溶液5mL及20%KI溶液5mL,轻轻摇匀,将瓶盖好,放在暗处反应5min。然后加入100mL水稀释,立即用Na2S2O3标准溶液滴?到溶液呈草黄色,加入0.2%淀粉指示剂5mL,继续滴定至溶液由肁色变为绿色,即位终点。
五、注意事项
1)K2Cr2O7与KI反应不是立刻完成的,在稀溶液中反应更慢,因此等反应完成后再加稀释自上述条件下,大约经5min反应即可完成。
2)因生成的Cr3?浓度较大时为暗绿色,妨碍终点观察,故应稀释后再滴定。开始滴定时?溶液中碘浓度较大,不要摇动太厉害,以免I2挥发。
