化学与制药工程学院
工业分析专业实验
实验题目:氯化物中氯含量的测定(莫尔法)
班 级: 应化0704 学 号: 07220412
姓 名: 实验日期:
实验题目:氯化物种氯含量的测定(莫尔法)
一、摘要
某些可溶性氯化物中氯含量的测定常采用莫尔法,本实验以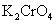 为指示剂,用
为指示剂,用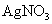 标准溶液在中性或弱碱性不含其他干扰离子的溶液中进行滴定 ,对氯化物中氯含量进行了定量分析。
标准溶液在中性或弱碱性不含其他干扰离子的溶液中进行滴定 ,对氯化物中氯含量进行了定量分析。
二、实验目的
1、熟练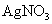 标准溶液的配制和标定;
标准溶液的配制和标定;
2、掌握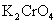 指示剂的应用原理;
指示剂的应用原理;
3、掌握用莫尔法进行沉淀滴定的原理、方法和实验操作。
三、实验原理
某些可溶性氯化物中氯含量的测定常采用莫尔法。莫尔法是在中性或弱碱性溶液中,以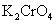 为指示剂,用
为指示剂,用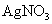 标准溶液进行滴定。
标准溶液进行滴定。
根据分步沉淀原理,由于AgCl的溶解度(AgCl——1.3×10—5 mol/L)比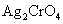 的溶解度(
的溶解度(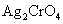 ——7.9×10—5 mol/L)小,因此溶液中首先析出AgCl沉淀。随着
——7.9×10—5 mol/L)小,因此溶液中首先析出AgCl沉淀。随着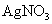 溶液的不断加入AgCl沉淀不断生成,溶液中的
溶液的不断加入AgCl沉淀不断生成,溶液中的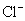 浓度越来越小,Ag+的浓度相应地愈来愈大,当AgCl定量沉淀后,过量1滴AgNO3溶液即与
浓度越来越小,Ag+的浓度相应地愈来愈大,当AgCl定量沉淀后,过量1滴AgNO3溶液即与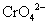 结合出现砖红色的
结合出现砖红色的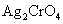 沉淀,借此可以指示滴定的终点。滴定过程中主要的反应式如下:
沉淀,借此可以指示滴定的终点。滴定过程中主要的反应式如下:


滴定必须在中性或弱碱性溶液中进行,最适宜pH范围为6.5~10.5。酸度过高,不产生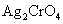 沉淀,过低,则形成
沉淀,过低,则形成 沉淀。如有铵盐存在,溶液的pH值范围最好控制在6.5~7.2之间。
沉淀。如有铵盐存在,溶液的pH值范围最好控制在6.5~7.2之间。
指示剂的用量对滴定有影响。根据溶度积原理,等当点时溶液中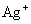 和
和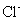 的浓度为:
的浓度为: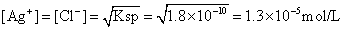
在等当点时,要求刚好析出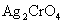 沉淀以指示终点,此时溶液中的
沉淀以指示终点,此时溶液中的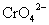 的浓度应为
的浓度应为 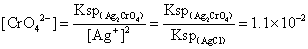
凡是能与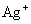 离子生成难溶化合物或络合物的阴离子都干扰测定,如
离子生成难溶化合物或络合物的阴离子都干扰测定,如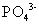 ,
,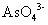 ,
,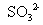 ,
,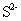 ,
,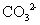 及
及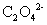 等离子,其中
等离子,其中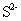 离子可成
离子可成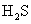 ,经加热煮沸而除去,
,经加热煮沸而除去,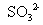 离子可经氧化成
离子可经氧化成 离子而不发生干扰。大量
离子而不发生干扰。大量 、
、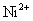 、
、 等有色离子将影响终点的观察。凡是能与
等有色离子将影响终点的观察。凡是能与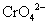 离子生成难溶化合物的阳离子也干扰测定,如
离子生成难溶化合物的阳离子也干扰测定,如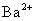 、
、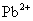 离子与
离子与 离子分别生成
离子分别生成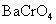 和
和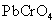 沉淀,但
沉淀,但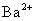 离子的干扰可借加入过量
离子的干扰可借加入过量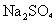 而消除。
而消除。
NaCl基准溶液浓度的计算:
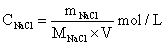
AgNO3标准溶液浓度的计算:
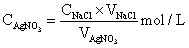
NaCl试样中氯含量的计算:
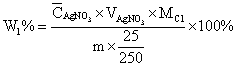
四、实验仪器和试剂
仪器:电子分析天平、酸式滴定管(1个)、容量瓶(100ml和250ml各一个)、锥形瓶250ml(3个)、移液管25ml(1个)、 试剂瓶 1000ml(1个)、 量筒(50ml)、烧杯100ml
试剂:NaCl基准试剂(分析纯)、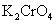 溶液(指示剂)、
溶液(指示剂)、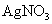 固体(分析纯)、 NaCl试样
固体(分析纯)、 NaCl试样
五、实验步骤
1、 AgNO3标准溶液的配制:
准确称取适量AgNO3溶解于100ml烧杯中,然后定量转移到棕色试剂瓶中用蒸馏水(不含Cl-)稀释到1000ml,置于暗处保存,以防光照分解。
2、 NaCl基准溶液的配制:
在称量瓶中用差减法准确称取NaCl基准试剂0.2~0.3g于100ml小烧杯中,用蒸馏水(不含Cl-)溶解,溶解完全后定量转移至100ml容量瓶中,再用蒸馏水稀释到刻度,摇匀。
3、 AgNO3标准溶液浓度的标定:
用25ml移液管准确移取25.00mlNaCl基准溶液于250ml锥形瓶中3份,均加入25~30mL水溶解完全后,加入1ml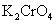 溶液,摇匀,然后用
溶液,摇匀,然后用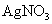 标准溶液滴定至溶液出现砖红色沉淀即为终点,记录消耗
标准溶液滴定至溶液出现砖红色沉淀即为终点,记录消耗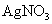 标准溶液的体积V,计算
标准溶液的体积V,计算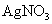 标准溶液的浓度。
标准溶液的浓度。
4、NaCl试液的制备及其氯含量的测定:
用分析天平称取NaCl试样0.7~0.9g,用蒸馏水完全溶解而后定量转移到250ml容量瓶中,再用蒸馏水稀释到刻度,摇匀。
用移液管准确移取25.00mLNaCl试样溶液于250ml锥形瓶中3份,均加入1ml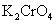 溶液,再用已标定好的
溶液,再用已标定好的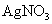 标准溶液滴定至溶液中出现砖红色沉淀,持续30s不消失即为滴定终点,记录消耗
标准溶液滴定至溶液中出现砖红色沉淀,持续30s不消失即为滴定终点,记录消耗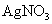 标准溶液体积V,计算NaCl试样中氯的含量。
标准溶液体积V,计算NaCl试样中氯的含量。
六、数据处理
1、NaCl基准溶液浓度的计算:
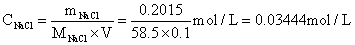
2、AgNO3标准溶液的标定:

第一次测定绝对偏差: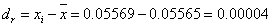
同理可得: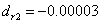
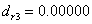
相对平均偏差: 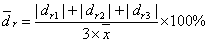
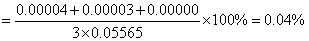
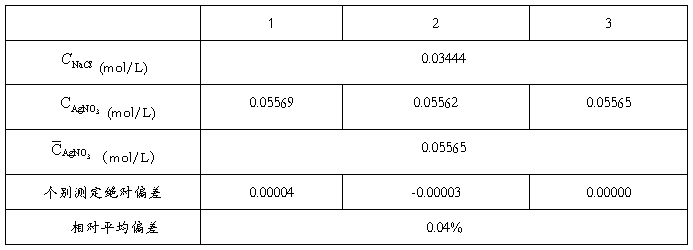
表1:AgNO3标准溶液的标定
2、NaCl试样中氯含量的测定:
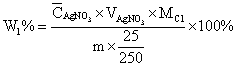
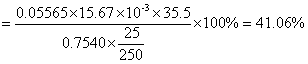
第一次测定Na2CO3绝对偏差:
同理可得: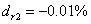
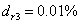
相对平均偏差: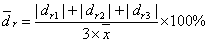
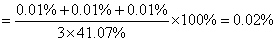
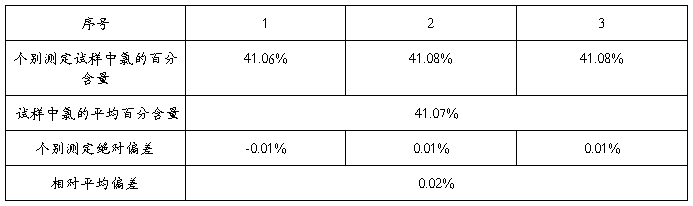
表2:NaCl试样中氯含量的测定
七、实验讨论与心得
1、配制好的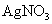 溶液要贮于棕色瓶中,并置于暗处,由于
溶液要贮于棕色瓶中,并置于暗处,由于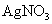 见光分解。
见光分解。
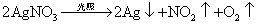 且Ag易氧化成氧化银影响测定结果。
且Ag易氧化成氧化银影响测定结果。
2、莫尔法不适用于以NaCl标准溶液直接滴定Ag+。因为在Ag+试液中加入指示剂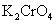 后,就会立即析出
后,就会立即析出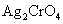 沉淀。用NaCl标准溶液滴定时,
沉淀。用NaCl标准溶液滴定时,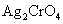 再转化成的AgCl的速度极慢,使终点推迟。
再转化成的AgCl的速度极慢,使终点推迟。
3、实验后一定先用蒸馏水冲洗滴定管,再用水洗,防止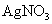 生成AgCl沉淀堵塞滴定管。
生成AgCl沉淀堵塞滴定管。
八、实验结论:
NaCl试样中氯的百分含量:41.07%
九、评语和成绩
成绩: 指导教师:
第二篇:莫尔法测定氯化物中氯含量







