
1.为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是
A.①③ 答案 B
( )
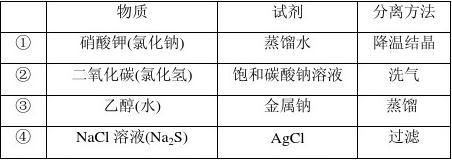
解析 硝酸钾的溶解度受温度的影响较大,而氯化钠的溶解度受温度的影响较小,故可以通过把混合物溶于蒸馏水后降温结晶的办法除去氯化钠,①正确;二氧化碳中混有的氯化氢应通过饱和碳酸氢钠溶液除去,②错误;金属钠与乙醇和水都能发生反应,故③错误;Na2S溶液和AgCl反应,生成Ag2S和NaCl,过滤除去Ag2S,④正确。
2.现有三组实验:①除去混在植物油中的水;②回收碘的CCl4溶液中的CCl4;③用食用酒精浸泡中草药提取其中的有效成分。分离以上各混合液的正确方法依次是
( )
A.分液、萃取、蒸馏 C.分液、蒸馏、萃取 答案 C
解析 植物油和水互不相溶,应采用分液法分离;碘易溶于CCl4,故用蒸馏法分离;用酒精浸取中草药中的有效成分,利用萃取原理。
3.下列溶液,只要用试管和胶头滴管,不用任何试剂就可以鉴别的是 A.KOH溶液和Al2(SO4)3溶液 B.稀H2SO4和NaHCO3溶液 C.CaCl2溶液和Na2CO3溶液 D.Ba(OH)2溶液和NaHSO4溶液
B.萃取、蒸馏、分液 D.蒸馏、萃取、分液
( )
答案 A
解析 将氢氧化钾溶液滴入硫酸铝溶液中,先有沉淀而后沉淀消失;若将硫酸铝溶液滴入氢氧化钾溶液中,先没有沉淀而后有沉淀生成。
4.提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为
( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸 B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸 C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸 D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
答案 D
解析 A项中加入过量碳酸钠,钠离子是新的杂质,不易除去;B项中加入过量硫酸钾,过量的硫酸根离子是新的杂质,不易除去;C项中加入过量硫酸钠,过量的钠离子和硫酸根离子都是新的杂质且不易除去;D项中碳酸钾可使硝酸钡生成碳酸钡沉淀,过滤除去沉淀后,过量碳酸钾跟适量硝酸生成硝酸钾、CO2气体和H2O,达到实验目的。
5.下列说法不正确的是 ( )
A.变色硅胶干燥剂含有CoCl2,干燥剂呈蓝色时,表示不具有吸水干燥功能
B.“硝基苯制备”实验中,将温度计插入水浴,但水银球不能与烧杯底部和烧杯壁接触
C.“中和滴定”实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗
净后,须经干燥或润洗后方可使用
D.除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗
气瓶
答案 A
解析 本题考查化学实验,意在考查学生对基本实验操作中注意事项的掌握。变色硅胶含有CoCl2,无水CoCl2为蓝色,因此干燥剂呈蓝色时表示其具有吸水干燥功能,A错;制备硝基苯时温度计插入水浴中控制温度,但水银球不能与烧杯内壁或底部接触,B对;中和滴定时,容量瓶和锥形瓶洗涤后无需干燥或用溶液润洗,但滴定管和移液管洗涤后必须干燥或用待装试剂润洗后方可使用,C对;CO2、SO2的混合气体通入酸性KMnO4溶液中,SO2被吸收,再通入浓硫酸中,水蒸气被吸收,最后可得到干燥的CO2,D对。
6.为除去MgCl2酸性溶液中的Fe3,可在加热搅拌的条件下加入一种试剂,过滤后,向滤液中加入适+
量盐酸,这种试剂是
A.NH3·H2O
C.Na2CO3
答案 D ( ) B.NaOH D.MgCO3
解析 加入NH3·H2O、NaOH及Na2CO3,最后溶液中混有新杂质;溶液呈酸性,加入MgCO3后,H被消耗,溶液碱性增强,Fe3转化为Fe(OH)3沉淀,杂质CO23可以用盐酸除去。 ++-
7.下列除去杂质的操作方法不正确的是 ( )
A.除去SiO2中的少量NH4Cl:在空气中充分灼烧
B.除去铜器表面的铜绿[Cu2(OH)2CO3]:用盐酸浸泡,再用清水冲洗
C.除去CO2中混有的SO2:用NaOH溶液洗气,再干燥
D.除去苯中溶解的Br2:加入足量NaOH溶液,充分振荡后,静置分液
答案 C
解析 在空气中充分灼烧,NH4Cl分解为氨气和氯化氢,可以得到纯净的SiO2,A正确;Cu2(OH)2CO3与盐酸反应,生成可溶性物质进入溶液,而铜不与HCl反应,可得到纯净的铜,B正确;CO2和SO2均为酸性氧化物,都能与NaOH溶液反应,C错;NaOH溶液能与Br2反应生成可溶于水的NaBr
和NaBrO,然后分液可以得到纯净的苯,D正确。
8.下列分离方法不合理的是 ( )
A.用分馏的方法,可从石油中得到汽油
B.用点燃的方法除去CO2中的少量CO杂质
C.只含有泥沙的粗盐,可通过溶解、过滤、结晶的方法提纯
D.加入适量铜粉除去Cu(NO3)2溶液中的AgNO3杂质
答案 B
解析 存在大量CO2,少量CO时无法点燃,B错;Cu可以置换出AgNO3溶液中的Ag,并生成Cu(NO3)2,D对。
9.以下实验装置一般不用于分离提纯物质的是 (
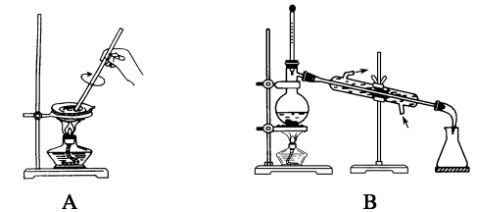
)
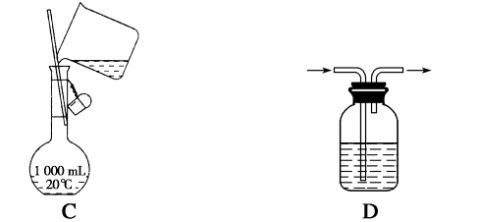
答案 C
解析 A为蒸发,分离溶液中的溶质;B为蒸馏,分离沸点不同的液体物质;C为配制一定物质的量浓度的溶液,不能用于分离物质;D为分离气体中的杂质。 10.如图所示是实验室蒸馏石油的实验装置,实验需要收集60~150 ℃和150~300 ℃的馏分。
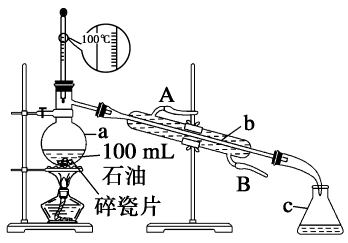
请回答下列问题:
(1)仪器a的规格和名称__________,仪器b、c的名称:b________,c________。
(2)实验所选温度计是错误的,正确的选择应该是_________________________。
(3)实验时在仪器a中加入了少量碎瓷片,其目的是________________________。
(4)实验时在仪器b中通入冷却水,请指明冷却水的流向
____________________________________________________________________。
答案 (1)250 mL蒸馏烧瓶 冷凝管 锥形瓶
(2)最大量程为350 ℃的温度计 (3)防止液体暴沸 (4)B口进,A口出
解析 本题考查化学实验基本操作和注意事项。
(1)实验所用的仪器a中盛放了100 mL石油,故其规格应该是250 mL,仪器a的名称是蒸馏烧瓶、b是冷凝管、c是锥形瓶。
(2)图中所用温度计的最大量程为100 ℃,而实验需要收集最高沸点为300 ℃的馏分,所以应该选用最大量程大于300 ℃的温度计,一般选用最大量程为350 ℃的温度计。
(3)在蒸馏烧瓶中加少量碎瓷片的目的是防止液体暴沸。
(4)冷凝管中的冷却水应该从B口进,A口出。
11.实验室里需要纯净的氯化钠溶液,但实验室中只有混有硫酸钠、碳酸氢铵的氯化钠。现有如下设
计方案:
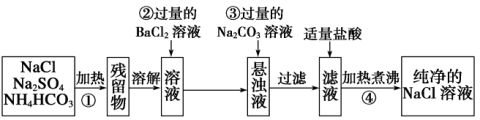
(1)操作①可选择的主要仪器是____________、__________仪器。
(2)操作②不用硝酸钡溶液的理由是____________________________________。
(3)操作④的目的是_________________________________________________。 答案 (1)坩埚(或试管、蒸发皿) 酒精灯
(2)选用Ba(NO3)2溶液会引入新的杂质离子NO3
(3)驱赶溶解在溶液中的CO2气体和HCl
解析 本题考查了学生对分离和提纯原理的理解和掌握情况,考查学生思维的严谨性和表达的准确性。
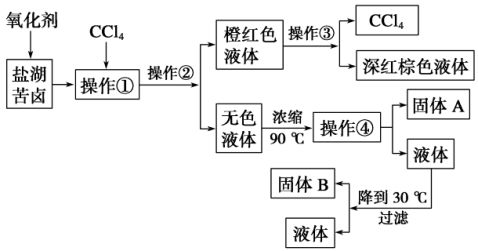
12.柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源。盐体矿床
以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含K、Mg2++-、Br、SO24、Cl等)来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
---
请根据以上流程,回答相关问题:
(1)操作①是________;操作②是________;操作③是________________________;
操作④所需要的玻璃仪器有_____________________________________________。
(2)参照如图所示溶解度曲线,欲得到较纯净的氯化钾晶体需用少量的________(填“热水”或“冷水”)洗涤固体____________________(填“A”或“B”)。
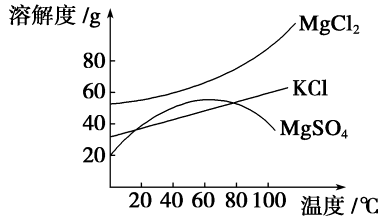
(3)在实验室常用减压的方法进行过滤,俗称抽滤,试猜想这种过滤方法的优点是_____________________________________________________________________。
答案 (1)萃取 分液 蒸馏 玻璃棒、漏斗、烧杯 (2)冷水 B (3)快速过滤
解析 最开始加的氧化剂将Br氧化生成Br2,由加入CCl4可知,是用萃取剂萃取
Br2,所以操作①是萃取;将CCl4层和水层分开的过程叫做分液;利用蒸馏(操作③)
从溴的CCl4溶液中分离得到CCl4和液溴。由溶解度图像知,将得到的溶液进行蒸发浓缩至90 ℃后进行结晶,再将固液不相溶的物质进行分离的操作叫过滤,此时所用的玻璃仪器有玻璃棒、烧杯、漏斗;在90 ℃时得到的固体A为MgSO4,而30 ℃时得到的固体B为KCl,所以应用冷水洗涤固体B,才可以得到较纯净的氯化钾。在减压条件下进行过滤,可使过滤的速度加快。
13.为了除去某氯化钠固体样品中含有的少量硫酸钠、氯化钙杂质,设计了以下实验流程:
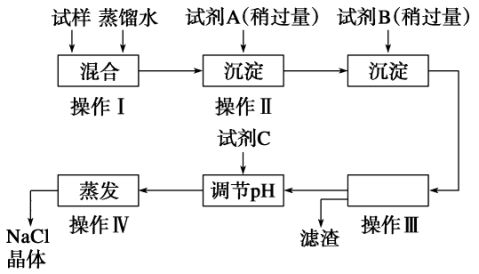
-
请回答:
(1)操作Ⅲ的名称是________。 (2)试剂A是________,试剂B是________,A和B都要稍过量的原因分别是____________________________________________________________________。
(3)试剂C是__________,加C的目的是________,为什么要调节滤液的pH?____________________________________________________________________
____________________________________________________________________。
(4)操作Ⅲ得到的滤渣的成分是________。
(5)最后得到的氯化钠与试样中的氯化钠质量是否相等?
答案 (1)过滤
(2)BaCl2溶液 Na2CO3溶液 A除去Na2SO4杂质,B除去CaCl2杂质和过量的A
(3)稀盐酸 除去CO23 节省试剂,避免过量盐酸在蒸发时挥发出HCl,污染环境 -
(4)BaSO4、CaCO3、BaCO3
(5)不相等
第二篇:新人教版化学选修6高中《物质的分离和提纯》word教案
山东选修6 实验化学第二单元物质的获取课题一 物质的分离和提纯
茶叶中某些元素鉴定的探究
一、 探究问题的提出
茶有健身、治疾之药物疗效,饮茶在给人精神愉悦的同时,还补充了人体所需的水分、氨基酸、维生素、茶多酚、生物碱、类黄酮、芳香物质等多种有益的有机物,并且还提供了人体组织正常运转所不可缺少的矿质元素。但饮茶为什么会有许多好处呢?这对一般人来说,是知其然而不知其所以然。随着科学的发展,到了19世纪初,茶业的成分才逐渐明确起来。经过现代科学的分离和鉴定,茶叶中含有机化学成分达四百五十多种,无机矿物元素达四十多种。茶叶中的有机化学成分和无机矿物元素含有许多营养成分和药效成分。有机化学成分主要包括:茶多酚类、植物碱、蛋白质、氨基酸、维生素、果胶素、有机酸、脂多糖、糖类、酶类、色素等;而无机矿物元素主要有:钾、钙、镁、钴、铁、锰、铝、钠、锌、铜、氮、磷、氟、碘、硒等。作为一名中学生,茶叶是生活中常见的物质,检测茶叶的主要元素,既可锻炼学生的探究精神,培养学生的创新精神,又可以提高学生的动手能力。所以,本方案应用已学和资料提供的检验离子的反应,检验茶叶中的某些主要元素。
二、问题解决设想
这主要包括几个方面。首先,通过查找资料了解茶叶中大概含有哪几种元素。其次,运用已学和资料提供的检验离子的反应设计出检验主要元素的方向和路线;然后,通过路线、查找资料得出可行方案和根据方案设计实验检测茶叶的主要元素;最后,通过实验结果分析茶叶中含有的元素和对此次实验的总结。
三、试验设计方案
(一)、实验原理
溶液中的阴、阳离子大多能发生特征的化学反应,根据反应现象,可以推知其是否存在,达到定性地检测物质中某种元素的目的。在表1中,归纳了中学一些常见的离子检验方法。
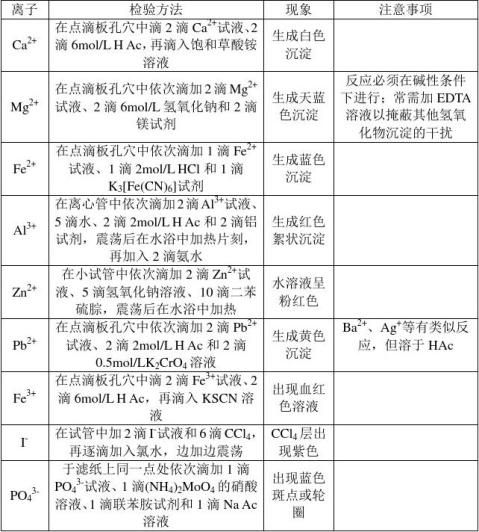
(二)、实验探究过程
1、 实验用品
药品:6mol/L HCl、浓氨水、草酸铵溶液、铝试剂、KSCN溶液、茶叶。 仪器:托盘天平、酒精灯、泥三角、蒸发皿、玻璃棒、三脚架、研钵、110mL
烧杯、漏斗、滤纸、pH试纸
2、 实验装置
3、实验方案设计
-1茶叶10克悬液浊滤液
煮沸30分白色沉淀Ca2+ 滤液 沉淀
-1盐酸 Al3+ 血红色溶液Fe溶液


4、实验步骤
(1)取10g茶叶于蒸发皿中用酒精中灼烧灰化,所得的灰分移至研钵中研细。
(2)在烧杯中加入两药匙研细的灰分,再加入30mL 6mol/L的HCl,搅拌后, 浸泡15min,过滤。
(3)用浓氨水调节滤液的pH至5左右,将得到的悬浊液煮沸30min后过滤。
(4)向实骤(3)得到的滤液中滴加草酸铵溶液,观察现象。
(5)实验步骤(3)得到的沉淀用6mol/L的HCl溶解。
(6)取两只试管,分别加入适量步骤(5)所得到的溶液,向其中一只试管加
入铝试剂,另一只试管加入KSCN溶液,观察现象。
四、实验过程记录
(一)实验现象记录
表2 实验现象记录
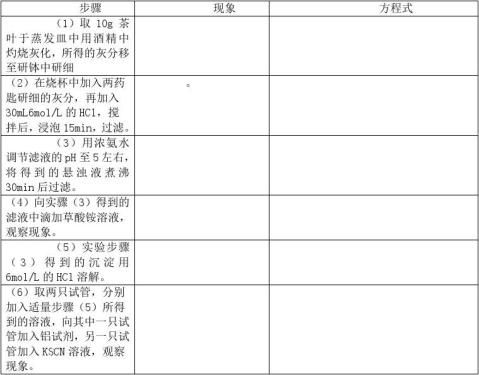
(二)实验结论
五、相关问题探讨
1、茶叶中的Ca2+、Al3+、Fe3+在茶叶的灼烧后,可能以什么形式存在于茶叶灰中?
-12、为什么要用6mol·L的浓盐酸来溶解茶叶灰呢?
3、为什么用浓氨水控制溶液的PH值,而不用氢氧化钠控制?
4、怎样鉴定溶液中的Al3+、Ca2+、Fe3+,说出使用的试剂及现象。
