

实验六堵水剂的制备与性质
一、实验目的
1. 学会几种堵水剂的制备方法。
2. 掌握几种堵水剂的形成机理及其使用性质。
二、实验原理
堵水剂是指从油、水井注入地层,能减少地层产出水的物质。从油井注入地层的堵水剂称油井堵水剂(或简称堵水剂),从水井注入地层的堵水剂称为调剖剂。
常用的堵水剂有冻胶型堵水剂、凝胶型堵水剂、沉淀型堵水剂和分散体型堵水剂,这些堵水剂的形成机理和使用性质各不相同。
1. 冻胶型堵水剂
冻胶(如锆冻胶)是由高分子(如HPAM)溶液转变而来,交联剂(如锆的多核羟桥络离子)可以使高分子间发生交联,形成网络结构,将液体(如水)包在其中,从而使高分子溶液失去流动性,即转变为冻胶。
锆冻胶是油田常用的冻胶型堵水剂。锆冻胶是由锆的多核羟桥络离子与HPAM中的羧基发生交联反应而形成的。体系的pH值可影响多核羟桥络离子的形成及HPAM分子中羧基的量,因此,pH值可影响锆冻胶的成冻时间和冻胶强度。
2. 凝胶型堵水剂
凝胶是由溶胶转变而来。当溶胶由于种种原因(如电解质加入引起溶胶粒子部分失去稳定性而产生有限度聚结)形成网络结构,将液体包在其中,从而使整个体系失去流动性时,即转变为凝胶。油田堵水中常用的是硅酸凝胶。硅酸凝胶由硅酸溶胶转化而来,硅酸溶胶由水玻璃(又名硅酸钠,分子式Na2O?mSO2)与活化剂反应生成。活化剂是指可使水玻璃先变成溶胶而随后又变成凝胶的物质。盐酸是常用的活化剂,它与水玻璃的反应如下:
Na2O?mSiO2 + 2HCl → H2O?mSiO2 + 2NaCl
由于制备方法不同,可得两种硅酸溶胶,即酸性硅酸溶胶和碱性硅酸溶胶。这两种硅酸溶胶都可在一定的条件(如温度、pH值和硅酸含量)下,在一定时间内胶凝。
评价硅酸凝胶堵水剂常用两个指标,即胶凝时间和凝胶强度。胶凝时间是指硅酸体系自生成至失去流动性的时间。凝胶强度是指凝胶单位表面积上所能承受的压力。
3. 沉淀型堵水剂
沉淀型堵水剂由两种可反应产生沉淀的物质组成。水玻璃-氯化钙是油田最常用的沉淀
型Na2O?mSiO2 + CaCl2 → CaO2?mSiO2 + 2NaCl
4. 悬浮体型堵水剂
悬浮体是指溶解度极小但颗粒直径较大(大于10-5cm)的固体颗粒分散在溶液中所形成的粗分散体系。分散体系中的固体颗粒可以在多孔介质的喉道处产生堵塞作用。油田中常用的分散体型堵水剂是粘土悬浮体型堵水剂。粘土悬浮体中的粘土颗粒可用聚合物(如HPAM)絮凝产生颗粒更大、堵塞作用更好的絮凝体堵水剂。絮凝是聚合物(HPAM)在粘土颗粒间通过桥接吸附形成。
三、仪器与药品
1. 仪器
100ml烧杯,10ml具塞刻度试管,5ml、25ml量筒,玻璃棒,广泛pH试纸。
2. 药品
聚丙烯酰胺,氧氯化锆,水玻璃,氯化钙,盐酸。
四、实验步骤
1. 锆冻胶堵水剂的制备与性质
取3个100ml烧杯,用量筒各加入质量分数为5×10-3的聚丙烯酰胺水溶液20ml,其中一个烧杯中滴加6滴质量分数为1×10-2的盐酸,另一烧杯中滴加7滴质量分数为1×10-2的NaOH,搅拌均匀,用广泛pH试纸测定三个烧杯中聚丙烯酰胺溶液的pH值,然后向三份聚丙烯酰胺溶液中分别加入2ml质量分数为5×10-3的ZrOCl2溶液(注意:边用玻璃棒搅拌,边缓慢加入),观察并记录冻胶形成的现象(注意记录成冻时间,由于都是瞬间成冻,均记为0)和冻胶的强度(用玻璃棒挑起程度衡量)。
2. 硅酸凝胶堵水剂的制备与性质
取三支10ml具塞刻度试管,加入质量分数为0.1的水玻璃5ml,用滴管向三支试管中依次加入质量分数为0.1的盐酸16滴、14滴、12滴并摇匀,观察凝胶的生成并记录胶凝时间,待三支试管中全部胶凝后用玻璃棒插入凝胶,从玻璃棒插入的难易排出三种凝胶强度的顺序。
3. 水玻璃—氯化钙沉淀型堵水剂的制备与性质
取一支10ml的具塞刻度试管,加入质量分数为0.1的水玻璃5ml,然后用滴管逐滴加入质量分数为0.1的氯化钙溶液,摇匀,观察硅酸钙沉淀的生成情况。
五、结果处理
用表格形式表达实验现象与数据,并解释实验现象。
表一 实验现象与数据
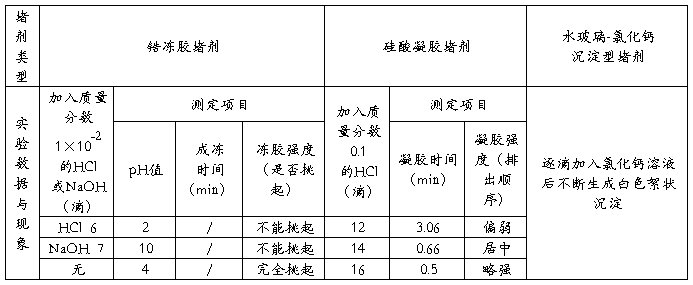
解释实验现象:
1、对锆冻胶堵剂实验现象的解释
锆冻胶是由锆的多核羟桥络离子与 HPAM 中的羧基发生交联反应而形成的。体系的 pH值可影响多核羟桥络离子的形成及 HPAM 分子中羧基的量,因此,pH值可影响锆冻胶的成冻时间和冻胶强度。pH过高或过低都不能形成足够强度的冻胶。
2、对硅酸凝胶堵剂实验现象的解释
盐酸浓度越高,硅酸凝胶堵剂的成胶时间越短,凝胶强度越高,因为硅酸凝胶由水玻璃与活化剂HCl反应生成的硅酸溶胶转化而来,体系先在一定的pH值、温度、硅酸含量下先形成硅酸溶胶,然后在一定时间内形成硅酸凝胶,因此,其形成与活化剂的浓度有关,活化剂的浓度又进而影响了成胶时间与成胶强度。
3、水玻璃-氯化钙沉淀型堵剂实验的解释
沉淀型堵水剂由两种可反应产生沉淀的物质组成。水玻璃-氯化钙是油田最常用的沉淀型堵水剂,它通过如下反应产生沉淀:
Na2O?mSiO2 + CaCl2→ CaO2?mSiO2 + 2NaCl
滴加氯化钙后不断生成钙盐沉淀即白色絮状沉淀。
六、思考题
1. 解释 pH值对锆冻胶生成的影响。
答:锆冻胶是由锆的多核羟桥络离子与 HPAM 中的羧基发生交联反应而形成的。体系的 pH值可影响多核羟桥络离子的形成及 HPAM 分子中羧基的量,因此,pH值可影响锆冻胶的成冻时间和冻胶强度。pH过高或过低都不能形成足够强度的冻胶。
2.本实验中制备的硅酸凝胶是碱性硅酸凝胶还是酸性硅酸凝胶,解释原因。
答:本实验制备的硅酸凝胶是碱性硅酸凝胶。
酸性硅酸凝胶是将水玻璃加到盐酸中制得的,此时H+过剩,它的胶粒表面带正电;反之,碱性硅酸凝胶是将盐酸加到水玻璃中制得的,因反应在SiO32-过剩的情况下制得,它的胶粒表面带负电。
由于本实验中的堵水剂是将盐酸加入到水玻璃中制得的,所以属于碱性硅酸凝胶。
七、实验总结
第二篇:氧气的制备与性质实验报告
氧气的制备与性质
一、实验原理
1、高锰酸钾法:
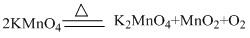 ↑
↑
2、过氧化氢法:
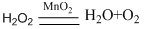 ↑
↑
3、氧气的性质:
在通常状况下,O2为无色无味的气体。在标准状况下,O2的密度比空气的平均密度大。不易溶于水。
氧气的化学性质比较活泼。它不仅可以助燃,而且在点燃或高温条件下可以和大多数金属、非金属发生反应,放出大量热。
二、实验操作过程与实验现象
1、氧气的制取与收集
(1)、过氧化氢分解制备法
1、安装实验装置如下图
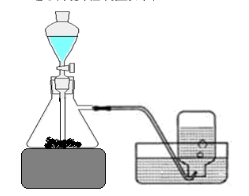
2、实验步骤:
a、检查装置气密性
b、在蒸馏烧瓶中装入0.5克MnO2,将与烧瓶口匹配的分液漏斗塞住烧瓶口,分液漏斗中加入H2O2(以体积比水:过氧化氢=1:3稀释过的过氧化氢溶液);
c、将集气瓶装满水并倒扣于水槽中,打开分液漏斗活塞,等到导管口有均匀连续气泡逸出,将导管伸入集气瓶内(此时集气瓶仍为倒置),观察到有连续的气泡从瓶口冒出,移开导管,用玻璃片毛面迅速封口,从水槽中取出集气瓶既可。收集四瓶气体。
※实验现象:
1打开分液漏斗活塞后,可以观察有大量气泡冒出.
2同时观察到烧瓶中出现烟雾.
(2)高锰酸钾加热分解制备法:
1、安装实验装置如下图

2、实验步骤:
a、检查装置气密性
b、称取3克高锰酸钾加入硬质试管中,管口塞一块蓬松的脱脂棉,塞紧单孔塞
c、点燃酒精灯后,先预热试管,然后集中在药品处加热
d、用排水法收集
※实验现象:
1高锰酸钾在加热时有强烈的迸裂
 2并伴有少量烟产生
2并伴有少量烟产生
2、氧气的性质
 (1)、硫在O2中的燃烧:
(1)、硫在O2中的燃烧:
取一洁净的燃烧匙,放入少量硫磺粉,在酒精灯上加热至燃烧,然后将燃着的硫匙由上往下缓缓伸进集有O2的集气瓶中。
※实验现象:
在酒精灯上加热会发出微弱的淡蓝色火焰,而在氧气瓶中火焰颜色为明亮的蓝色,并有刺激性气味的气体产生。
(2)、碳在O2中的燃烧:
用坩埚钳夹取一小段木炭,在酒精灯上烧至红热,再缓慢伸进盛满氧气的集气瓶中,观察现象。给此集气瓶中倒入少量澄清石灰水,振荡。
※实验现象:
木炭在O2中燃烧剧烈,并发出白色亮光,并伴有少量烟产生。加入的澄清石灰水变浑浊。
(3)、铁在O2中的燃烧:
取一小段细铁丝,将其绕在火柴上,用坩埚钳夹住两头的铁丝,点燃火柴,烧至火焰将尽时,伸入瓶底留有少许水的集气瓶中。
※实验现象:
在空气中只看到火柴燃烧,铁丝被烧红。铁丝在氧气中燃烧,火星四射,并生成黑色的熔融物。
(4)、蜡烛在O2中的燃烧:
取一小截蜡烛,点燃后伸入集气瓶中,观察现象,给此集气瓶中倒入少量澄清石灰水,振荡。
※实验现象:
蜡烛在酒精灯上只在一端燃烧,而在O2中会全部燃烧,火焰更加亮白,石灰水变浑浊。
三、实验应注意的事项
1、在加热高锰酸钾时,颗粒容易迸裂而从导气管冲进水槽,或致导气管堵塞,因此要在试管口放一团脱脂棉;而且加热前要先预热,然后集中加热。
2、使用过氧化氢时,要注意先用蒸馏水稀释,控制滴加速度;将分液漏斗中的过氧化氢完全加入到蒸馏烧瓶中后,需要将活塞关闭,以免气体从漏斗排出,影响实验的进行。
3、排水法收集气体完后,要先把导气管从水槽中取出再撤装置,防止倒吸。
4、燃烧物定要放于集气瓶中央,切勿靠近瓶壁,以防集气瓶炸裂
5、在硫的燃烧试验中,为避免污染空气,将燃烧匙取出后及时淬入盛有冷水的大烧杯中;
6、在铁丝的燃烧试验中,集气瓶底一定要铺细砂或者留有部分水,高温的熔融物会使集气瓶底炸裂。
四、相关文献与重点文献综述
1、铁丝在氧气中燃烧实验的探究
(1)、铁丝为什么要绕在一根火柴上?
点燃火柴后,放出热量,使铁丝达到一定温度才能在氧气中燃烧,即火柴起预热铁丝的作用;而且螺旋状是为了增大铁丝与氧气的接触面积。同理,我们可以只让铁丝绕成螺旋状,蘸入酒精中,也可起到此作用。
(2)、铁丝伸人集气瓶时,为什么要从瓶的正中央慢慢地往下移?
因铁丝燃烧时放出大量的热,若不在瓶的正中央伸人,会使集气瓶局部过热而炸裂,如果快速伸人,则会将瓶里中部和上部的氧气排出,铁丝就不能顺利燃烧
(3)、集气瓶里为什么要预先盛少量水或铺一薄层细沙?
防止实验时溅落的高温熔化物炸裂瓶底。
(4)“火星四射”为什么不能说成“耀眼的火焰”?
火焰是由气体或蒸气燃烧而形成的现象,而铁丝是固体,且熔点极高,不易气化,因而看不到火焰
2、氧气的化学性质“很活泼”应该为“比较活泼”:
人教社20##年3月第一版初中《化学(全一册)》,第一章第二节中对氧气化学性质的叙述为:“通过以上实验可以看出,氧气是一种化学性质比较活泼的气体”;但又在第四节这样叙述:“证明氧气性质的几个实验,不仅说明了氧气的化学性质很活泼……”表示物质化学性质时用很活泼、比较活泼、不活泼、很不活泼是有一定区别的。
通过14页习题2.(3)可知,,第四节的表述应改为:“证明氧气性质的几个实验,不仅说明了氧气的化学性质比较活泼……”氧气的化学性质“很活泼”应改为“比较活泼”。
3、本次试验的目的
(1)、首先,对比三种制取氧气方法,了解其优缺点,由于氯酸钾制取氧气反应装置复杂,操作不当容易引起试管炸裂,所以本次实验不用此方法。
(2)、教材所提供的三种制取氧气的方法其教学侧重点是不一样的: “用双氧水和二氧化锰混合制取氧气” 侧重于催化剂概念的教学; 用“氯酸钾和二氧化锰混合共热制取氧气” 侧重于基本实验方法和技能的教学; “单独加热高锰
酸钾制取氧气” 侧重于为中学化学的后续学习打下基础。
(3)、即将作为教师的我们在演示实验中不仅要引导学生从物质颜色、状态的变化、是否有气体等方面进行观察实验,还要引导学生将所观察的实验现象进行总结提升,达到以实验促进知识掌握的目的。
五、参考文献
1、胡大勇.氧气的化学性质“很活泼”应该为“比较活泼”〔J〕.实验教学与仪器,2003,2:42
2. 耿庆梅 刘金瑞. 新课程下的化学实验教学〔J〕.现代教育科学·中学教师,2001.3:25
3. 徐良水 曹向华.氧气性质实验探究〔J〕.中学生数理化,2003,25:59
