硫酸四氨合铜(Ⅱ)的制备
【实验目的】
1、了解配合物的制备,结晶,提纯的方法,学习硫酸四氨合铜(Ⅱ)的制备原理及制备方法。
2、进一步练习溶解、抽滤、洗涤、干燥等基本操作。
【基本操作】
溶解、抽滤、洗涤、干燥等基本操作。
【实验原理】
一水合硫酸四氨合铜(Ⅱ)[Cu(NH3)4]SO4·H2O为蓝色正交晶体,在工业上用途广泛,常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,也用于制备某些含铜的化合物。本实验通过将过量氨水加入硫酸铜溶液中反应得硫酸四氨合铜。反应式为:
CuSO4 + 4NH3 + H2O ====[Cu(NH3)4]SO4·H2O
由于硫酸四氨合铜在加热时易失氨,所以其晶体的制备不宜选用蒸发浓缩等常规的方法。硫酸四氨合铜溶于水但不溶于乙醇,因此在硫酸四氨合铜溶液中加入乙醇,即可析出深蓝色的[Cu(NH3)4]SO4·H2O晶体。由于该配合物不稳定,常温下,一水合硫酸四氨合铜(Ⅱ)易于与空气中的二氧化碳,水反应生成铜的碱式盐,使晶体变成绿色粉末。在高温下分解成硫酸铵,氧化铜和水,故不宜高温干燥。
【实验用品】
1、仪器:托盘天平、烧杯、量筒、玻璃棒、布氏漏斗、抽滤瓶、真空泵、表面皿
2、药品:五水硫酸铜(AR)、氨水(AR)、无水乙醇、乙醇:浓氨水(1: 2)、乙醇:乙醚(1: 1)、2mol·L-1H2SO4、2mol·L-1NaOH
3、材料:滤纸
【实验步骤】
1、制备
用托盘天平称取5.0g五水硫酸铜,放入洁净的100ml烧杯中,加入10ml去离子水,搅拌至完全溶解,加入10mL 浓氨水,搅拌混合均匀(此时溶液呈深蓝色,较为不透光。若溶液中有沉淀,抽滤使溶液中不含不溶物)。沿烧杯壁慢慢滴加20mL无水乙醇,然后盖上表面皿静置15min。待晶体完全析出后,减压过滤,晶体用乙醇:浓氨水(1: 2)的混合液洗涤,再用乙醇与乙醚的混合液淋洗,抽滤至干。然后将其在60 ℃ 左右烘干,称量。
2、铜氨络离子的性质
取产品0.5g,加5mL蒸馏水溶解备用。
(1) 取少许产品溶液,滴加2mol·L-1硫酸溶液,观察现象;
(2) 取少许产品溶液,滴加2mol·L-1氢氧化钠溶液,观察现象;
(3) 取少许产品溶液,加热至沸,观察现象;继续加热观察现象;
(4) 取少许产品溶液,逐渐滴加无水乙醇,观察现象。
(5) 在离心试管中逐渐滴加0.1mol·L-1Na2S溶液,观察现象。
【实验结果记录】
产品 g,产品外观 ;收率%=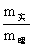 ×100%=
×100%=
表1铜氨络离子的性质检验
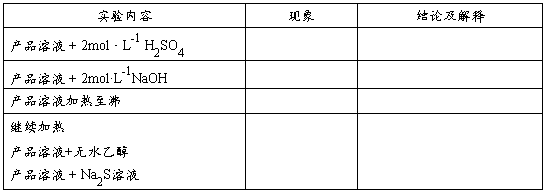
【实验习题】
1、为什么使用乙醇:浓氨水(1: 2)的混合液洗涤晶体而不是蒸馏水?
【实验指导】
硫酸铜溶解较为缓慢,为加快溶解速度,应研细固体硫酸铜,同时可微热促使硫酸铜溶解。
实验 硫酸铝钾的制备
【实验目的】
1、了解由金属铝制备硫酸铝钾的原理及过程;
2、学习复盐的制备及性质;
3、认识铝及氢氧化铝的两性性质;
4、巩固蒸发、结晶、沉淀的转移、抽滤、洗涤、干燥等无机物制备的基本操作。
【基本操作】
1、溶解、蒸发、冷却、结晶、沉淀的转移等基本操作。
2、抽滤、洗涤、干燥等基本操作。
【实验原理】
硫酸铝同碱金属的硫酸盐(K2SO4)生成硫酸铝钾复盐KAl(SO4)2(俗称明矾)。它是一种无色晶体,易溶于水并水解生成Al(OH)3胶状沉淀,具有很强的吸附性能,是工业上重要的铝盐,可作为净水剂、媒染剂、造纸填充剂等。
本实验利用金属铝可溶于NaOH 溶液中,生成可溶性的四羟基铝酸钠Na[Al(OH)4]:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑
金属铝中其它杂质则不溶,再用稀硫酸调节此溶液的pH值为8~9,即有Al(OH)3沉淀产生,分离后在沉淀中加入H2SO4致使Al(OH)3沉淀转化为Al2(SO4)3:
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
在Al2(SO4)3溶液中加入等量的K2SO4,在水溶液中结合生成溶解度较小的复盐,当冷却溶液时,硫酸铝钾以大块晶体结晶析出,即制得KAl(SO4)2·12H2O:
Al2(SO4)3 + K2SO4 + 12H2O → 2KAl(SO4)2·12H2O
【实验用品】
1、仪器:托盘天平、烧杯、量筒、布氏漏斗、抽滤瓶、真空泵、蒸发皿、表面皿、酒精灯、石棉网、铁三角
2、药品:铝屑、K2SO4 (s)、3mol·L-1H2SO4、1+1H2SO4、NaOH (s)
3、材料:滤纸、广泛pH试纸
【实验步骤】
1、Na[Al(OH)4]的制备
称取2.3g固体NaOH,置于250mL烧杯中,加入30mL蒸馏水溶解。称取1g铝屑,分批放入NaOH溶液中(反应激烈,为防止溅出。应在通风橱中进行),搅拌至不再有气泡产生,说明反应完毕。补充少量蒸馏水使溶液体积约为40mL,反应后,趁热抽滤。
2、 Al(OH)3的生成
将滤液转入250 mL烧杯中,加热至沸,在不断搅拌下,逐滴滴加3mol·L-1H2SO4,使溶液的pH值为8~9,继续搅拌煮沸数分钟,抽滤,用沸水洗涤沉淀,直至洗出液的pH值降至7左右,抽干。
3、Al2(SO4)3的制备
将制得的Al(OH)3沉淀转入烧杯中,加入约16mL(1+1)H2SO4,并不断搅拌,小火加热使其溶解,得Al2(SO4)3溶液。
4、复盐的制备
将Al2(SO4)3溶液与3.3g K2SO4 固体配成的饱和溶液相混合。搅拌均匀,充分冷却后,减压抽滤,尽量抽干,称重。
【实验结果记录】
产品 g,产品外观 ;
产率%=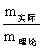 ×100%=
×100%=
注:m理论以铝屑量为基准进行计算
【实验习题】
1、第一步反应中是碱过量还是铝屑过量?为什么?
2、铝屑中的杂质是如何除去的?
3、如何制得明矾大晶体?
附录:硫酸钾在水中的溶解度
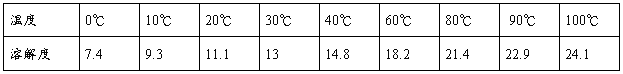
第二篇:硫酸四氨合铜(Ⅱ)的制备及组分分析
硫酸四氨合铜(Ⅱ)的制备及组分分析
一、实验目的
1.了解硫酸四氨合铜(Ⅱ)的制备步骤并掌握其组成的测定方法;
2.掌握蒸馏法测定氨的技术
二、实验原理
硫酸四氨合铜([Cu(NH3)4]SO4)常用作杀虫剂、媒染剂在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。硫酸四氨合铜属中度稳定的绛蓝色晶体,常温下在空气中易与水和二氧化碳反应,生成铜的碱式盐,使晶体变成绿色的粉末
1. 制备
CuSO4+4NH3+H2O=([Cu(NH3)4]SO4)·H2O
由于硫酸四氨合铜在加热时易失氨,所以其晶体的制备不宜选用蒸发浓缩等常规的方法。
析出晶体主要有两种方法:
一种是向硫酸铜溶液中通入过量氨气,并加入一定量硫酸钠晶体,使硫酸四氨合铜晶体析出。
另一种方法,是根据硫酸四氨合铜在乙醇中的溶解度远小于在水中的溶解度的性质。向硫酸铜溶液中加入浓氨水之后,再加入浓乙醇溶液使晶体析出。
2. 组分分析
1)NH3 含量的测定:
Cu(NH3)4SO4+NaOH=CuO↓+4NH3↑+Na2SO4+H2O
NH3+HCl(过量)=NH4Cl
HCl(剩余量)+NaOH=NaCl + H2O
2)SO42-含量的测定:
SO42- + Ba2+ =Ba SO4↓
三、实验药品及仪器
CuSO4·5H2O晶体、浓氨水、乙醇95%、0.5mol/L HCl、0.5mol/L NaOH溶液
烧杯、酒精灯、洗瓶、药匙、抽滤漏斗
四、实验步骤
1. 制备
(一)硫酸四铵合铜的制备
取10g CuSO4.5H2O溶于14mL水中,加入20mL浓氨水, 沿烧杯壁慢慢滴加35mL95%的乙醇,然后盖上表面皿。静置析出晶体后,减压过滤,晶体用1:2的乙醇与浓氨水的混合液洗涤,再用乙醇与乙醚的混合液淋洗,然后将其在60 ℃左右烘干,称重,保存待用。
2. 组分分析
NH3的测定(装置)
称取0.25-0.30g 样品,放入250mL锥形瓶中,加80mL水溶解,再加入10 mL10%的NaOH溶液。在另一锥形瓶中,准确加入30-35mL标准HCl 溶(0.5mol?L-1),放入冰浴中冷却。
 按图 装配好仪器,从漏斗中加入3-5 mL10% NaOH溶液于小试管中,漏斗下端插入液面下2-3cm。加热样品,先用大火加热,当溶液接近沸腾时改用小火,保持微沸状态,蒸馏1h左右。即可将氨全部蒸出。蒸馏完毕后,取出插入HCl 溶液中的导管,用蒸馏水冲洗导管内外,洗涤液收集在氨吸收瓶中,从冰浴中取出吸收瓶,加 2 滴0.1% 的甲基红溶液,用标准NaOH溶液(0.5mol?L-1)滴定剩余的溶液
按图 装配好仪器,从漏斗中加入3-5 mL10% NaOH溶液于小试管中,漏斗下端插入液面下2-3cm。加热样品,先用大火加热,当溶液接近沸腾时改用小火,保持微沸状态,蒸馏1h左右。即可将氨全部蒸出。蒸馏完毕后,取出插入HCl 溶液中的导管,用蒸馏水冲洗导管内外,洗涤液收集在氨吸收瓶中,从冰浴中取出吸收瓶,加 2 滴0.1% 的甲基红溶液,用标准NaOH溶液(0.5mol?L-1)滴定剩余的溶液
0.5mol/L HCl溶液的标定
0.5mol/L NaOH溶液的标定
注意:基准物质的质量
计算NH3含量
 NH3%=
NH3%=
式中: C1V1 :标准HCl 溶液的浓度和体积;
C2V2 :标准NaOH 溶液的浓度和体积
mS :样品质量:
17.04 :NH3 的摩尔质量
称取试样约0.65g(含硫量约90mg),置于400ml烧杯中,加25ml蒸馏水使其溶解,稀释至200ml
SO42-的测定
①沉淀的制备
在上述溶液中加稀HCl(6mol/L)2ml,盖上表面皿,置于电炉石棉网上,加热至近沸。取BaCl2(0.1mol/L)溶液30-35ml于小烧杯中,加热至近沸,然后用滴管将热BaCl2溶液逐滴加入样品溶液中,同时不断搅拌溶液。当BaCl2溶液即将加完时,静置,于BaSO4上清液中加入1-2滴BaCl2溶液,观察是否有白色浑浊出现,用以检验沉淀是否已完全。盖上表面皿,置于电炉(或水浴)上,在搅拌下继续加热,陈化约半小时,然后冷却至室温
②沉淀的过滤和洗涤
将上清液用倾注法倒入漏斗中的滤纸上,用一洁净烧杯收集滤液(检查有无沉淀穿滤现象。若有,应重新换滤纸)。用少量冷蒸馏水洗涤沉淀3-4次(每次加入水10-15ml),然后将沉淀小心地转移至滤纸上。用洗瓶吹洗烧杯内壁,洗涤液并入漏斗中,并用撕下的滤纸角擦拭玻璃棒和烧杯内壁,将滤纸角放入漏斗中,再用少量蒸馏水洗涤滤纸上的沉淀(约10次),至滤液不显Cl-离子反应为止(用AgNO3(0.1mol/L)溶液检查)。
沉淀的过滤:
③沉淀的干燥和灼烧
取下滤纸,将沉淀包好,置于已恒重的坩埚中,先用小火烘干炭化,再用大火灼烧至滤纸灰化。然后将坩埚转入马弗炉中,在800-850℃灼烧约30min。取出坩埚,待红热退去,置于干燥器中,冷却30min后称量。再重复灼烧20min,冷却,取出,称量,直至恒重。
根据BaSO4重量计算试样中硫酸的百分含量。
先称好坩埚的质量,并认准,做好标记。
v 注意事项
v 组分含量的理论值:Cu2+% 25.85,NH3% 27.73,SO42-% 39.08,H2O% 7.33。
v 实验前,应预习和本实验有关的基本操作相关内容。
v 溶液加热近沸,但不应煮沸,防止溶液溅失。
v BaSO4沉淀的灼烧温度应控制在800-850℃,否则,BaSO4将与碳作用而被还原。
v 检查滤液中的Cl-时,用小表面皿收集10-15滴滤液,加2滴AgNO3溶液,观察是否出现浑浊,若有浑浊则需继续洗涤。
