酚酞电离平衡常数的测定
姓名:王诗瑶 学号:20105052020
班级:20##级应用化学 成绩:
一、实验目的
1.用分光光度计测定酚酞的平衡常数。
2.了解分光光度计测定弱电解质电离平衡常数的原理。
3.掌握分光光度计和PH计的使用方法。
二、实验原理
酚酞是一元有机弱酸,用HR表示,在水溶液中按下式部分电离:
HR===H++R- (1)
无色 红色
在一定温度下,上述反应达到平衡后,若改变体系的酸的浓度,将是平衡移动;新的平衡到达时,各反应物浓度均有所变化,但平衡常数不变。本实验以不同的PH的缓冲溶液为反应介质在定温下测定酚酞的电离平衡常数。
若以[HR]0表示酚酞的原始浓度,则应有:
[HR]= [HR]0 - [R-] (2)
把(2)代入{1},并令电离度α=[R-]/[HR]0 则得:
KT=[H+] [α/(1-α)] (3)
本实验用分光光度计测吸光度,用PH计测其PH。
根据朗伯比尔定律,一有色物质溶液,在光径不变时,其浓度与吸光度成正比。故若取一定体积的酚酞溶液加到一已知PH的缓冲溶液中测定吸光度为A,在相同的条件下,加适量的氢氧化钠溶液,使酚酞完全电离,测得吸光度为A0。根剧电离度的定义和比尔定律,下式成立:
α=[R-]/[HR]0=A/ A0 (4)
从而得出KT的计算公式为:
KT=[A/(A0-A)]x10-PH (5)
三、实验仪器
分光光度计、容量瓶(1000ml)烧杯(50ml),移液管,乳头滴管
酚酞溶液0.5%,NaOH溶液0.1M 混酸0.4M 、蒸馏水
四、实验步骤
在1,3,5,号的三个250ml的容量瓶中分别加入2.50ml0.5%的酚酞和2.50ml0.4M的混酸后,加入蒸馏水至容量瓶体积的2/3,摇匀,用乳头滴管吸取1M NaOH分别滴在上述5只容量瓶中,刚好滴至微红,然后改用0.1M NaOH,使1至5号瓶中的溶液的颜色红色由浅到深形成一个色阶,最后用蒸馏水稀释到刻度,在另一支100ML的容量瓶中,编号6,加入0.25ml0.5%的酚酞,5.00ml0.1M的NaOH,用蒸馏水稀释到刻度,迅速测定它们的吸光度和PH值。
五、实验数据记录与处理
实验温度:20℃
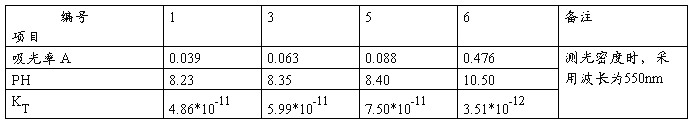
由实验数据可得A0=10A0=4.76,且KT=[A/(A0-A)]x10-PH
故可得各组结果KT如上表所列。因为KT4很小造成误差大故忽略。
 =
=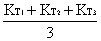
故 =6.12*10-11
=6.12*10-11
六、思考题
1.所配溶液色阶颜色太深对实验有无影响?
答:有影响。溶液的吸光度在0.1至0.7这个范围准确性最高,吸光度超出这个范围,即对应的浓度超出这个范围,准确性要打折扣。吸光度在0.434时,准确度最高,越接近这个值,精度越高。
2.一至五号瓶子中酚酞的量不一致对实验结果有无影响?
答:没有影响,平衡常数对于一个特定的反应来说,当温度确定时,它是一个常数,不随着反应物的量的变化而变化,故1至5号瓶子中的酚酞的量可以不一致。。
七、误差分析
1.移液时有误差,进而对实验结果造成误差。
2.容量瓶定容是存在误差,进而对实验结果造成误差。
3.比色皿的清洗不彻底,会对实验造成一定误差。
4.吸光率的测定和PH的测定不是同时进行也会造成一定实验误差。
5.由于实验仪器长期使用,会出现一定的磨损,是使实验仪器的精密度降低,进而对实验结果造成一定影响。
第二篇:化学平衡常数2

