实验 《硝酸钾溶解度的测定和溶解度曲线的绘制》实验报告
姓 名: 班 级: 柜 号: 日期:
一、 实验目的:
二、 原理:
三、 实验步骤流程图:
四、实验结果与讨论:
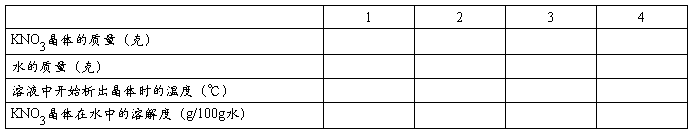
查阅资料,列出KNO3晶体在水中的溶解度:
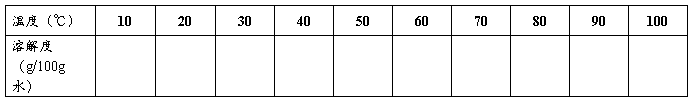

温度 (℃)

 硝酸钾的溶解度曲线(实验值 ,理论值 )
硝酸钾的溶解度曲线(实验值 ,理论值 )
五、思考题:
1. 为什么小试管要悬在盛有250mL水的烧杯内?为什么温度计要紧贴小试管且水银球要全部浸入水面以下?
2. 能否用量筒取1mL水?为什么?
3. 本实验中,如果冷却过程太快将产生什么结果?
成绩: .
评阅人: 日期: .
第二篇:溶解度实验报告
实验一 溶解度实验
一、实验目的
掌握不同的溶剂对有机化合物进行分组的方法
二、实验原理
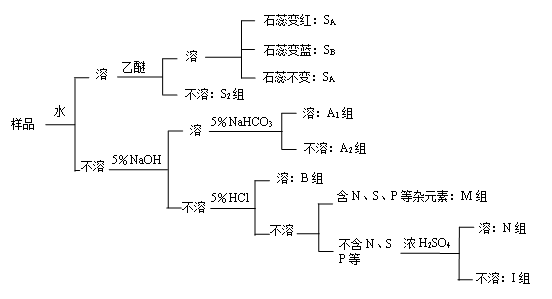
利用“相似相溶”原理,根据化合物在水、乙醚、5%NaOH、5%NaHCO3、5%HCl、浓H2SO4这六种溶剂中的溶解行对有机化合物进行分组。
三、仪器及试剂
仪器:干燥试管、试管夹、滴管
试剂:蒸馏水、乙醚、5%氢氧化钠、5%盐酸、5%碳酸氢钠、浓硫酸
乙醇、甘油、环己烯、氯苯、苯甲酸、乙酰苯胺、苯酚、未知物
四、实验步骤
1.水溶度试验
取0.2mL(4~5滴)液体或0.1g固体试样于试管中,加1mL水振荡后,如不溶解可加至3mL观察是否溶解,若液体试样与水分层应注意试样与水的相对密度,固体试样微溶要继续做下面的溶度试验,水溶性试样应用pH试纸试其酸碱性。
2.乙醚溶度试验
若试样溶于水,可做乙醚试验,方法同水溶度试验,但必须用干燥试管及纯净的乙醚。
若试样溶于乙醚列入S1组。
若试样不溶于乙醚列入S2组。
3.5%盐酸溶度试验
取不溶于水而含氮的试样0.1g或0.2mL,分3次加入3mL5%HCl,振荡后,试样溶解的为含氮的碱性化合物,属于B组。可再做5%NaOH的溶度试验,试其是否为两性化合物。
不含氮的水不溶物不必做此试验。
4.5%NaOH溶度试验
取不溶于水和5%HCl的试样0.1g或0.2mL按照上法分3次加入3mL5%NaOH溶液,振荡后溶解者为酸性化合物,可再做5%NaHCO3溶度试验。
5.5%NaHCO3溶度试验
另取溶于5%NaOH试样0.1g或0.2mL按照上法分3次加入3mL5%NaHCO3溶液,振荡(注意观察是否有CO2气体放出)溶解为A1强酸性组,不溶解为A2弱酸性组。
6.浓H2SO4溶度试验
在干燥试管中加3mL冷浓H2SO4,慢慢加入0.1g或0.2mL试样,随时振荡,观察所起变化:是否放热?颜色变化?有无沉淀生成?有无气体放出?溶者为中性化合物属N组不溶者属惰性组I组。
对以上试验均为负性反应,且不含N、S、P等杂元素的化合物列为惰性化合物属I组。
以(1)乙醇、(2)甘油、(3)环己烯、(4)氯苯、(5)苯甲酸、(6)乙酰苯胺、(7)苯酚为例下表列出溶度测定试验的报告格式:
表1-3 试验报告表

注:表中“+”表示溶解;“-”表示不溶解;若介于溶解和不溶解之间的现象,则用符号“±”表示;“/”表示不需试验的项目。
五、注意事项
1. 实验时溶剂必须按顺序进行,不能前后颠倒。当试样找到溶解度组后不再试验其在其它溶剂中的溶解情况。
2. 所有实验均在室温下进行,不能加热。
3. 如果溶质与溶剂发生作用,不论是否形成均匀溶液,均认为溶解。
4. 注意两性物质。
六、实验讨论
1. 水溶性化合物以pH试纸试酸碱性。
2溶质在非反应性溶剂中溶解度的大小,主要取决于溶质分子之间,溶剂分子之间及它们相互之间作用力的大小。溶质与溶剂的极性愈相近,则该溶质在该溶剂中的溶解度愈大;反之,溶解度就愈小。
3. 在有机化合物的分子中引入卤原子后,卤代物的水溶性随卤素相对原子质量的增大而减小。往往成为难溶于水或不溶于水的化合物。
4. 形成氢键的效应,对于化合物在水中溶解度的影响,往往比化合物分子的极性对溶解度的影响更为显著。
5. 含有支链的化合物,分子间的引力减小,溶解度增大。并且支链愈多,溶解度就愈大。
6.通过实验大体确定某物质的组成性质,为其提取或纯化确定条件提供依据。
7.溶质的介电常数愈大它在介电常数大的溶剂中就愈易溶解,溶质的介电常数愈小,则它在介电常数愈小的溶剂中愈易溶解。
8.熔沸点高的化合物,分子间的作用力较大,溶解度较小;熔沸点低的化合物,分之间的作用力较小,溶解较大。
附表:
溶度分组表

