双缩脲法测定小麦面粉中蛋白质的含量
实验八 双缩脲法测定面粉中蛋白质的含量
一、目的要求
1.学习双缩脲法的基本原理及操作。 2.通过实验学会制作标准曲线。 二、实验原理:
双缩脲(NH3CONHCONH3)是两个分子脲经180℃左右加热,放出一个分子氨后得到的产物。在强碱性溶液中,双缩脲与CuSO4形成紫色络合物,称为双缩脲反应。凡具有两个酰胺基或两个直接连接的肽键,或能过一个中间碳原子相连的肽键,这类化合物都有双缩脲反应。在一定的浓度范围内,紫色络合物颜色深浅与蛋白质含量呈线性关系(即:颜色的深浅与蛋白质浓度成正比)而与蛋白质分子量及氨基酸成分无关,故可在540nm处比色用来测定蛋白质含量。测定范围为1-10mg蛋白质/ml。干扰这一测定的物质主要有:硫酸铵、Tris缓冲液和某些氨基酸等。
此法的优点是较快速 ,不同的蛋白质产生颜色的深浅相近,以及干扰物质少。主要的缺点是灵敏度差。因此双缩脲法常用于需要快速,但并不需要十分精确的蛋白质测定。 三、操作方法:
1.标准曲线的制作。酪蛋白:10mg/ml(如果用干酪素来配制则需用0.05M NaOH做溶剂,也可以用酪蛋白酸水解物直接配制。)
管号
酪蛋白(ml) 蒸馏水(ml) 双缩脲试剂(ml) 1 0 2 3
A540 0
计算出各管浓度(计算出各管浓度,再做标准曲线,那么最后计算的公式中就不用除以6了,这么做好理解些。)
混匀,放置30分钟后,在540nm处以1号管调0点,测定各管吸光度,以吸光度(OD值)为纵坐标,蛋白质浓度(酪蛋白的毫克数)为横坐标绘制
2 3
0.4 0.8 1.6 1.2 3 3
混匀,放置30分钟
4
1.2 0.8 3 5 1.6 0.4 3 6 2 0 3
双缩脲法测定小麦面粉中蛋白质的含量
标准曲线。
四、样品处理
1.0.25g小麦面粉+0.5ml四氯化碳+25ml双缩脲试剂(四氯化碳为有机溶剂,在这里作为分散剂,使面粉不成团。);
2.加塞,在摇床上振摇30分钟,使之充分混匀、反应,然后于实验台上静置10分钟;
3.离心,4000rPm,离心15分钟;
4.取上清比色:OD 540 nm;(在用滴管取上清时要轻、缓,避免沉淀物上浮。对照管是以介质溶液调零,即去除样品后的溶剂,在这里为0.5ml四氯化碳+25ml双缩脲试剂。)
五、计算
OD值所对应的蛋白质毫克数×25.5/6/200 ×100% 即面粉中酪蛋白的百分含量。
『双缩脲试剂』:取 1.5g 硫酸铜(CuSO4·5H2O)和 6.0g 酒石酸钾钠
(NaKC4H4O6·4H2O)溶于500ml蒸馏水中,搅拌加入300ml的10%NaOH(或KOH)(可另加 lg KI以防止Cu2+自动还原成一价氧化亚铜沉淀),用水稀释至l000ml。此试剂存于棕色瓶中避光可长期保,若有黑色沉淀产生需重配。
【注意事项】
标准曲线绘制和样品测定应使用同一台分光光度计。注意事项
(1)本法应用范围,因不同书籍报道,数值不一。本实验方法测定范围1—10mg蛋白质/ml。
(2)须于显色后30min内比色测定。30min后,可有雾状沉淀发生。各管由显色到比色的时间应尽可能一致。
(3)有大量脂肪性物质同时存在时,会产生混浊的反应混合物,这时可用乙醇或石油醚使溶液澄清后离心,取上清液再测定。
第二篇:实验一 双缩脲法测定血清蛋白质含量
实验一 双缩脲法测定血清蛋白质含量
【实验名称】:双缩脲法测定血清蛋白质含量
室温:20°
(一)实验目的: 1.掌握双缩脲法测定蛋白质的原理。2.学习掌握分光光度计的使用。
3.掌握标准曲线的制作。4.学习分光光度法测定的原理和方法。
(二)实验原理:血清中蛋白质的肽键(-CO-NH-)在碱性溶液中能与2价铜离子作用生成稳定的紫红色络合物。此反应和两个尿素分子缩合后生成的双缩脲(H2N-OC-NH-CO-NH2)在碱性溶液中与铜离子作用形成紫红色的反应相似,故称之为双缩脲反应。这种紫红色络合物在540nm处有明显吸收峰,吸光度在一定范围内与血清蛋白含量呈正比关系,经与同样处理的蛋白质标准液比较,即可求得蛋白质含量。
(三)实验材料与仪器:
1.仪器和材料: 分光光度计、7支试管、1毫升刻度吸管3支、移液器、坐标纸。
2.试剂:6mol/L的NaOH、双缩脲试剂、9g/L的NaCl溶液、蛋白质标准液(10g/L)、待测血清样本。
(四)实验步骤和结论:
1.取7支试管,编号,按照图1操作并记录。
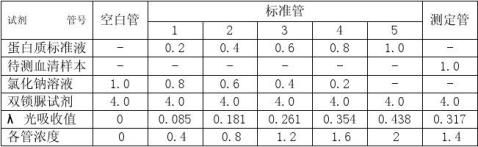
表 1
2.在坐标纸上以各管蛋白质含量为横坐标,光吸收值(两管平均值)为纵坐标,绘制标准曲线。
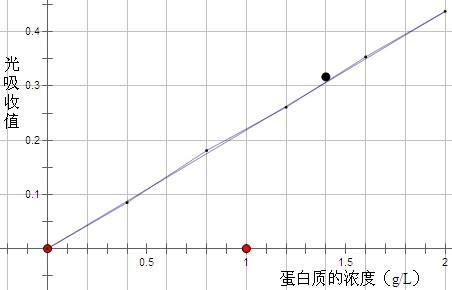
表2
3、由标准曲线查出待测的血清样本的蛋白质浓度,由表1得出测定管的蛋白质的λ光吸收值为0.317,由表2得出测定管的蛋白质的浓度为1.4g/L
4、按照光吸收法计算公式计算,从标准管中选一管与测定管光吸收值接近者,按公式
C标A测C测?A标
计算待测血清样本的蛋白质浓度,从上可选A测 = 0.317
C标=0.354 ,A标=1.6 g/L; 则得到:C测=1.432 g/L
【注意事项】 : 1.本实验是定量实验,要求所有玻璃仪器必须清洁,整齐、干燥。蛋白质标准液和血清取量必须准确。
2.各管加好样后必须充分混匀。显色反应需在20到30min才完成。
3.3用分光光度计要注意:取吸收池时,应拿毛玻璃两面,切忌用手拿捏透光面,以免粘上油污;液体的体积为比色杯的2/3-3/4;不要将比色杯放在分光光度计上;试验完成后,关闭电源,洗净比色皿。
【思考题】1、蛋白质的肽键(-CO-NH-)在碱性溶液中能与2价铜离子作用生成稳定的紫红色络合物,这种紫红色络合物在540nm处有明显吸收峰,吸光度在一定范围内与血清蛋白含量呈正比关系,经与同样处理的蛋白质标准液比较,即可求得蛋白质含量。
3、各管加好样并充分混匀后,20到30min才能完成显色反应,所以本实验在加入双缩脲试剂20到30min左右的时间才进行比色,在显色后30min内进行显色,且各管测定时间几乎要相同。
