肝糖原的提取、鉴定与定量
一、实验目的
1. 掌握组织样品的制备方法,了解其注意事项。
2. 了解肝糖原提取、糖原和葡萄糖鉴定与蒽酮比色测定糖原含量的原理和注意事项,掌握其操作方法。
3. 正确操作使用刻度吸管和可调微量取液器。
4. 熟练运用溶液混匀的各种方法(视具体情况,采用合适的混匀方法)。
5. 正确掌握溶液转移的操作。
6. 正确操作使用分光光度计。
二、实验原理
(一)肝糖原的提取、鉴定
糖原储存于细胞内,采用研磨匀浆等方法可使细胞破碎,低浓度的三氯醋酸能使蛋白质变性,破坏肝组织中的酶且沉淀蛋白质,而糖原仍稳定地保存于上清液中,从而使用糖原与蛋白质等其它成分分离开来。糖原不溶于乙醇而溶于热水,故先用95%乙醇将滤液中糖原沉淀,再溶于热水中。
糖原水溶液呈乳样光泽,遇碘呈红棕色。这是糖原中葡萄糖长链形成的螺旋中,依靠分子间引力吸附碘分子后呈现的颜色。糖原还可被酸水解为葡萄糖,利用呈色反应和葡萄糖的还原性,可判定肝组织中糖原的存在。
CuSO4十2NaOH═ Na2 SO4+Cu(OH)2↓
2Cu(OH)2十C6H12O6 ═ 2CuOH十氧化型葡萄糖+H2O
2CuOH═ Cu2O↓(红色)+H2O
 Cu(OH)2 ═ CuO↓(黑色)+H2O
Cu(OH)2 ═ CuO↓(黑色)+H2O
(二)肝糖原的定量
糖原在浓酸中可水解成为葡萄糖,浓硫酸能使葡萄糖进一步脱水生成糠醛衍生物—5-羟甲基呋喃甲醛,此化合物再与蒽酮脱水缩合生成蓝色的化合物。该物质在620nm处有最大吸收。糖含量在10-100μg范围内,溶液颜色的深浅与可溶性糖含量成正比。利用此反应与同样处理的已知葡萄糖含量标准溶液比色,通过标准对照法(直接比较法)即可计算出样品中糖原的含量。糖原在浓碱溶液中非常稳定,故在显色之前,肝组织先置于浓碱中加热,以破坏其它成分,而保留肝糖原。
三、材料与方法:以流程图示意
实验材料:
(一)仪器
1. 普通离心机,室温~100℃恒温水浴箱(×2),分光光度计,精度为10mg级电子天平(×1)
2. 剪刀(×1),镊子(×1),研钵(×1)
3. 试管架(×1),(100×15)mm试管(×3)
4. 刻度吸量管(2mL×1,5 mL×2),1000μL微量可调取液器(×1)
5. 100mL容量瓶(×1)
6. 白瓷反应板(×1)
(二)实验样品和试剂
1. 鸡肝。
2. 95%乙醇。
3. 0.31mol/L(5%)三氯醋酸溶液。
4. 0.15mol/L NaCl溶液。
5. 12mol/L HCl。
6. 12.5mol/L(50%)NaOH。
7. 碘试剂。
8. 班氏试剂。
9. 5.35mol/L(30%)KOH溶液。
11. 标准葡萄糖液(50mg/L)。
12. 17mol/L(90%)H2SO4(用于制备蒽酮显色剂)。
13. 蒽酮显色剂:称取蒽酮0.20g,用17mol/L H2SO4溶解至100 mL。此试剂不稳定,以当日配制为宜,冰箱保存可用4-5d。
实验方法:
吸取1mL量溶液时使用可调微量取液器,吸取1mL以上量溶液时使用刻度吸量管。
(一)肝糖原的提取与鉴定
操作流程如下:
 鸡肝约1.0g,剪碎
鸡肝约1.0g,剪碎
+5%CCl3COOH 1 ml
研磨至乳状
 +5%CCl3COOH 3 ml
+5%CCl3COOH 3 ml
 研磨成肝匀浆
研磨成肝匀浆
 全部转入离心管中,离心3分钟(4000 r / min)
全部转入离心管中,离心3分钟(4000 r / min)
沉淀(弃去) 上清(取2 ml)
 +2ml 95%乙醇,混匀,静置10分钟
+2ml 95%乙醇,混匀,静置10分钟
 离心5分钟(4000 r / min)
离心5分钟(4000 r / min)

上清(弃去) 沉淀
 +蒸镏水1 ml
+蒸镏水1 ml
 沸水浴2分钟,溶解沉淀
沸水浴2分钟,溶解沉淀

白瓷板孔穴中 糖原溶液1ml


 +浓HCl 5滴
+浓HCl 5滴
加碘试剂2滴 加碘试剂2滴 沸水浴15分钟,冷却


 糖原溶液2滴 +50%NaOH 5滴
糖原溶液2滴 +50%NaOH 5滴

呈色对比 糖原水解液2滴 糖原水解液
 +班氏试剂4滴
+班氏试剂4滴
混匀
沸水浴2分钟,观察变化
注意事项
1. 肝糖原提取一步,向上清液中加入95%乙醇后,务必注意混匀。由于上清液为水溶液,比重大于95%乙醇,溶液分成两层。总量相对较多,混匀操作比较困难,最好用倾倒混匀,也可用滴管或吸量管吸、吹混匀,或用玻璃棒搅拌混匀。
2. 糖原中葡萄糖螺旋链吸附碘产生的颜色与葡萄糖残基数的多少有关。葡萄糖残基在20个以下的会使碘呈现红色,20,30个之间使碘呈现紫色,60个以上的会使碘呈现蓝色。淀粉中分枝链较长,故呈蓝色,而肝糖原分枝中的葡萄糖残基在20个以下(通常8-12个葡萄糖残基),吸附碘后呈现红棕色。
3. 糖原水解液中葡萄糖的鉴定一步,加班氏试剂不能过量,否则反应液呈黑色浑浊,观察不到应有的结果。
(二)肝糖原定量测定
操作流程如下:
鸡肝0.10 g
 +30%KOH 1.5ml (用吸量管)
+30%KOH 1.5ml (用吸量管)
沸水浴15分钟
冷却,全部转入100 ml容量瓶中

 加水至标线,仔细混匀,此为糖原提取液
加水至标线,仔细混匀,此为糖原提取液
糖原的测定
取3支试管,按下表操作。

混匀,沸水浴10分钟,冷却。在分光光度计620 nm波长处,用空白管溶液调零,测定各管溶液的吸光度(A)。
计算:
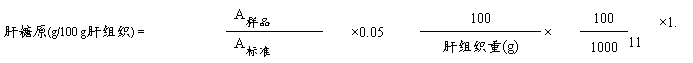
四、结果与讨论:①结果:实验数据、现象、图谱;②讨论:以结果为基础的逻辑推论,并得出结论。
(一)结果
1.鉴定实验中的呈色对比
1) 结果:
2) 结论:如图所示,加入提取的糖原溶液后,颜色变浅(碘液稀释后变浅),但并未变成红棕色,所以用这种鉴定方法鉴定不出有糖原的存在。
2.鉴定实验中葡萄糖还原反应
1) 结果:
2) 结论:水浴后,溶液的颜色加深,但并未生成红黄色沉淀,所以用这种鉴定方法鉴定不出有糖原的存在。
3.肝糖原定量测定实验
1) 结果
定量实验中沸水浴后空白管、标准管和样品管的颜色(从左至右)
吸光度测定结果

2) 结论:
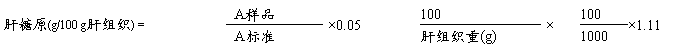
根据上式计算,代入 A样品=, A标准=,肝组织重(g)=,
可得
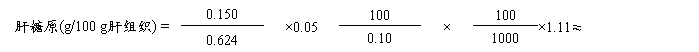
此鸡为不饱食鸡。
第二篇:肝糖原提取和测定
肝糖原的提取和鉴定
一、实验目的
1.了解肝糖原的性质并掌握其提取的方法。
2.熟悉肝糖原的鉴定方法。
二、实验原理
肝糖原是糖在体内的重要储存形式之一。其储存量虽然不多,但在代谢过程中,它是动物体内糖的重要的来源之一。肝糖原的合成或分解对血糖浓度的调节起着重要的作用。
糖原属于高分子糖类化合物,微溶于水,无还原性,与碘作用变成红棕色。提取肝糖原是利用三氯醋酸破坏肝组织中的酶,且肝组织中的蛋白质也被三氯醋酸所沉淀,而糖原仍留在溶液中。过滤除去沉淀,滤液中的肝糖原可借加入的乙醇而沉淀。将沉淀的糖原溶于水,即可得到糖原溶液。
糖原与碘作用呈红棕色。糖原被酸水解为葡萄糖,可用班氏试剂检验。利用呈色反应和葡萄糖的还原性,可判定组织中糖原的存在。
三、实验材料、仪器和试剂
1. 材料:
小白鼠等动物新鲜肝脏组织
2. 仪器:
(1)天平 (2)研钵 (3)离心机
(4)离心管 (5)恒温水浴锅 (6)试管
(7)广泛试纸 (8)移液管 (9)洗耳球
Page 1 of 3
(10)电炉 (11)量筒 (12)滤纸
3. 试剂:
(1)10%的三氯醋酸溶液
(2)5%的三氯醋酸溶液
(3)95%乙醇溶液
(4)浓盐酸
(5)20%的NaOH溶液
(6)碘液:(取碘1g、碘化钾2g溶于500mL蒸馏水中)
(7)班氏试剂:(将硫酸铜17.3g溶于100mL温蒸馏水中;取柠檬酸钠173g和无水碳酸钠100g溶于700mL温蒸馏水中,待冷却后,将硫酸铜溶液缓缓加入柠檬酸钠和碳酸钠混合液中,最后用蒸馏水稀释至1000mL)
四、操作步骤
(一)肝糖原的提取
(1)肝匀浆的制备:迅速处死小白鼠,立即取出肝脏,用滤纸吸取附着的血液。称取约1g肝脏置研钵中,加入少许石英砂及10%的三氯醋酸溶液1mL,研磨至呈乳状后再加入5%的三氯醋酸2mL,继续研磨,直至肝脏组织已充分磨成均匀糜浆。
(2)提取糖原:将制备好的肝匀浆以3000r/min的转速离心10min。取上清液于另一离心管并量取体积,加入等体积的95%乙醇溶液,混匀后静置10min,使糖原呈絮状析出。将沉淀溶液以3000r/min的转速离心10min,弃去上清液,将离心管倒置于滤纸上1~2min,向沉 Page 2 of 3
淀中加入蒸馏水1mL,用细玻璃棒搅拌至溶解,即成糖原溶液。
(二)肝糖原的鉴定
(1)与碘的呈色反应:取小试管2支,一支加入糖原溶液10滴,另一支加入蒸馏水10滴,然后两管各加入碘液2滴,混匀。观察两试管中溶液的颜色变化,并解释现象。
(2)糖原水解液中葡萄糖的鉴定:在剩余的糖原溶液中加入浓盐酸3滴,放入沸水浴中加热10min,取出冷却,用20%的NaOH溶液中和至中性(用pH试纸检测)。然后加入班氏试剂2mL,再置沸水浴中加热5min,取出冷却。观察管中沉淀的生成,并解释现象。
五、注意事项
(1)实验用小白鼠在实验前必须饱食,因为空腹时肝糖原易分解而使其含量减少。
(2)肝脏离体后,肝糖原会迅速分解,所以在杀死动物后,所得刚脏必须迅速用三氯醋酸溶液处理。
Page 3 of 3
