总糖和还原糖含量的测定实验报告
南京大学生命科学学院
张茜 111070094
实验目的 :
植物体内的还原糖,主要是葡萄糖、果糖和麦芽糖。它们在植物体内的分布,不仅反映植物体内碳水化合物的运转情况,而且也是呼吸作用的基质。还原糖还能形成其他物质如有机酸等。此外,水果蔬菜中糖量的多少,也是坚定其品质的重要指标。还原糖在有机体的代谢中起着重要的作用,其他碳水化合物,如淀粉蔗糖等,经水解也生成还原糖。通过本实验,掌握还原糖定量测定的基本原理,练习比色定糖法的基本操作,热悉分光光度计的使用方法。 实验原理:
1. 还原糖
还原糖是具有还原性的糖类的统称。分子中含有游离醛基或者酮基的单糖和含有游
离醛基的二糖都具有还原性。如葡糖糖、果糖、半乳糖、乳糖、阿拉伯糖、麦芽糖等。
2. 美拉德反应
美拉德反应广泛分布于食品工业中的非酶褐变反应:还原糖与氨基酸/蛋白质在加
热时发生的一系列复杂反应,生成棕/黑色的大分子物质,同时还产生具有不同气味的中间体分子,包括还原酮、醛和杂环化合物,为食物提供诱人可口的风味和诱人的色泽。
3. 还原糖的测定方法:3,5-二硝基水杨酸法
在波长540nm下,一定浓度范围内,还原糖的量与光吸收值呈线性关系,可利用标准曲线法测定样品中的还原糖含量。
利用多糖能被酸水解为单糖的性质可以通过测定水解后的单糖含量来对总糖进行测定。
4. Lambert-Beer定律
A=lg(I0/I)=lg(1/T)=KCl
A:吸光度
I0:入射光强度
I:透射光强度
T:透光度(透射比)
K:比例常数
l:溶液厚度
实验仪器,试剂与材料:
1. 实验仪器:UV2600紫外可见分光光度计
2. 实验试剂:
(1)1.0mg/ml标准葡萄糖

(2)3,5-二硝基水杨酸(DNS试剂)
(3)6mol/L HCl(张茜配置)
(4)6mol/L NaOH(张茜配置)
(5)碘-碘化钾溶液
3. 实验材料:市售面粉。
实验步骤:
1. 还原糖的提取
准确称取0.20g面粉,加蒸馏水约3ml,在研钵中磨成匀浆。,转入三角烧瓶中,用约30ml蒸馏水冲洗研钵2~3次,洗出液也转入三角烧瓶中。于50℃恒温水浴中保温20min,不时搅拌,使还原糖浸出。将浸出夜(含沉淀)转移到100ml离心管中,于4000r/min下离心5min,沉淀用20ml蒸馏水洗一次,再离心,将两次离心的上清液合并,用蒸馏水定容至100ml,混匀,作为还原糖待测液。取1ml进行还原糖的测定。
2. 总糖的水解
准确称取0.50g面粉,加蒸馏水3ml,在研钵中磨成匀浆后转入三角烧瓶中,并用12ml蒸馏水冲洗研钵2~3次,洗出液也转入三角烧瓶中。再向三角烧瓶中加入6mol/L HCl 10ml,搅拌均匀后在沸水浴中水解0.5h,取出1~2滴置于白瓷板上,加1滴I2-KI溶液检查水解是否完全。如已水解完全,则不显蓝色。水解完毕,冷却至室温后用6mol/L NaOH溶液中和至pH呈中性。然后用蒸馏水定容至100ml,过滤,取滤液10ml,用蒸馏水定容至100ml,成稀释1000倍的总糖水解液。取0.5ml总糖水解液,测定其还原糖的含量。
3. 还原糖标准曲线的制作与样品的测定
数据记录与处理:
一.
还原糖的提取
面粉质量:m1=0.20g 二.
总糖的提取
面粉质量:m2=0.50g
6M HCl;6M NaOH(张茜配置) 三.
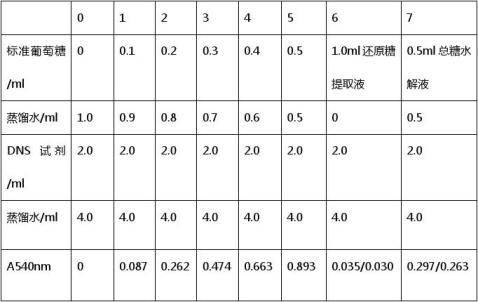
样品的测定
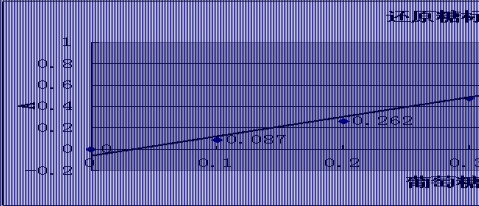
标准曲线:回归曲线为y=0.183x-0.061
1) 由第六组数据分析可知,还原糖提取液对应的吸光度值为: (0.035+0.030)/2=0.032
样品还原糖含量为:
X=(0.032+0.061)/0.183=0.508
实验对象中还原糖的含量为:
100X/200 = 25.4 %
2) 由第七组数据分析可知,总糖提取液对应的吸光度值为: (0.297+0.263)/2=0.280
样品总糖的含量为:
X=(0.280+0.061)/0.183= 1.863
实验对象中总糖的含量为:
200X/500 = 74.5 %
注意事项:
1. 沸水浴时应将试管口用保鲜膜封住,以防止水分蒸发引起体积误差。
2. 应该待反应体系稳定后进行比色(约10min)。
3. 比色时,比色皿中盛放的溶液体积不应过多,一般在2/3~3/4。
4. 比色时不能将溶液溅在仪器面板和仪器内。
5. 标准曲线制作与样品含糖量测定应同时进行,一起显色和比色。
第二篇:实验二 还原糖及总糖的测定
实验二 还原糖及总糖的测定
(3、5——二硝水杨酸比色法)
目的和要求:
1.掌握3、5-二硝基水杨酸比色法测定糖量的原理及方法。
2.熟悉722分光光度计基本工作原理和操作方法。
原理:
各种单糖和麦芽糖是还原糖,蔗糖和淀粉是非还原糖。利用溶解度不同,可将植物样品中的单糖、双糖和多糖分别提取出来,再用酸水解法使没有还原性的双糖和多糖彻底水解成有还原性的单糖。
在碱性条件下,还原糖与3、5—二硝基水杨酸共热,3、5—二硝基水杨酸被还原为3-氨基-5-硝基水杨酸(棕红色物质),还原糖则被氧化成糖酸及其它物质。

在一定范围内,还原糖的量与棕红色物质颜色深浅的程度成一定的比例关系,可在分光光度计540nm波长测定棕红色物质的吸光值。查标准曲线计算,便可分别求出样品中还原糖和总糖的含量。
多糖水解时,在单糖残基上加了一分子水,因而在计算中须扣除已加入的水量,测得所得到的总糖量乘以0.9即为实际的总糖量。
该方法是半微量定糖法,操作简便,快速,杂质干扰较少。
试剂和材料:
1.试剂
(1)1mg/ml葡萄糖标准液:准确称取100ml分析纯葡萄糖(预先在105℃烘至恒重),置于小烧杯中,用少量蒸馏水溶解后,定量转移到100ml容量瓶中,以蒸馏水定容到刻度,摇匀,冰箱中保存备用。
(2)3、5—二硝基水杨酸试剂(又称DNS试剂)
甲液——溶解6.9g结晶酚(苯酚)于15.2ml 10%NaOH中,并稀释至69ml,在此溶液中加入6.9g亚硫酸氢钠。
乙液——称取22.5g酒石酸钾钠,加到300ml 10% NaOH中,再加入880ml 1%的3、5—二硝基水杨酸溶液。
将甲液和乙液相混合即得黄色试剂,贮于棕色试剂瓶中,放置7—10天使用。
(3)碘—碘化钾溶液(碘试剂):称取5g碘和10g碘化钾,研匀后溶于100ml蒸馏水中。
(4)酚酞指示剂:称取0.1g酚酞溶于70%乙醇中。
(5)6 mol·L-1 HCl
(6)6 mol·L-1NaOH
(7)面粉
2.器材
比色管、离心管、量筒、三角瓶、容量瓶、刻度吸管、玻璃漏斗、滤纸、白瓷板、
电热恒温水浴槽、离心机、天平、分光光度计。
操作步骤:
1.标准曲线的制作
取6支干燥试管,编号,按下表所示的量,精确浓度为1.00mg/ml的葡萄糖标准液和3、5—二硝基水杨酸试剂。
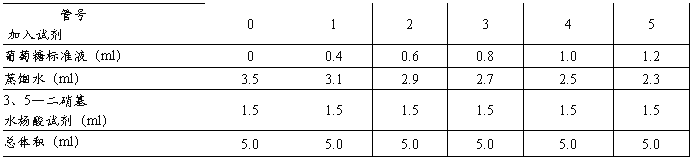
将各管摇匀,带上小漏斗,在沸水浴中加热5min,立即用冷水冷却至室温,再向各管中加入蒸馏水20.0ml,用橡皮塞塞住管口,颠倒混匀。切勿用力振摇,引入气泡。在540nm波长下,以0号管为空白,在分光光度计上测定1-5号管的吸光值。以吸光值为纵坐标,葡萄糖毫克数为横坐标,绘制标准曲线。
2.样品中还原糖和总糖含量的测定
(1) 样品中还原糖的提取:
称取2.00g左右在常温下于干燥器内保存数日的面粉,置于125ml三角瓶中,以少量水调成糊状,再加入40ml蒸馏水,搅匀,置于50℃恒温水浴中保温20 min。其间间或振荡,使还原糖浸出。
将上液倒入100ml容量瓶中,用少量的蒸馏水多次洗涤三角瓶内残留物,将所得的洗涤液全部收集于100ml容量瓶中,用蒸馏水定容至刻度,混匀。
取适量上液于离心管中,在3500转/分下离心10分钟。上清液作为还原糖待测液。
(2) 样品中总糖的水解和提取:
称取0.80g左右同样的面粉,置于125ml三角瓶中,加入15ml蒸馏水,10ml 6 mol·L-1的HCl,在沸水浴中加热30 min。用滴管取1-2滴于白瓷板上,加1滴碘-碘化钾试剂,若不显蓝色,表明水解完全。
将瓶中水解液冷却,加入1滴0.1%的酚酞指示剂,用6 mol·L-1NaOH中和至微红色。然后将上溶液倒入100ml容量瓶中,并用少量的蒸馏水多次洗涤三角瓶内的残留物,将所得的洗涤液全部收集于100ml容量瓶中,用蒸馏水定容至刻度,混匀。
取适量上液于离心管中,在3500转/分下离心10分钟 ( 或过滤于干燥的三角瓶中,弃去前几毫升滤液,得滤液约15ml);准确吸取其上清液10.0ml,再定容至100ml,作为总糖的待测液。
取5支干燥试管,编号,按下表所示的量,精确加入待测液和试剂:

加完试剂后,其余操作步骤与制作葡萄糖标准曲线时的相同,测定出各管溶液的吸光值。
计算:
以管1、2、3的吸光值的平均值和管4、5、6的吸光值的平均值,分别在标准曲线上查出相应的还原糖毫克数,按下式计算样品中还原糖和总糖的百分含量:


 还原糖 % =
还原糖 % =
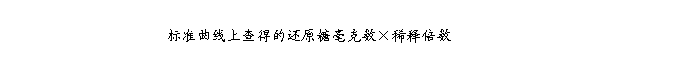

 总 糖 % = × 0.9×100
总 糖 % = × 0.9×100
思考题
(1) 若要获得较为理想的标准曲线,操作时应注意哪些问题?
(2) 比色测定时为什么要设空白管?
