双液体系沸点-成分图的绘制
实验者:
学号:
班级
合作者:
编号:
实验日期:
室温:
大气压
摘要:本实验采用冷凝回流法测定不同成分比例下的环己烷-乙醇混合体系的沸点,用阿贝折射仪测定相应沸点下气相冷凝液与液相的折射率,用内插法根据已知成分比例体系绘制的标准工作曲线得到各沸点下液相、气相成分,在坐标纸上绘制T-x平衡图,并求出最低恒沸点65.09℃,该沸点下气相、液相的混合物成分均为质量分数33.87%的乙醇及质量分数66.13%的环己烷。
引言部分
一、实验目的
1、用冷凝回流法测定不同浓度的环己烷-乙醇体系的沸点;
2、正确使用阿贝折射仪;
3、绘制沸点-成分图,确定体系的最低恒沸点和相应的组成。
二、实验原理
1、沸点-成分图
在恒压下,完全互溶双液体系的沸点与成分关系有三种情况:
(1)溶液沸点介于二纯组分之间,如甲苯与苯;
(2)溶液有最高恒沸点,如卤化氢和水,丙酮和氯仿等;
(3)溶液有最低恒沸点,如环己烷和乙醇,水和乙醇等。
图1表示有最低恒沸点的体系的沸点-成分图。图中:A’LB’代表液相线,AVB’代表气相线。等温的水平线段和气、液的交点表示在该温度时互成平衡的两相成分。
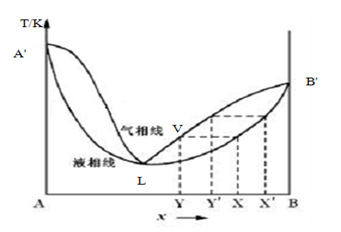
图1 具有最低恒沸点的体系的沸点-成分图
绘制沸点-成分图的简单原理:当总成分为x的溶液开始蒸馏时,体系的温度沿虚线上升,开始沸腾时成分为y的气相生成,气相量很少,继续蒸馏,气相量增多,沸点沿虚线继续上升,当气相线与液相线沿箭头指示方向达到x’和y’时,体系气液两相达成平衡,两相的物质数量按杠杆原理分配。在实验装置中,利用回流的方法保持气、液两相的相对量一定,体系温度恒定。待两相平衡后,取出两相物质用阿贝仪侧折射率,再用标准曲线取点的方法分析两相成分,给出该温度下气、液二相平衡成分的坐标点;改变体系总成分,再如上法找出另一对坐标点。将所有气相点和液相点连成气相线和液相线,即得T-x平衡图。
2、阿贝仪的使用
阿贝仪利用了折射和全反射全反射原理设计而成。 将样品滴在棱镜上,旋转棱镜使目镜能看到半明半暗现象。旋转补偿棱镜消除色散,在转动棱镜使明暗界线正好与目镜中的十字线交点重合,从标尺上直接读取折射率。
实验部分
三、实验仪器及药品
1、仪器
恒沸点仪 阿贝尔折射仪(WZS-I 940168) 蒸馏瓶 电阻丝 变压器
水银温度计(50~100℃ ,分度值0.1℃ )
恒温水浴装置 5mL、20mL移液管 滴瓶 万分之一天平
2、药品
乙醇 环己烷
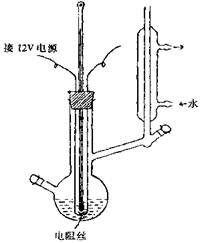
图2 恒沸点仪
四、实验内容
1、沸点和两相成分的测定
1)洗净、烘干蒸馏瓶,加20mL乙醇使温度升高并沸腾,每隔30s记一次数据;
2)待温度稳定3min后,记最终温度及大气压;
3)断电,用两只滴管取支管口处气相冷凝液及蒸馏瓶中液体,用阿贝折射仪测折射率,气相冷凝液测1次,液相测2次;
4)蒸馏瓶中依次加2mL、2mL、3mL、4mL、5mL环己烷,按上述方法测沸点及气液两相折射率;
5)回收母液,少量环己烷洗蒸馏瓶3~4次,注入20mL环己烷,测纯沸点及气液两相折射率;
6)再向蒸馏瓶中依次加0.5mL、0.5mL、0.5mL、2mL、5mL、5mL乙醇,分别测沸点及气、液两相折射率。
2、标准工作曲线绘制
1)8个滴瓶编号,分别准确称质量并记录,依次向各瓶加5mL、4mL、3mL、2.5mL、2mL、1.5mL、1mL、0.5mL乙醇,称质量并记录数据,再依次向各瓶加入1mL、2mL、3mL、3.5mL、4mL、4.5mL、5mL、5.5mL环己烷,称质量并记录数据;
2)恒温下测配置样品折射率(三次);
3)利用内插法,在标准工作曲线中找出各折射率对应成分,画T-x平衡图。
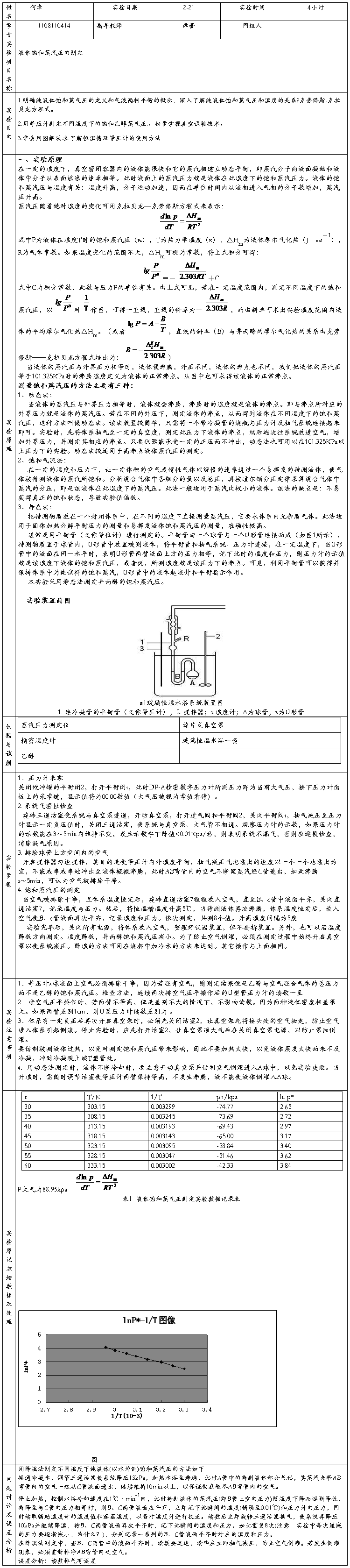
五、实验数据及处理
1、初始为20mL乙醇
表1 向乙醇中加环己烷数据表
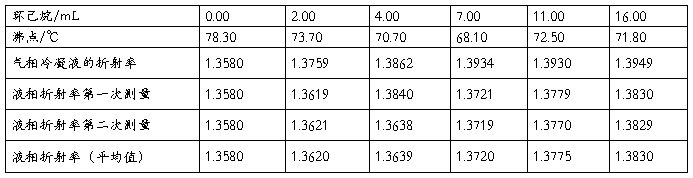
注:大气压102.36KPa 阿贝折射仪恒温:25.60℃
2、初始为20mL环己烷
表2 向环己烷中加乙醇数据
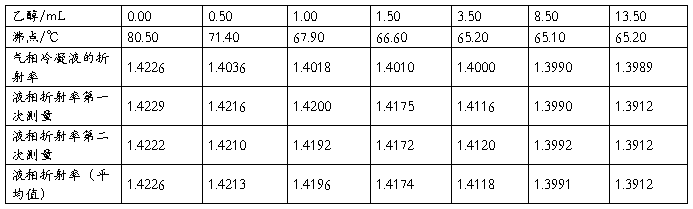
注:大气压102.36KPa 阿贝折射仪恒温:25.60℃
3、 绘制标准工作曲线
表3 标准成分数据表
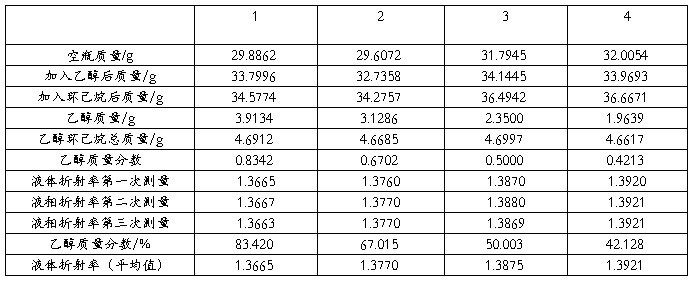
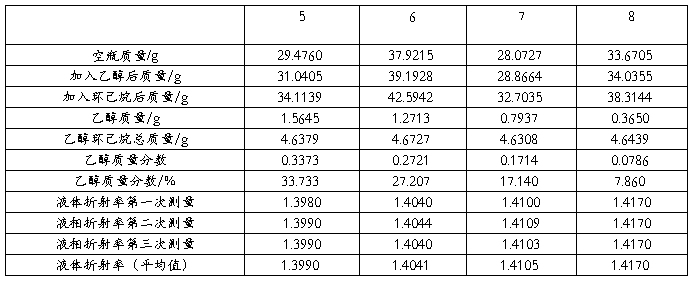
注:大气压102.36KPa 阿贝折射仪恒温:25.60℃
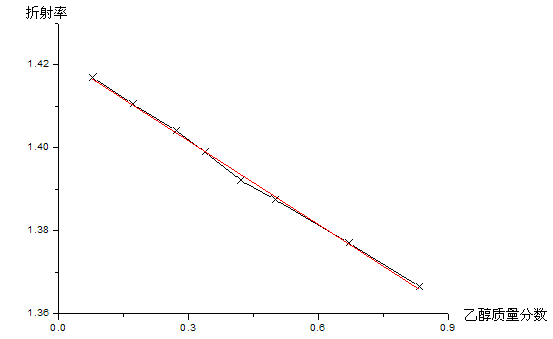
图3 标准工作曲线
其中拟合函数(一次拟合):
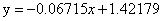
拟合相关系数R-square=0.9979
表4 计算乙醇质量分数表

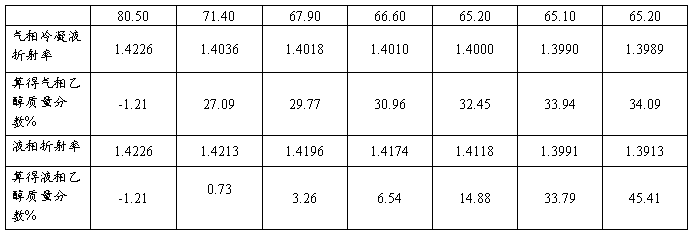
T-x图见附图
求得最低恒沸点:65.09℃。
相应成分:乙醇33.87%,环己烷66.13%。
思考与讨论
六、实验讨论
1、在每一次沸点测量实验中,我和合作者每隔30s就记录一次温度,发现温度是在上升下降中来回波动的,这是气相回流的缘故,气相开始逸出转移到冷凝管附近温度降下来,冷凝的气相积聚到一定程度便会回流到液相中,这时温度迅速降低,再慢慢升温,这样来回才最终在较稳定的温度下,并且在较稳定的温度也应该是动态平衡过程,只是温度变化不再明显。
2、向乙醇中加环己烷实验中,最后加4mL和5mL环己烷后,测得沸点过大,在实验过程中已经注意将气相冷凝液倒回液相中,但温度迟迟不降,怀疑是由于液体加入量过多导致温度计感受部分已完全浸没在液体中。由于整个体系并非绝对恒温,气液两相会有少许差别,因此要实验求温度计水银球的位置一般浸在溶液中,一半露在蒸气中,并在实验过程中不断调节温度计位置,但是实验条件所限我们不能不断调节温度计高度,因此可能仅仅测得局部液体温度。在处理数据时,已将这两个温度对应的四个数据排除考虑。
3、在用阿贝仪测液相折射率时,发现第一次与第二次测量值相差很大,因为液体折射率随温度变化而变化,约每摄氏度差5× 10-4。虽然阿贝折射仪有恒温装置保持恒温,但实验者每次在断电后就急于作第一次测量液体折射率,这时温度还高于恒温。并且该混合体系有强烈挥发性,折射率很难稳定下来,所以多次测量求平均值能消除一部分误差,但整体误差还是很大。
七、思考题
1.本实验中,气、液两相是怎样达成平衡的?若冷凝管D处体积太大,对测量有何影响?
答:在本实验采用的恒沸点仪中,利用冷凝回流的方法保持气、液两相的相对量一定,则体系温度一定,两相达平衡。
若冷凝管D处的体积太大,则气相冷凝液不易更新,客观上会造成气相蒸汽分馏,影响气相的平衡成分测定。
2.平衡时气、液两相温度应该不应该一样?实际是否一样?怎样防止温度的差异?
答:平衡时气、液两相温度应该一样,但实际上存在差异。气相温度存在梯度,温度略低于液相。
为防止差异可采用以下方法:给气相保温,如本实验那样,在恒沸点仪上部和支管处缠绕石棉绳;在支管口处增加一支温度计(其水银球上沿与支管口下沿相齐),上下两个温度计同时使用可以指示体系的平衡状态:实验过程中随加热进行,下方温度计先达到沸点温度,此时上面的温度计示数还很低;一段时间后,当蒸气达到上方温度计的高度(支管口)时,可以观察到上方温度计示数迅速上升,此后两个温度计示数趋于稳定,这时可以认为体系已经达到平衡,可以记录沸点和取样测量;在保证沸腾的液体不会溅到D处的条件下尽量缩短支管的长度和降低支管的位置。
八、实验结论
本实验通过冷凝回流法,对不同组成时的乙醇-环己烷体系的沸点和折射率进行了测定,并通过绘制标准工作曲线,确定在各沸点下乙醇-环己烷体系的气液两相组成,绘制了双液体系的相图, T-x图见附图,得出最低恒沸点65.09℃和此时气相液相各组分的质量分数均为:乙醇33.87%,环己烷66.13%。查文献得理论上最低恒沸点64.77℃(相对误差:4.940×10-3 )。该温度下乙醇质量分数为30.1%(相对误差:0.1252)。
参考资料
[1]北京大学化学学院物理化学实验教学组.物理化学实验(第四版).北京:北京大学出版社.2002
[2]高月英等.物理化学(生命科学类第二版).北京:北京大学出版社.2007
[3]从欢.介绍改进的恒沸点仪.大学化学,第22卷第2期,20##年4月:46-48
[5]Keshpande A K,lu B C Y.Journal of Chemical and Engineering Data,1963,8(4):549
[6]里佐威等.光纤干涉法测量液体折射率随温度变化.激光技术,1993年2月:50-52
第二篇:饱和蒸汽压的测定(1)
物理化学实验报
学院:化学与化工学院
班级: 无 机 111
姓名: 何孝
学号:1108110414
大学化学实验II实验报告—— 物理化学实验
学院: 化学与化工学院 专业: 无机非金属材料工程 班级:无机111
成绩: 指导教师签
20## 年 月 日
