
1 引言
在分子生物学日益普及的今天,基因操作已成为一项重要的常规技术。体外连接的DNA重组体导入合适的受体细胞便能大量地复制、增殖和表达,从而得到大量的重组基因,其中尤以转化为主[1]。感受态细胞的制备是分子生物学研究中的一个重要环节,其制备质量的好坏直接影响到后续实验工作的进行。本次实验的目的旨在了解转化的概念,及其在分子生物学研究中的意义,学习氯化钙法制备大肠杆菌感受态细胞的方法。
2 材料和方法
2.1 实验原理
质粒DNA需经过转化过程(transformation),才能将其导入感受态细胞(competent cell)或者大肠杆菌体中,然后通过寄主细菌的系统来达到复制DNA的目的。进行细菌转化作用最常用的一种方法是加入大量的氯化钙(calcium chloride),导致大肠杆菌的细胞壁发生结构上的变化,变成感受态细胞,而有利于质体DNA进入细菌细胞内。
大部分大肠杆菌品系的转化效率在105-108之间,即每μg质粒DNA中成功的转化细胞数目,影响此效率的因子与感受态细胞状況或吸收DNA的能力有关。而这2项因子又受细菌是否处于对数生长期、处理时是否将细胞保持在4°C以下,以及氯化钙处理细胞的时间影响。感受态细胞制备完成后,利用热休克处理,使细胞质膜的油脂变性而刺激转化作用,而后给予一段时间恢复后,可用对抗生素之抗性标记,进行筛选工作。本实验是利用冰冷的氯化钙溶液制备感受态细胞,其转化效率约在105-107之间。
转化(transformation)是将异源DNA分子引入另一细胞品系,使受体细胞获得新的遗传形状的一种手段,它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术。
本实验以E coli DH5α菌株为受体细胞,用CaCl2 处理受体菌使其处于感受态,然后与pMD18-T载体共保温,实现转化。
pMD18-T载体是一种高效克隆PCR产物 (TA Cloning) 的专用载体。这种载体是由pUC18载体改建而成,在pUC18载体的多克隆位点处的Xba I和Sal I识别位点之间插入了EcoR V识别位点,用EcoR V进行酶切反应后,再在两侧的3'端添加 "T" 而成。因大部分耐热性DNA聚合酶进行PCR反应时都有在PCR产物的3'末端添加一个 "A" 的特性,所以使用这两种制品可以大大提高PCR产物的连接、克隆效率。
该载体携带有抗氨苄青霉素基因,因而使接受了该质粒的受体菌具有抗氨苄青霉素的特性,同时还能进行蓝白斑筛选,其中有β-半乳糖苷酶基因(lacZ)的调控序列和前146个氨基酸的编码信息。在这个编码区中插入了一个多克隆位点(MCS),它并不破坏读框,但可使少数几个氨基酸插入到β-半乳糖苷酶的氨基端而不影响功能,这种载体适用于可编码β-半乳糖苷酶C端部分序列的宿主细胞。因此,宿主和质粒编码的片段虽都没有酶活性,但它们同时存在时,可形成具有酶学活性的蛋白质。这样,lacZ基因在缺少近操纵基因区段的宿主细胞与带有完整近操纵基因区段的质粒之间实现了互补,称为α-互补。由α-互补而产生的LacZ+细菌在诱导剂IPTG的作用下,在生色底物X-Gal存在时产生蓝色菌落,因而易于识别。然而,当外源DNA插入到质粒的多克隆位点后,几乎不可避免地导致无α-互补能力的氨基端片段,使得带有重组质粒的细菌形成白色菌落。这种重组子的筛选,又称为蓝白斑筛选。如用蓝白斑筛选则经连接产物转化的钙化菌平板37℃温箱倒置培养12-16hr后,有重组质粒的细菌形成白色菌落。图1为pMD18-T载体的克隆位点图[2]。
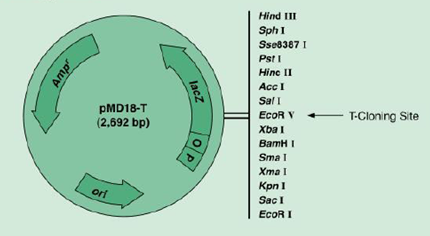

2.2 实验材料
2.2.1 仪器
所用仪器有超净工作台、低温离心机、恒温摇床、恒温箱、恒温水浴器、制冰机等。
2.2.2 器皿
所用器皿有移液枪(2.5ul、10ul、1000ul)、枪头盒(蓝、黄)、枪头(蓝、黄)、培养皿、1.5ml离心管、泡沫塑料盒、带帽试管、250ml锥形瓶、酒精灯、浮子等。
2.2.3 试剂
所用试剂有0.1mol/L CaCl2溶液,购买的感受态细胞,LB液体培养基,LB固体培养基,氨苄青霉素(Amp),X-gal,IPTG等。
2.3 实验方法
从大肠杆菌DH5α平板上挑取一个单菌落接于50ml LB液体培养基的试管中,37℃振荡培养过夜(16小时)。分别取2.0ml菌液转接到三个含有100ml LB液体培养基锥形瓶中, 37℃振荡培养2-3h。(此时,OD600<=0.5,细胞数务必<108/ ml,此为实验成功的关键)。将菌液转移到1.5 ml离心管中,冰上放置30min。在低温离心机中于4℃离心10min(4000rpm),回收细胞。倒出培养液,将管倒置1min以便培养液流尽。用冰冷的0.1mol/L CaCl2700μl悬浮沉淀,立即放在冰上保温30min。4℃ 4000rpm,离心10min,回收细胞。用冰冷的0.1mol/L CaCl2300μl悬浮细胞 (务必放冰上)。取200μl新鲜配制的感受态细胞和20μl已购买的感受态细胞,分别加入DNA 2μl(50ng)混匀,冰上放置30min。将管放到42℃恒温水浴1-2min(约90秒)。冰浴2min。每管加800μl LB液体培养基,置于恒温摇床于37℃培养1h(慢摇)。100 ml的琼脂培养基中,灭菌后冷却到60度左右,加入100 μl的IPTG溶液、200 μl的X-Gal和100 μl的Amp,制作成IPTG、X-Gal、Amp平板培养基。将适当体积已转化的感受态细胞,涂在含有X-gal 、IPTG及氨苄青霉素的LB固体培养基上。倒置平皿37℃培养12-16h,则出现菌落,观察并记录结果。
3 结果
两只培养皿经一天培养后,观察得到以下实验结果:自己配制的感受态细胞与质粒结合后经含有X-gal 、IPTG及氨苄青霉素的LB培养基培养24h,长出6个白色菌落,无蓝色菌落生长;购买的感受态细胞与质粒结合后经培养24h,长出8个白色菌落,无蓝色菌落生长。两板培养皿长出的菌落直径约1mm,呈白色,不透明,菌落突起,表面光滑湿润,边缘整齐。纵观两个平板上的菌落分布,都很均匀。
4 讨论
4.1 对实验结果的分析及结论
根据实验原理中阐述的蓝白菌落的形成原因,两个平板都只长出白色菌落而未长出蓝色菌落的结果表明:转化进大肠杆菌细胞内的质粒都是连接成功的质粒,也可以进一步说明连接那一步做得很成功。
自制的感受态细胞所得的那一板与购买的感受态细胞所得的那一板相比,菌落数较少。说明自制的感受态细胞有可能没有完全达到理想的感受态,导致进入的质粒偏少。两板平皿所得菌落分别是6、8,有些偏少,说明在转化的时候可能没有控制好条件致使有些质粒没有进入感受态细胞。
两板平皿菌落分布均匀说明菌液涂布得很均匀。
4.2 感受态细胞制备及转化中的影响因素
4.2.1 细胞的生长状态和密度
最好从-70℃甘油保存的菌种中直接转接用于制备感受态细胞的菌液。细胞生长密度以每毫升培养液中的细胞数在5×107个左右为佳。即应用对数期或对数生长前期的细菌,可通过测定培养液的OD600控制。
4.2.2 质粒DNA的质量和浓度
用于转化的质粒DNA主要是超螺旋态的,转化率与外源DNA的浓度在一定范围内成正比,但外源DNA的量过多时,则会使转化率下降。一般来说,DNA溶液的体积不应超过感受态细胞体积的5%,1ng的超螺旋DNA即可使50ul的感受态细胞达到饱和。对于以质粒为载体的重组分子而言,分子量大的转化效率低。此外,重组DNA分子的构型与转化效率也密切相关,环状重组质粒的转化率较分子量相同的线性重组质粒高10~100倍。
4.2.3 试剂的质量
化合物及无机离子的影响:所用的CaCl2等试剂均需是最高纯度的,并用最纯净的水配制,分装保存于4℃。在Ca2+的基础上联合其他二价金属离子(如Mn2+或Co2+)、DMSO或还原剂等物质处理细菌,可使转化效率大大提高。
4.2.4 防止杂菌和杂DNA的污染
整个操作过程均应在无菌条件下进行,所用器皿,如离心管、移液枪头等最好是新的,并经高压灭菌处理。所有的制剂都要灭菌,且注意防止被其它试剂、DNA酶或杂DNA所污染,否则均会影响转化效率或杂DNA的转入。
4.3 大肠杆菌感受态细胞其他的制备方法
除了本次实验用的氯化钙法之外,实验室常用的制备大肠杆菌感受态细胞的其他方法还有以下几种:
4.3.1 Glycerin-PEG(甘油-聚乙二醇法)
常规氯化钙法制备的感受态细胞维持其感受态时间往往较短,而甘油-聚乙二醇法较常规氯化钙法为优,转化结果显示:在-30℃条件下其感受态维持时间至少在180d以上。这可能与该细胞储存液中含有一定浓度的甘油和葡萄糖等保护剂有关。一般认为能保留少量水分的结晶化合物与一种胶态物质结合作为保护剂对菌体细胞长期储存的存活是必要的。此外,由于保护剂对菌体细胞和水均有很强的亲和力,故在复苏过程中它可代替结合水而稳定细胞构型。储存液中含有一定浓度镁离子和葡萄糖可以增强转化。此外,聚乙二醇为多糖类物质,这里可能有促使质粒DNA与感受态细胞膜结合的作用,与镁离子及葡萄糖共同促进质粒转化。
4.3.2 氯化铷法
氯化铷法也是实验室常用的一种感受态细胞制备方法,可用于不同的质粒的转化。此种方法对于同一种质粒,不同的菌种和冻存时间对转化效率无影响,其转化效率要高于氯化钙法,是一种可以长期保存而不影响转化效率的感受态细胞制备方法。
4.3.3 一步制备法
此种方法的特点是只加一种试剂即可,且不需要另加保护剂就可直接冻存,转化时不需要热激。但一步法对实验操作要求较高,如所用器具一定要清洁,OD600值不要高于0.6,制备感受态细胞时所有操作尽量保证在冰上操作等。其转化效率相对较低,适用于对转化率要求不高的实验[3]。
4.4 注意事项
实验中凡涉及溶液的移取、分装等需敞开实验器皿的操作,均应在无菌超净台中进行,以防污染。
衡量受体菌生长情况的OD600值和细胞数之间的关系随菌株的不同而不同,因此,不同菌株的合适OD600值是不同的。
悬浮菌体时不要剧烈推打枪头,要轻轻的悬浮菌体。
5 参考文献
[1]李芳,墙克信,王玉炯.大肠杆菌感受态细胞制备方法及应用的研究进展[J].宁夏医学院学报,2003,25(5):372-374.
[2]分子生物学实验指导.大肠杆菌感受态细胞的制备.
[3]房功思.浅谈大肠杆菌感受态细胞的几种制备方法[J].安徽卫生职业技术学院学报,2008,7(2):96-97.
第二篇:大肠杆菌感受态细胞的制备原理、步骤以及重组质粒转化
大肠杆菌感受态细胞的制备原理、步骤以及重组质粒转化
一、 目的
1.了解感受态细胞生理特性及制备条件,掌握大肠杆菌感受态细胞制备方法。
2.掌握质粒DNA 转化大肠杆菌的方法,了解转化的条件和利用半乳糖苷酶基因插入失活选择重组质粒DNA 的原理。
二、原理
(一)大肠杆菌感受态细胞制备的原理
所谓感受态,是指细菌生长过程中的某一阶段的培养物,只有某一生长阶段中的细菌才能作为转化的受体,能接受外源DNA而不将其降解的生理状态。感受态形成后,细胞生理状态会发生改变,出现各种蛋白质和酶,负责供体DNA 的结合和加工等。细胞表面正电荷增加,通透性增加,形成能接受外来的DNA 分子的受体位点等。本实验为了把外源DNA(重组质粒)引入大肠杆菌,就必须先制备能吸收外来DNA分子
的感受态细胞。在细菌中,能发生感受态细胞是占极少数。而且,细菌的感受态是在短暂时间内发生。
目前对感受态细胞能接受外来DNA 分子的本质看法不一。主要有两种假说:
1、局部原生质体化假说――细胞表面的细胞壁结构发生变化,即局部失去细胞壁或局部溶解细胞壁,使DNA 分子能通过质膜进细胞。证据有:
(1)发芽的芽孢杆菌容易转化;
(2)大肠杆菌的原生质体不能被噬菌体感染,却能受噬菌体DNA 转化;
(3)适量的溶菌酶能提高转化率。
2、酶受体假说――感受态细胞的表面形成一种能接受DNA 的酶 位点,使DNA分子能进入细胞。证据是:(1)蛋白质合成的抑制剂如氯霉素,可以抑制转化作用;
(2)细胞分裂过程中,一直有局部原生质化,但感受态只在生长对数期的中早期出现;
(3)分离到感受态因子,能使非感受态细胞转变为感受细胞。
目前对感受态细胞的转化理论尚未有统一结论,但是许多实验室一直进行探索,试图从实验中获得明确回答。有人根据pBR322 质粒DNA对E?coli K――12X1776菌株的转化结果,认为:
近来,在许多研究室都发现CaCl2对受体菌处理,可提高转化效率几十倍,通常把细胞悬浮在pH6.0 的100mmol/L CaCl2中,在冰浴条件下,放置过夜,转化率转高,但一过24小时,转化率测恢复为原来的水平。
(二)重组DNA 的转化原理
我们已经制备好大肠杆菌感受态细胞,接下的实验是把重组的DNA 引入受体细胞,使受体菌具有新的遗传特性,并从中选出转化子。作为受体的大肠杆菌C600 或DH5α,必须不同外来DNA分子发生遗传重组,通常是rec基因缺陷型的突变体,同时它们必须是限制系统缺陷或限制与修饰系统均缺陷的菌株。这样外来的DNA分子不会受其限制酶的降解。保持外来DNA分子在受体细胞中的稳定性。制备的大肠杆菌细胞就具有这三种缺陷(rk- mk- rec- )同时此受体细胞还是氨苄青霉素敏感(Ap)。
在体外构建好的重组分子上具有分解氨苄青霉素(Ap)基因存在,当它导入受体细胞后,就赋于这些受体细胞新的特性,即Ap 抗性。同时载体质粒上具有乳糖操纵的β一半乳糖苷酶基因(lacZ),我们可以利用外源基因插入载体β一半乳糖苷酶基因(lacZ),使其失去β一半乳糖苷酶活性的原理来选择新构建的重组子。
因pUC18带有Ampr 基因而外源片段上不带该基因,故转化受体菌后只有带有pUC18 DNA的转化子才能在含有Amp的LB平板上存活下来;而只带有自身环化的外源片段的转化子则不能
存活。此为初步的抗性筛选。
pUC18 上带有β-半乳糖苷酶基因(lacZ)的调控序列和β-半乳糖苷酶N 端146 个氨基酸的编码序列。这个编码区中插入了一个多克隆位点,但并没有破坏lacZ 的阅读框架,不影响其正常功能。E.coli DH5α菌株带有β-半乳糖苷酶C 端部分序列的编码信息。在各自独立的情况下,pUC18 和DH5α编码的β-半乳糖苷酶的片段都没有酶活性。但在pUC18 和DH5α融为一体时可形成具有酶活性的蛋白质。这种lacZ 基因上缺失近操纵基因区段的突变体与带有完整的近操纵基因区段的β-半乳糖苷酸阴性突变体之间实现互补的现象叫α-互补。
由α-互补产生的Lac 细菌较易识别,它在生色底物X-gal(5-溴-4 氯-3-吲哚-β-D-半乳糖苷)存在下被IPTG(异丙基硫代-β-D-半乳糖苷)诱导形成蓝色菌落。当外源片段TGFβⅠ插入到pUC18 质粒的多克隆位点上后会导致读码框架改变,表达蛋白失活,产生的氨基酸片段失去α-互补能力,因此在同样条件下含重组质粒的转化子在生色诱导培养基上只能形成白色菌落。由此可将重组质粒与自身环化的载体DNA 分开。此为α-互补现象筛选。
本实验是把外来重组分子和感受态细胞在低温下混合,使其进入受体细胞。DNA分子转化的原理较复杂:
1、吸附――完整的双链DNA 分子吸附在受体菌表面。
2、转入――双链DNA 分子解链,单链DNA 分子进入受体菌,另一链降解。
3、自稳――外源质粒DNA 分子在细胞内又复制成双链环状DNA。
4、表达――供体基因随同复制子同时复制,并被转录和翻译
5.无菌条件下将上述1 毫升菌液倒入1.5毫升EP 离心管中(离心管应带盖并高压灭菌过),每组2 支。
6、带菌液的离心管置于冰上10 分钟,冷却菌液,平衡好,置于台式低速离心机上,3500r/min 离心5 分钟。
7、无菌条件下,倒去上清LB,倒斜离心管,让LB 流干,留下沉淀菌体,加入预冷的100mmol/L CaCl2溶液600微升,用微量取样器轻轻吸冲底部沉淀菌体,使其悬浮后,把2支管转为1支,摇匀后于冰浴中放置30分钟。
8、重新将CaCl2 菌悬浮液置于台式低速离心机上,3500r/min离心10分钟,小心侧倒掉上清CaCl2 ,留沉淀菌体。
9、再把菌体悬浮在200 微升100mmol/L CaCl2 的溶液中,置于冰上作为转化的受体菌液。此制备的感受态细胞应在此步后1小时至24小时内使用,效率比较高。
10.在事先制备好的含50μg/ml Amp的LB 平板表面加40ml X-gal 储液和4μlIPTG储液,用无菌玻棒将溶液涂匀,置于37℃下放置3-4小时,使培养基表面的液体完全被吸收,备用。
(二)重组DNA 转化
1.取0.2ml 大肠杆菌感受态细胞,在无菌条件下,加入到连接液的Eppendorf管,混匀,置冰浴中30 分钟。
2.冰浴后,将正在转化反应的细胞悬浮液加入已调好42℃的的恒温水浴槽内,保温2分种。
3.热冲击处理后的细胞易死亡,应迅速倒入LB培养液1 毫升,(无抗菌素LB 液,有助于基因表达)马上置37℃水浴1 小时,每10 分钟翻转1 次。
4.用移液器取0.1 毫升的转化菌液直接涂布含50μg/ml Amp、40ml X-gal储液和4μlIPTG 储液LB 固体平皿上,共涂布三个培养皿。
5.用移液器取未经转化的受体大肠杆菌感受态菌液0.1毫升直接涂布于含50μg/mlAmp、40ml X-gal 储液和4μlIPTG 储液LB 固体平皿上,作为受体菌对照。
6.将第14、15 步涂布培养皿先放室温15 分钟左右,使涂布上的菌液干燥不会流动。然后倒置放于恒温箱中37℃培养过夜。
7.第二天取出培养皿,观察对照平皿和转化平皿菌落情况。对照平皿因受体菌对Amp 敏感,故不能在含Amp的培养基上生长。转化平皿是否有兰色和白色菌落生成?如果长出兰色菌落,说明自连的载体pUC18质粒
已转入受体菌,但目的基因没有接入载体。如果长出白色菌落,说明目的基因已接入载体,重组质粒的转化子因此丧失了β-半乳糖苷酶活性,在x-gal 和ITPG 存在的生色诱导培养基上只能形成白色菌落。
五、结果和讨论
比较对照平皿和转化平皿,讨论转化成败原因.
