实验七 溶液表面张力的测定——最大气泡压力法
一. 实验目的
1. 用最大气泡法测定不同浓度乙醇溶液的表面张力。
2. 了解表面张力的性质,表面自由能的意义以及表面张力和吸附的关系。
3. 学会镜面法作切线的方法。
二. 实验原理
1. 用本法测定[乙醇,水]溶液的数据对[σ,c],作图将c-σ曲线在不同浓度的斜率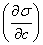 T代入吉布斯等温吸附式:
T代入吉布斯等温吸附式:
Γ=﹣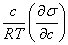 T
T
求出相应的吉布斯吸附量Γ;
按朗格茂尔等温吸附变形公式:
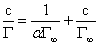
C/Γc-C直线斜率tgβ求出饱和吸附量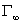 ,进而得出乙醇分子横切面积S和分子长度
,进而得出乙醇分子横切面积S和分子长度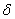 ,结合直线截距得出吸附系数α:
,结合直线截距得出吸附系数α:
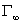 =(tgβ)-1
=(tgβ)-1
以上个式中,c为浓度;T为绝对温度(K);σ为表面张力;Γ为吉布斯吸附量;M为溶质摩尔质量;ρ为溶质密度;S为分子截面积;δ为分子长;α为吸附系数;NA为阿伏伽德罗数(6.02×1023/mol);R为气体常数。为了求以上参数,关键是测σ。
2. 表面张力及界面张力 ,矢量。源于凝聚相界面分子受力不平衡,意为表面的单位长度收缩力。σ也是在个条件下凝聚系表面相得热力学强度性质,如果恒温 、恒压下扩大单位表面积所需的可逆功,故亦称为表面自由焓。
σ与凝聚相和表面共存接触相种类有关,还与T,P有关,与凝聚相纯度和杂志种类有关。浓度升高,溶液的σ有增有减,随溶质、溶剂而异,表面活性剂是两亲分子,他们的水溶液σ随浓度升高先剧降,后微升,在渐趋稳定。σ随c而变化的本质是溶液表面浓度对体相浓度的偏离,此现象称为表面吸附。表面吸附量Γ与浓度有关,用吉布斯等温方程求出 为σ-c曲线在指定浓度的斜率。
为σ-c曲线在指定浓度的斜率。 <0, Γ>0为正吸附,表面浓度较体浓度高,达饱和吸附时,Γ趋于饱和吸附量
<0, Γ>0为正吸附,表面浓度较体浓度高,达饱和吸附时,Γ趋于饱和吸附量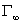 ,此时两亲分子在溶液表面处于高度有序的竖立密集,形成单分子膜。,
,此时两亲分子在溶液表面处于高度有序的竖立密集,形成单分子膜。,
若将兰格缪尔等温吸附式中的吸附量赋予吉布斯吸附量的特定意义,则可从其变形式求出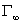 设分子吸附层厚δ,δ即两亲分子长。依δ*ρ=
设分子吸附层厚δ,δ即两亲分子长。依δ*ρ=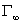 *M,由此得出求分子的式子。
*M,由此得出求分子的式子。
3. δ的测定方法有环法、滴重法、毛细管上升法等, 其中最大气泡法设备简单,易操作,应用广。此法是将下口齐平的毛细管垂直插入试液,并使管口刚与液面相切,则可看到在毛细管内形成凹液面。凹液面受力一是大气压,二是附加压力,因此凹液面受到的总压是p1=p0+△p=p0+2σ/r.
现对管外减压,随管外压力p2=p0+ρg△h减小,|△h|增大,|r|减小,p1随p2同步减小,故p2=p1,得:
σ=rgρ△h/2
由于减压凹液面不断下降,r为不定值,但当凹液面上形成的小气泡降至毛细管下口,并随时气流的瞬间,|r|降至极小,刚等于毛细管下口内径,此时△h 升至最大。若在微微减压。气泡逸出,△h剧降,r为定值,所以只要测出最大的|△h|,即可用上式求出σ。由于r一定。故rgρ/2为定值,称仪器常数K,可用纯水的σ和同条件下实验测得的△h求出。故:
σ=K*△h=σ0*△h/△h0
溶液浓度c用折射仪测出。
四.仪器与药品
仪器: 蓄水瓶,毛细管,试管,烧杯,U型水柱压力计,温度计,分液漏斗表面张力仪一套
药品:乙醇溶液:5%,10%,20%,30%,40%,50%
五.实验步骤
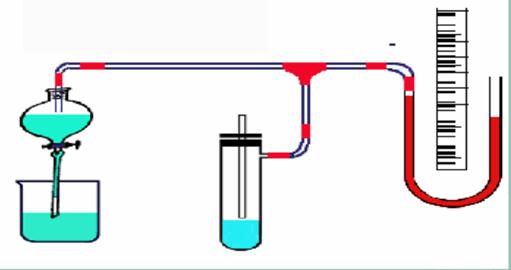
1.按下图安装好实验仪器,检查仪器是否漏气,检查方法如下:由分液往
蓄水瓶中注水,是压力计产生一定的压力差,停止加水,如果压力计维持3~5
分钟不变,可认为不漏气。
2.仔细用热的铬酸洗液洗涤毛细管。
3.毛细管常数的测定:
在清洁的试管中加入约1/4体积的蒸馏水,装上清洁的毛细管,是端面
恰好与液面相接,打开分液漏斗,使水缓缓滴出,以增加毛细管内压力,使气泡
冒出,观察冒出的速度与压力的关系,调节气泡逸出速度不超过每分钟20个,
如此三次,若每次得△h,差别在2mm以内,取平均值,求K。否则重复步骤2,
然后再测。
4.乙醇溶液表面张力的测定:
将试管中的水倒出,用待测溶液洗涤试管和沾洗毛细管(尖端沾取待测
液,然后用耳洗球吹掉内溶液)3次,在试管中装入待测溶液,用上述方法快速
测定浓度为5%,10%,20%,30%,40%,50%的乙醇溶液压力差△h,都测三次取平均
值。
六.数据处理和结果
原始数据表
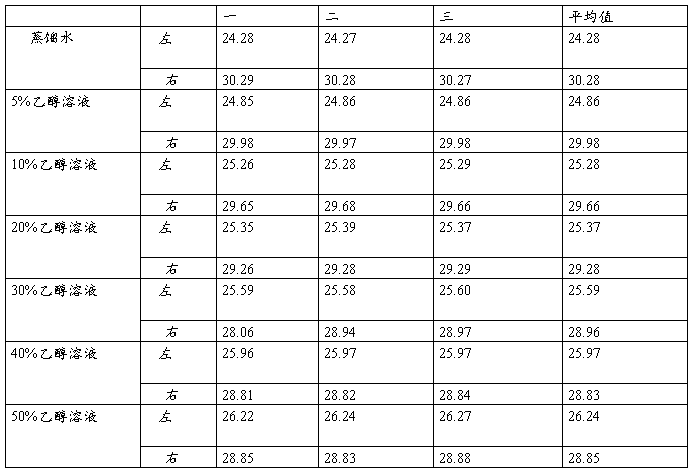
1.将实验记录的数据用表格列出

2.利用水的表面张力球毛细管常数k。
由上表知蒸馏水:△h=6.00cm 查表得:б水=73.078×10-3N/m
所以: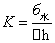 =
= ×10-3=1.218N/m2
×10-3=1.218N/m2
3.计算各浓度乙醇溶液的表面张力。
计算举例:5%的乙醇溶液
б=K×△h=1.218×0.0512=62.36×10-3N/m
其余结果见上表。
4. 作σ-c图。
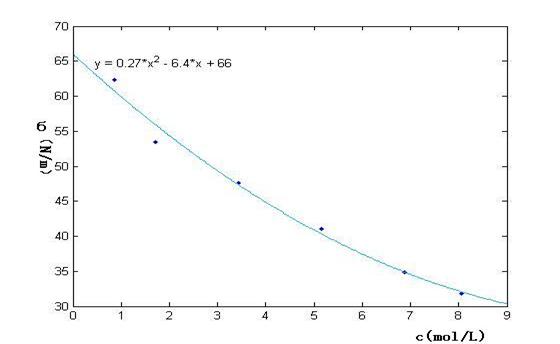
对上曲线方程求导得:y=0.54×10-3x-6.4×10-3
所以:5%的乙醇溶液 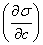 T=0.00054×0.8601-0.0064=--5.9355×10-3
T=0.00054×0.8601-0.0064=--5.9355×10-3
同理得:10%的乙醇溶液 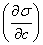 T=-5.4711
T=-5.4711
20 %的乙醇溶液 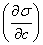 T=-4.5421
T=-4.5421
30%的乙醇溶液 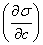 T=-3.6132
T=-3.6132
40%的乙醇溶液 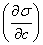 T=-2.6843
T=-2.6843
50%的乙醇溶液 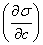 T=-2.0470
T=-2.0470
5计算各浓度的Γ和C/Γ。
计算举例:5%的乙醇溶液
Γ=﹣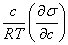 T=
T=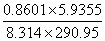 ×10-3=2.1105×10-6mol/ m2
×10-3=2.1105×10-6mol/ m2
C/Γ=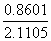 ×10-6=0.4075×10-6
×10-6=0.4075×10-6
其余结果见上表。
5. 作C/Γ—C图,求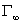
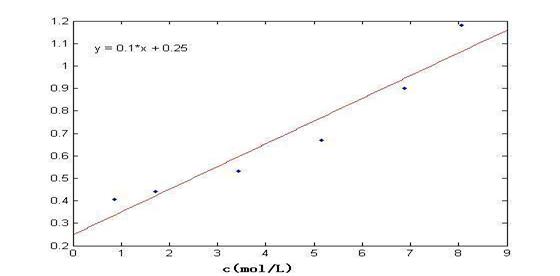
由图知直线的斜率为:tgβ=0.1×106
所以 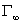 =(tgβ)-1=
=(tgβ)-1=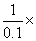 10-6=1.0×10-5
10-6=1.0×10-5
七.思考题
1为什么液体的表面张力随温度升高而减小?
答:同一种物质的表面张力因温度不同而异,当温度升高时物质的体积膨胀,分子间的距离增加,分子之间的相互作用减弱,所以表面张力一般随温度的升高而减小。
2仪器的清洁与否对所测数据有无影响?
答:有影响。毛细管如果不清洁会影响气泡逸出的速度。
八.误差分析
1.实验装置气密性不好,影响压差计的读数。
2.毛细管没有用热的铬酸洗涤干净,这是实验的关键。
3.没有调节好气泡逸出的速度,气泡逸出速度太快每分钟超过30个,气泡逸出速度不均匀。
4.一次测量后没有用待测液洗试管和沾洗毛细管。
5.实验温度,溶液浓度对实验结果的影响。
九.心得体会
本实验是第一次没有老师讲解,自己和同组同学独立完成的物理化学实验,也是最后一次物理化学实验。通过一年的物理化学实验,了解了许多的物理化学原理、想象,懂得了物理化学实验的基本操作和应注意的问题,实验时科学严谨的态度,更重要的是学会了用计算机处理实验结果。这些将会对我经后的学习和工作有很大的帮助。
第二篇:溶液表面张力测定实验报告
学号:201114120222

基础物理化学实验报告
实验名称:溶液表面张力的测定
应用化学二班 班级 03 组号
实验人姓名: xx
同组人姓名:xxxx
指导老师: 杨余芳老师
实验日期: 20##-11-12
湘南学院化学与生命科学系
一、实验目的
1、测定不同浓度正丁醇(乙醇)水溶液的表面张力;
2、了解表面张力的性质,表面自由能的意义及表面张力和吸附的关系;
3、由表面张力—浓度曲线(σ—c曲线)求界面上吸附量和正丁醇分子的横截面积S;
4、掌握最大气泡法测定表面张力的原理和技术。
二、实验原理
测定液体表面张力的方法很多,如毛细管升高法、滴重法、环法、滴外形法等等。本实验采用最大泡压法,实验装置如图一所示。
图一中A为充满水的抽气瓶;B为直径为0.2~0.3mm的毛细管;C为样品管;D为U型压力计,内装水以测压差;E为放空管;F为恒温槽。
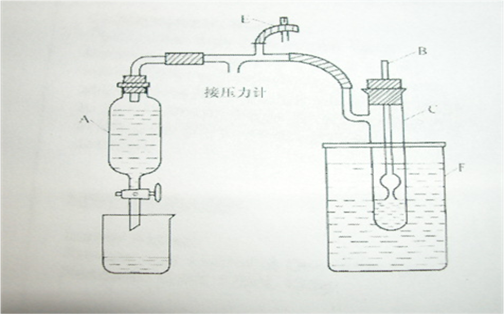
图一 最大泡压法测液体表面张力仪器装置图
将毛细管竖直放置,使滴口瓶面与液面相切,液体即沿毛细管上升,打开抽气瓶的活栓,让水缓缓滴下,使样品管中液面上的压力渐小于毛细管内液体上的压力(即室压),毛细管内外液面形成一压差,此时毛细管内气体将液体压出,在管口形成气泡并逐渐胀大,当压力差在毛细管口所产生的作用力稍大于毛细管口液体的表面张力时,气泡破裂,压差的最大值可由U型压力计上读出。
若毛细管的半径为r,气泡从毛细管出来时受到向下的压力为:
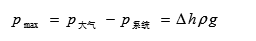
式中,△h为U型压力计所示最大液柱高度差,g为重力加速度,ρ为压力计所贮液体的密度。
气泡在毛细管口所受到的由表面张力引起的作用力为2πr?γ,气泡刚脱离管口时,上述二力相等:
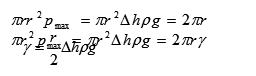
若将表面张力分别为和的两种液体用同一支毛细管和压力计用上法测出各自的和,则有如下关系:


即:
对同一支毛细管来说,K值为一常数,其值可借一表面张力已知的液体标定。本实验用纯水作为基准物质,20.0℃时纯水的表面张力为7.275×10-2N/m(或J/m2)。
三、实验仪器及试剂
表面张力测定装置(包括恒温槽)1套;容量瓶100ml1个,50ml5个;1ml刻度移液管1支;吸耳球1个;正丁醇(二级);去离子水。
四、简述实验步骤和条件
1、分别配制浓度为0.050、0.100、0.200、0.300、0.400、0.500、0.600、0.700mol/L的正丁醇溶液100mL。
2、将仪器仔细洗涤干净,调节恒温槽温度为25℃。
3、样品管中装入蒸馏水,使液面与毛细管端面向切,注意保持毛细管与液面垂直。
4、打开抽气瓶活塞,让水缓慢流下,使毛细管中气泡逸出速度为5—10秒/个。
5、纪录压力计最大值,重复二次,求出P最大1平均值。
6、同法测定各浓度下正丁醇水溶液的P最大2值。
五、实验数据及现象的原始记录
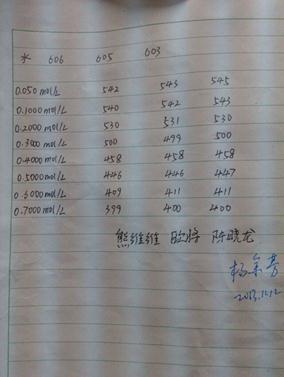
温度: 25℃ 水的表面张力:0.07197N/m 仪器常数K:0.1190
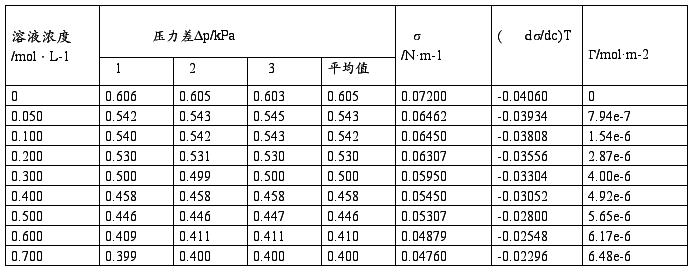
(1)查出实验温度下水的表面张力,计算仪器常数K。
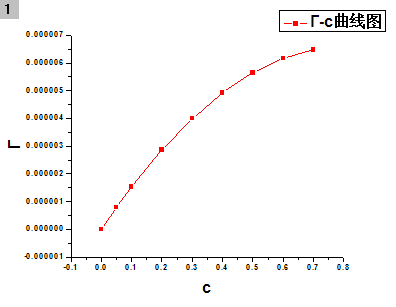
(2)计算系列正丁醇溶液的表面张力,根据上述计算结果,绘制σ—c等温线。
Γ=-(c/RT)*( dσ/dc)

(3) 求导得到dσ/dc代入吉布斯方程可计算溶液表面吸附量Γ;
y=ax2+bx+c
a=0.0126 b=-0.0406 c=0.0695
dσ/dc= dy/dx=ax+b=0.0252x-0.0406
Γ=-(c/RT)*( dσ/dc)
(4)再利用计算机作Γ~c图,c/Γ~c图,并运用c/Γ~c图拟合直线方程,由直线斜率可得饱和吸附量Γ∞= 1/A.计算出横截面积 A:
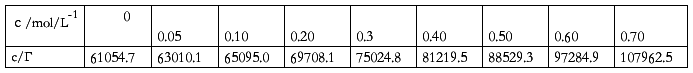
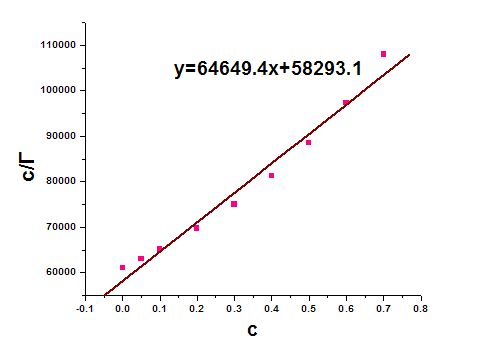
Γ∞= 1/64649.4mol*m-2=1.55e-5 mol*m-2
Am=1/(NA*Γ∞)= 1.07e-19m2
六、 结果与讨论
1、 毛细管尖端为何必须调节地恰好与液面相切?
答:如果毛细管尖端插入液下,会造成压力不只是液体表面的张力,还有插入部分液体的压力。
2、 本实验结果准确与否关键决定哪些因素?
答:本实验结果准确的关键在于仪器必须洗涤清洁,毛细管应保垂直,其端部应保持平整,溶液恒温后,体积略有改变,应注意毛细管平面与液面接触处要相切。控制好出泡速度、平稳地重复出现压力差。
