漂白粉中有效氯和固体总钙含量的测定
作者:高分子09-1 莫谋劲 30号
摘要:本实验中主要采用碘量法测定漂白粉中有效氯,用络合滴定法测定固体总钙。
关键词:漂白粉 有效氯 固体总钙含量 测定
前言:
漂白粉的有效成分Ca(OCl)2,其中有效氯和固体总钙含量是影响产品质量的两个关
键指标,它质量的好坏是根据它的有效氯和总钙量以及它能在长时期保持有效氯的能力来决定的。所以实际当中漂白粉有效氯和固体总钙含量的测定是很重要的。
一、实验原理
1、碘量法测定有效氯的原理:
- - 利用 I 其中用 I 与2 的氧化性和 I 的还原性进行滴定分析的方法称为碘量法。
氧化剂作用生成 I 2 ,再用 Na2S2O3 标准溶液滴定所生成的 I2 ,从而间接测定氧化性物质的方法称为间接碘量法。
+ 2- Ca(C1O)Cl + H= Ca+ Cl2 ↑ +H2O
C12 + 2KI = 2KCl + I2
I2 +2Na2S2O3 = Na2S4O6 + 2NaI
2、络合滴定法测定固体总钙:
在PH ≥12 的溶液中,以钙指示剂作指示剂用EDTA 标准溶液滴定。钙指示剂(常以H3 Ind 表示) 在水溶液中按下式解离:
H3 Ind 2H+ + HInd2-
HInd2 - 与Ca2 + 形成比较稳定的配离子,其反应为:
HInd2 - + Ca2 +CaInd - + H+
(纯蓝色) (红色)
当用EDTA 溶液滴定时,由于EDTA 能与Ca2 + 形成比CaInd - 更稳定的配离子其反应如下:
CaInd - + H2 Y2 - + OH-CaY2 - + HInd2 - + H2O
(红色) (无色) (纯蓝色)
二、实验仪器与试剂
分析天平,称量瓶,烧杯, 250mL 容量瓶,100ml容量瓶, 50mL 带塞锥形瓶, 10mL 量简,棕色试剂瓶, 5mL 吸量管,滴定管,多用滴管,20 % KI , 1 %淀粉溶液,盐酸(6 mol/L),KBrO3‘ Na2S2O3·5H2O( c=0.02082mol/L) ,漂白粉,EDTA(c= 0.06324 mol/L)、质量分数为10 %的NaOH 溶液、碘量瓶等
三、实验步骤
1、Na2S2O3溶液和EDTA的配制与标定
用分析天平称取Na2S2O3·5H2O3.2g 左右和 0.2g左右的Na2S2O3溶于400mL 新煮沸过冷却的蒸馏水中。转入500mL棕色溶量瓶中,稀释至标线,摇匀。放置于避光处 7 ~ 10 天后标定。
在分析天平上称取 0.27g 左右的 KBrO3 ,置于250mL 烧杯中,加入约40mL 蒸馏水溶解,转入100m L 容量瓶中,用少量蒸馏水洗涤烧杯三次,洗液全部转入容量瓶中。
加水至刻度线,摇匀。计算此KBrO3 标准溶液的浓度。
移取KBrO3 标准溶液 20.00mL ,放入洁净的 250mL 碘量瓶中,依次加入 20%KI 溶液 10mL 和 3mol/L H2SO410mL ,加盖摇匀后置于暗处放 5min 。加 150mL 蒸馏水,用Na2S2O3待标定的溶液滴定。接近终点时(溶液由深褐色变为浅黄色),加入淀粉指示剂 5mL ,溶液变蓝,继续滴定至溶液由蓝色刚好褪去即为终点,记下所用Na2S2O3溶液的体积,平行测定三次。计算Na2S2O3溶液的浓度。
称取乙二胺四乙酸二钠(A.R.)12.35g溶于200ml温水中,冷却后稀释至0.5l,摇匀,如浑浊应过滤后使用,并贮存于500ml试剂瓶中
o钙标准溶液的配制 准确称取120C干燥过的CaCO31.0-2.0g于150ml烧杯中,加少
量水湿润,盖上表面皿,从烧杯嘴滴加2︵3mlHCL,待CaCO3完全溶解后,加热近沸,冷却后淋洗表面皿,再定量转入250ml容量瓶中,稀释定容,摇匀
EDTA的标定 用移液管移取25.00ml钙标准于250ml锥形瓶中,加水25ml,镁溶液2ml,10﹪NaOH溶液5ml及少量钙指示剂,摇匀后用EDTA标准溶液滴至由酒红色恰变为纯蓝色即为终点。平行实验三次,计算EDTA浓度。
二、有效氯的测定
用电子天平称取基本相同的0.13g-0.15g漂白粉于碘量瓶中,加入约少量蒸馏水溶解,然后加入5mLKI 溶液,接着加入2到3滴管盐酸放于暗处5 分钟后,然后用40mL水稀释,并迅速用Na2 S2O3 溶液滴定至溶液呈浅黄色,加入1mL 淀粉溶液,继续滴定溶液蓝色消失即为终点,平行测定3次,
w(Cl)?CV?10?3?MCl
式中:C 为Na2S2O3 溶液的物质的量浓度(mol/L) ;V 为Na2S2O3 溶液的体积(mL) ;MCl为氯的相对原子质量;m为漂白粉的质量(g)。
三、固体总钙量的测定
在上述滴定后的碘量瓶中,为使滴定终点更敏锐,通常加入1mL 镁溶液。然后加约10%NaOH 10ml 溶液,加入约10 滴钙指示剂,摇匀后,用EDTA 溶液滴定至由红色变为纯蓝色,即为终点。平行测定3 次。
w(Ca)?CV?10?3m?100% ?MCa
m?100%
式中:C 为EDTA 的浓度;V 为EDTA 溶液的体积;MCa 为钙的相对原子质量;m 为漂白粉的质量。
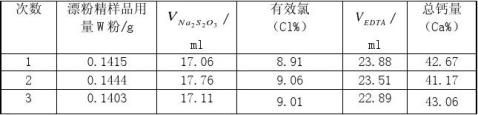
Cl=(8.91%+9.06%+9.01%)/3=8.99%
偏差:
d1?wCl?Cl=| 8.91%-8.99%|=0.08%
d2?wCl?Cl
d3?wCl?Cl=| 9.06%-8.99%|=0.07% =| 9.01%-8.99%|=0.02%
相对偏差:
dr1?wCl?Cl?Cl?100%=0.9%
dr2?wCl?Cl?Cl?100%=0.8%
dr3?wCl?Cl?Cl?100%=0.2% Ca=(42.67%+41.17%+43.06%)/3=42.3%
偏差:
d4?wCa?Ca
d5?wCa?Ca
d6?wCa?Ca=| 42.67%-42.3%|=0.37% =| 41.17%-42.3%|=1.13% =| 43.06%-42.3%|=0.76%
=0.9%
=2.7%
=1.8% 相对偏差: dr4?wCa?Ca?Ca?100%dr5?wCa?Ca?Ca?100%
dr6?wCa?Ca?Ca?100%
结果与讨论
1、误差分析:
①固体未完全溶解
②滴定终点判断不准确
③主观读数误差
2、总结实验成败的关键
①这个实验的关键是滴定,滴定时要有耐心,先快后慢。
②称量漂白粉用同一瓶,可以很大程度的是结果的误差减少。
参考文献
【1】 古风才、肖衍繁.基础化学实验教程【M】北京:科学出版社.2000
【2】 傅洵、许泳吉、解从霞.基础化学教程(无机与分析化学),北就:科学出版社,2007.5
第二篇:漂白粉中有效氯的测定方法