蟾蜍坐骨神经腓肠肌标本制备和
不同强度和频率对肌肉收缩的影响
一、实验摘要
1. 目的:掌握制备具有正常兴奋收缩功能的蛙类坐骨神经腓肠肌标本基本操作以及蛙类手术器械的使用方法。学习微机生物信号采集处理系统和换能器的使用。记录在刺激时间、强度变化率恒定的条件下,不同强度和频率的电刺激对肌肉收缩的影响。
2. 方法:应用蛙类捉拿方法并且毁脑脊髓后制备坐骨神经-腓肠肌标本,用锌铜弓分别刺激坐骨神经和腓肠肌,观察肌肉变化。再利用张力换能器将压力变化转换为电信号,用微机生物信号采集处理系统记录不同强度和频率对肌肉收缩的影响的变化曲线。
3. 结果:用锌铜弓刺激坐骨神经时腓肠肌发生收缩。在保持足够的刺激时间(脉冲波宽)不变的条件下,通过逐步增加对蟾蜍坐骨神经的刺激强度(脉冲振幅)和改变电脉冲刺激频率可发现当电压低于阈值的强度刺激,坐骨神经支配腓肠肌的神经纤维不发生兴奋,刺激电压达到阈强度时,坐骨神经干中阈值最低的神经开始兴奋。刺激强度逐渐增大,总收缩张力增加。当刺激电压达到使支配腓肠肌的神经纤维全部兴奋,则收缩张力达单收缩最大值。
4. 结论:在一定刺激时间下,刚能引起组织发生兴奋的刺激称为阈刺激,所达到的强度为阈强度;能引起组织发生最大兴奋的最小刺激称为最大刺激,相应的刺激强度叫最大刺激强度。介于阈刺激和最大刺激间的刺激称阈上刺激,相应的刺激强度称为阈上刺激强度。
二、关键词:坐骨神经、腓肠肌、兴奋性、阈值
三、引言:刺激神经使神经细胞产生兴奋,兴奋沿神经纤维传导,通过神经 肌接头的化学传递,使肌肉终板膜上产生终板电极,终板电极可引起肌肉产生兴奋(即动作电位),传遍整个肌肉纤维,再通过兴奋-收缩耦联使肌纤维中粗、细肌丝产生相对滑动,宏观上表现为肌肉收缩。[1]
四、材料和方法
1. 实验对象:蟾蜍
2. 实验仪器:张力换能器、微机生物信号采集处理系统、剪刀、铁碗、培养皿、锌铜弓、玻璃分针、大头针、蛙板、尖头镊子、棉线、针形引导电极
3. 实验药品和试剂:任氏液
4. 实验方法:
1) 观察蟾蜍毁脑脊髓前后四肢肌张力的变化。用锌铜弓分别刺激坐骨神经和腓肠肌,观察肌肉的反应。
2) 毁脑脊髓 取蟾蜍一只,用左手握住,以食指压其头部前端使其尽量前俯,右手持探针自枕骨大孔处垂直刺入,到达椎管,即将探针改变方向刺入颅腔,向各侧不断搅动,彻底捣毁脑组织;再将探针原路退出,刺向尾侧,捻动探针使逐渐刺入整个椎管内,捣毁脊髓。此时蟾蜍下颌呼吸运动应消失,四肢松软,即成为一毁脑脊髓的蟾蜍。否则须按上法再行捣毁。
3) 剪除躯干上部及内脏 用粗剪刀在颅骨后方剪断脊柱。左手握住蟾蜍脊柱,右手将粗剪刀沿两侧(避开坐骨神经)剪开腹壁。此时躯干上部及内脏即全部下垂。剪除全部躯干上部及内脏组织,弃于瓷盆内。
4) 剥皮 避开神经,用右手拇指和食指夹住脊柱,左手捏住皮肤边缘,逐步向下牵拉剥离皮肤。拉至大腿时,如阻力较大,可先剥下一侧,再剥另一侧。将全部皮肤剥除后,将标本置于盛有任氏液的培养皿中。
5) 洗净双手和用过的全部手术器械,再进行下列步骤。
6) 分离双腿 避开坐骨神经,用粗剪刀从背侧剪去骶骨,然后沿中线将脊柱剪成左右两半,再从耻骨联合中央剪开(为保证两侧坐骨神经完整,应避免剪时偏向一侧)。将已分离的标本浸入盛有任氏液的培养皿中。
7) 游离坐骨神经 取腿一条,先用剥离分针沿脊柱侧游离坐骨神经腹腔部,然后用大头针将标本背位固定于干净蛙板上。用玻璃分针循股二头肌和半膜肌之间的坐骨神经沟,纵向分离暴露坐骨神经之大腿部分,直至分离至腘窝颈神经分叉处。然后剪断股二头肌腱、半膜肌和半膜肌肌腱,并绕至前方剪断股四头肌腱。自上向下剪断所以坐骨神经分支。将连着3-4节椎骨的坐骨神经分离出来。
8) 完成坐骨神经小腿标本 将已游离的坐骨神经搭在腓肠肌上。用粗剪刀自膝关节周围向上剪除并刮净所以大腿肌肉,在距膝关节约1cm处剪断股骨。弃去上段股骨,保留部分即为坐骨神经小腿标本。
9) 完成坐骨神经腓肠肌标本 用尖子镊子在上述坐骨神经腓肠肌标本的跟腱下方穿孔,穿线结扎之。提起结扎线,在结扎线下方剪断跟腱,并逐步游离腓肠肌至膝关节处,左手握住标本的股骨部分,使已游离的坐骨神经和腓肠肌下垂,右手持粗剪刀水平方向伸进腓肠肌与小腿之间,在膝关节处剪断,与小腿其余部分分离。左手保留部分即为附着于股骨之上的、具有坐骨神经支配的腓肠肌标本。将标本浸入盛有新鲜任氏液的培养皿中待用。
10) 实验系统连接和参数设置 张力换能器的输出端与生物信号采集处理系统的输入通道相连。启动RM6240系统软件,在系统软件窗口设置仪器参数:点击“实验”菜单,选择“刺激强度(或频率)对骨骼肌收缩的影响”项。参数:通道模式为张力,采样频率400 Hz~1 kHz,扫描速度1 s/div,灵敏度10~30 g,时间常数为直流,滤波频率100 Hz。在“选择”下拉菜单中选择“强度/频率”项,显示刺激参数。
11) 将离体蟾蜍坐骨神经腓肠肌标本固定在屏蔽盒中,腓肠肌跟腱的扎线固定在张力换能器的悬臂梁上。坐骨神经放在刺激电极和引导电极上,保持神经与电极接触良好。针形引导电极插入腓肠肌并固定。
12) 观察实验现象 设定在刺激时间、强度变化率恒定,且强度和频率初始条件均为零的条件下,采集不同强度和频率的电刺激对肌肉收缩的影响数据。
五、实验结果
1)用锌铜弓刺激坐骨神经时腓肠肌发生收缩。
2)不同频率递增对肌肉收缩影响记录图
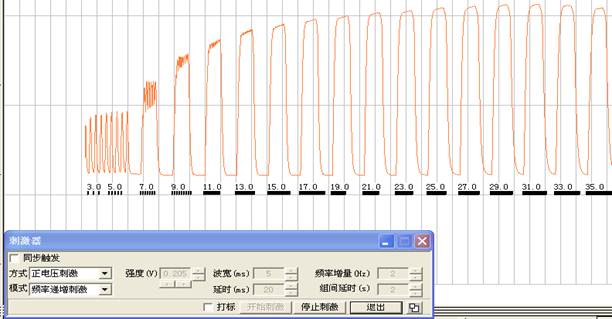
3)不同强度对肌肉收缩影响记录图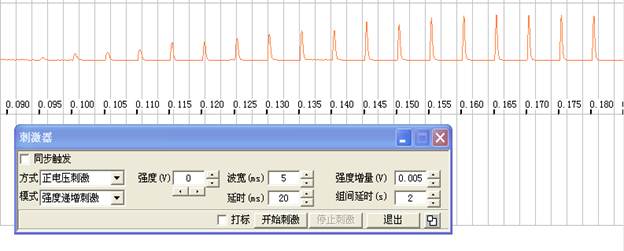
在一定刺激时间下,刚能引起组织发生兴奋的刺激称为阈刺激,所达到的强度为阈强度;能引起组织发生最大兴奋的最小刺激称为最大刺激,相应的刺激强度叫最大刺激强度。介于阈刺激和最大刺激间的刺激称阈上刺激,相应的刺激强度称为阈上刺激强度。
如上图所示:阈强度为0.096V,最大刺激强度0.162V。
开始收缩的频率为3Hz ,完全强直收缩的频率为23Hz
六、实验分析
1. 锌铜弓用金属锌和铜铆接而成,锌铜弓在极性溶液中形成回路时,锌与铜两极产生约0.5-0.7V的直流电压,电流的刺激作用于神经肌肉标本,由于产生生物电流,因而引起肌肉的收缩。
2. 制备标本的过程中,要不断滴加任氏液,以防标本干燥,丧失正常生理活性;操作过程中应避免强力牵拉和手捏神经或夹伤神经肌肉;毁脑脊髓时防止蟾蜍皮肤分泌的蟾蜍毒液射入操作者眼内或污染实验标本。
3. 在恒定时间间隔用不同强度的电压刺激坐骨神经,当电压低于阈值的强度刺激,坐骨神经支配腓肠肌的神经纤维不发生兴奋,其所支配的肌细胞也不会发生兴奋和收缩。刺激电压达到阈强度(本次实验阈强度为0.095V)时,坐骨神经干中阈值最低的神经开始兴奋,其所支配的运动单位的肌纤维兴奋并发生收缩。刺激强度逐渐增大,坐骨神经干中兴奋的神经纤维增加,兴奋和收缩的运动单位增加,令总收缩张力增加。当刺激电压达到使支配腓肠肌的神经纤维全部兴奋,则收缩张力达单收缩最大值(本次实验最大刺激强度0.162V)。
4. 如果给肌肉以连续短促刺激,随着刺激频率的不同,肌肉收缩会出现不同的形式。当频率较低时(本实验频率为3Hz),后一个刺激落在前一个刺激引起的收缩过程结束之后,则只引起一连串各自分开的单收缩。随频率增加,后一个刺激落在前一个刺激引起的收缩过程的舒张期,则如实验记录数据所示的在频率为7Hz时形成了不完全强直收缩。当频率增加到每一个后面的刺激落在前一个收缩过程中的收缩期,则各次收缩的张力变化和长度完全融合或叠加起来,就形成完全强直收缩,如实验结果记录所示,开始完全强直收缩的频率为23Hz。
七、实验结论
1. 蛙类的某些基本生命活动和生理功能与哺乳类动物有相似之处,而且其离体组织的生活条件比较简单,易于控制和掌握,来源也较丰富,由此在生理学实验,尤其是细胞生理学的某些实验中,常用蛙或蟾蜍的坐骨神经腓肠肌标本来观察神经肌肉的兴奋性、刺激与反应的规律及肌肉收缩的特点等。
2. 在保持足够的刺激时间(脉冲波宽)不变的条件下,通过逐步增加对蟾蜍坐骨神经的刺激强度(脉冲振幅),当电压低于阈值的强度刺激,坐骨神经支配腓肠肌的神经纤维不发生兴奋。刺激电压达到阈强度时,坐骨神经干中阈值最低的神经开始兴奋。当刺激电压达到使支配腓肠肌的神经纤维全部兴奋,则收缩张力达单收缩最大值。
3. 在保持足够的刺激时间(脉冲波宽)不变的条件下和改变电脉冲刺激频率可发现当频率较低时,只引起一连串各自分开的单收缩。随频率增加,后一个刺激落在前一个刺激引起的收缩过程的舒张期,则形成了不完全强直收缩。当频率增加到每一个后面的刺激落在前一个收缩过程中的收缩期,则各次收缩的张力变化和长度完全融合或叠加起来,就形成完全强直收缩。
参考文献:
[1]陆源、林国华、杨午鸣主编《机能学实验教程》朱大年、王庭槐第8版《生理学》
[2]朱大年、王庭槐第8版《生理学》
第二篇:实验1 蛙坐骨神经–腓肠肌标本制备、1
实验1 蛙坐骨神经–腓肠肌标本制备、
刺激频率对肌肉收缩的影响
【目的要求】
1.学习坐骨神经–腓肠肌标本的制备方法。
2.分析探讨刺激频率对肌肉收缩的影响。
【原理】
刺激坐骨神经能引起腓肠肌产生收缩。在其他条件不变情况下,不断增大刺激频率可引起肌肉收缩形式发生改变。若刺激频率较小,两次刺激间隔时间大于一次肌肉收缩和舒张所持续的时间(即单收缩)时,肌肉收缩表现为一连串的单收缩;若增大刺激频率,使两次刺激间隔时间大于一次肌肉收缩的收缩期时间,而小于单收缩时,肌肉呈现不完全强直收缩;若继续增加刺激频率,使两次刺激间隔时间小于一次肌肉收缩的收缩期时间,肌肉则表现出完全强直收缩。
【器材】
蟾蜍或蛙;任氏液;二道生理记录仪、双脉冲刺激器、肌槽、常规手术器械、玻璃分针、毁髓针、锌铜弓、解剖盘、烧杯、滴灌、任氏液等。
【步骤】
1、双毁髓:左手握蟾蜍,背部向上。用食指按压其头部前端,拇指压住躯干的背部,使头向前俯;右手持毁髓针,由两眼之间中线向后方划触,触及两耳后腺之间的凹陷处即是枕骨大孔的位置。将毁髓针由凹陷处垂直刺入枕骨大孔,然后针尖向前刺入颅腔,在颅腔内搅动,以毁脑组织。再将毁髓针退至枕骨大孔,针尖转向后方,与脊柱平行刺入椎管,以捣毁脊髓。脊髓彻底捣毁时,可看到蟾蜍后肢突然蹬直,然后瘫软,此时的动物为双毁髓动物。
2、剥制后肢标本:左手持手术镊提起两前肢之间背部的皮肤,右手持手术剪横向剪断皮肤,然后往后肢方向撕剥皮肤。剪开腹壁肌肉,用手术镊提起内脏,翻向头部,在看清支配后肢的脊神经发出部位后,于其前方剪断脊柱。
3、分离两后肢:将去皮的后肢腹面向上置于解剖盘上,右手持金冠剪纵向剪开脊柱,再剪开耻骨联合,使两后肢完全分离。
4、分离坐骨神经:将一侧后肢的脊柱端腹面向上,用玻璃分针沿脊神经向后分离坐骨神经,股部沿腓肠肌正前方的股二头肌和半膜肌之间的裂缝,找出坐骨神经,剪断盖在上方的梨状肌,完全暴露坐骨神经,剪去支配腓肠肌之外的分支,再剪去脊柱及肌肉,只保留坐骨神经发出部位的一小块脊柱骨。
5、分离股骨头:沿膝关节剪去股骨周围的肌肉,保留股骨的后2/3,剪断股骨。
6、游离腓肠肌:在腓肠肌跟腱下穿线并结扎,提起结扎线,剪断肌腱与胫腓骨的联系,游离腓肠肌,剪去膝关节下部的后肢,保留腓肠肌与股骨的联系,制备出完整的坐骨神经-腓肠肌标本。标本应包括:坐骨神经、腓肠肌、股骨头和一段脊柱骨四部分。
7、检验标本:用任氏液沾湿的锌铜弓的两极接触神经,如腓肠肌发生收缩,则标本机能正常,把标本固定在肌槽上。
8、连接好装置,调节适宜的灵敏度及刺激强度,开动记录仪,走纸速度为10mm/s,用手控触发开关,以单脉冲刺激神经,记录肌肉的单收缩曲线。
9、分别用1 Hz、2 Hz、3 Hz、4 Hz、6 Hz、12 Hz、24 Hz、30Hz等频率去刺激坐骨神经,记录肌肉的收缩曲线。
【注意事项】
(1)双毁髓时应注意使蟾蜍头部前俯,防止耳后腺分泌物射入实验者眼内,如被射入,应立即用生理盐水冲洗眼睛。
(2)标本制备过程中应经常滴加任氏液,防止标本干燥,以保持正常生理活性。
(3)避免污染、过度牵拉或用器械夹伤坐骨神经和腓肠肌。
(4)在骨骼肌收缩后,应让其休息一定时间后再作下一次刺激,特别是在观察刺激频率的影响时。
