制备坐骨神经腓肠肌标本
【目的和原理】
蛙类的一些基本生命活动规律与温血动物相似,而维持其离体组织正常活动所需的理化条件比较简单,易于建立和控制。因此,在实验中常用蟾蜍或蛙的坐骨神经腓肠肌标本来观察兴奋与兴奋性、刺激与肌肉收缩等基本生命现象和过程。故制备坐骨神经腓肠肌标本(sciatic nerve-gastrocnemius muscle specimen)是机能学实验中必须掌握的一项基本技术。本实验要求掌握制备坐骨神经腓肠肌标本的技能,并获得兴奋性良好的标本。
【实验材料】
蟾蜍或蛙;蛙板、玻璃分针、普通剪刀、手术剪、镊子、探针、玻璃分针、蛙钉、瓷盘、滴管、培养皿、锌铜弓;任氏液(Ringer’s solution)。
【实验步骤】
标本制作方法:
1.破坏脑和脊髓取蟾蜍一只,用自来水冲洗干净。左手握住蟾蜍,用食指按压其头部前端,拇指按压背部,右手持探针于枕骨大孔处垂直刺入,然后向前通过枕骨大孔刺入颅腔,左右搅动充分捣毁脑组织。然后将探针抽回至进针处,再向后刺入脊椎管,反复提插捣毁脊髓。此时如蟾蜍四肢松软,呼吸消失,表明脑和脊髓已完全破坏,否则应按上法反复进行。
2.剪除躯干上部及内脏在骶骼关节水平以上1~2cm处剪断脊柱,
左手握住蟾蜍后肢,用拇指压住骶骨,使蟾蜍头与内脏自然下垂,右手持普通剪刀,沿脊柱两侧剪除一切内脏及头胸部,留下后肢、骶骨、脊柱以及紧贴于脊柱两侧的坐骨神经。剪除过程中注意勿损伤坐骨神经。
3.剥皮左手握紧脊柱断端(注意不要握住或压迫神经),右手握住其上的皮肤边缘,用力向下剥掉全部后肢的皮肤。把标本放在盛有任氏液的培养皿中。将手及用过的剪刀、镊子等全部手术器械洗净,再进行下面步骤。
4.分离两腿用镊子夹住脊柱将标本提起,背面朝上,剪去向上突起的尾骨(注意勿损伤坐骨神经)。然后沿正中线用剪刀将脊柱和耻骨联合中央劈开两侧大腿,并完全分离,注意保护脊柱两侧灰白色的神经。将两条腿浸入盛有任氏液的培养皿中。
5.制作坐骨神经腓肠肌标本取一条腿放置于蛙板上或置于蛙板上的小块玻璃板上。
(1)游离坐骨神经将腿标本腹面朝上放置(如图1)。用玻璃分针沿脊柱旁游离坐骨神经,并于近脊柱处穿线结扎神经。再将标本背面朝上放置,把梨状肌及其附近的结缔组织剪去。循坐骨神经沟(股二头肌与半膜肌之间的裂缝处),找出坐骨神经的大腿段。用玻璃分针仔细剥离,然后从脊柱根部将坐骨神经剪断,手执结扎神经的线将神经轻轻提起,剪断坐骨神经的所有分支,并将神经一直游离至腘窝。
(2)完成坐骨神经小腿标本将游离干净的坐骨神经搭于腓肠肌上,在膝关节周围剪掉全部大腿肌肉,并用普通剪刀将股骨刮干净。然后从股骨中部剪去上段股骨,保留的部分就是坐骨神经小腿标本。
(3)完成坐骨神经腓肠肌标本将上述坐骨神经小腿标本在跟腱处穿线结扎后,于结扎处远端剪断跟腱。游离腓肠肌至膝关节处,然后从膝关节处将小腿其余部分剪掉,这样就制得一个具有附着在股骨上的腓肠肌并带有支配腓肠肌的坐骨神经的标本。
6.检查标本兴奋性用经任氏液湿润的锌铜弓轻轻接触一下坐骨神经,如腓肠肌发生迅速而明显的收缩,则表明标本的兴奋性良好,即可将标本放在盛有任氏液的培养皿中,以备实验用。若无锌铜弓,亦可用中等强度单个电刺激测试神经肌肉标本的兴奋性。
【结果分析与讨论】
结果:捣毁脊髓后四肢张力消失,用锌铜弓刺激坐骨神经和腓肠肌,可观察到肌肉收缩。
分析:当肌细胞发生兴奋时,首先在肌膜上出现动作电位,然后才发生肌丝滑行、肌小节缩短、肌细胞的收缩反应。目前认为,这个过程至少包括三个步骤:电兴奋通过横管系统向肌细胞深处传导;三联体结构处的信息传递;肌质网中钙离子释放入胞浆以及钙离子向肌质网的再聚集。
讨论:捣毁脊髓后,蟾蜍四肢张力消失,任氏液有一定的浸润神经,维持神经的生理活动的作用。锌铜弓金属类物质可导电,当
刺激浸润在任氏液的腓肠肌,使肌肉产生兴奋而发生收缩,实验时应该注意制备神经肌肉标本过程中,要不断加任氏液,以防标本干燥,丧失正常生理活性,还需要注意捣毁脊髓时,防止蟾蜍分泌的毒液摄入眼睛。
第二篇:蛙或蟾蜍坐骨神经-腓肠肌标本的制备
实验1 蛙或蟾蜍坐骨神经-腓肠肌标本的制备
【实验目的】
1. 学习急性实验的实验方法。
2. 通过本实验熟悉刺激、兴奋、兴奋性和可兴奋组织的概念。
3. 掌握蛙坐骨神经-腓肠肌标本的制备,为进行神经肌肉实验打下基础。
【实验原理】
蛙或蟾蜍等两栖类动物的一些基本生命活动和生理功能与温血动物相似,而其离体组织生活条件易于掌握,在任氏液的浸润下,神经肌肉标本可较长时间保持生理活性。因此,在生理学实验中常用蛙或蟾蜍坐骨神经腓肠肌离体标本来观察神经肌肉的兴奋性、兴奋过程以及骨骼肌收缩特点等。
【实验对象】
蛙或蟾蜍。
【实验器材与药品】
蛙类坐骨神经一腓肠肌标本制备手术器械和药品1套,包括:蛙板、小玻板各1块、粗剪刀、直剪刀各1把,大镊子、小镊子各1把,眼科剪刀1把、探针1根、玻璃分针2根、大烧杯、小烧杯各1个,滴管1支,培养皿1个、棉线,任氏液、锌铜叉。
【实验方法和步骤】
1. 破坏脑脊髓 取蟾蜍一只,用自来水冲洗干净。左手握住蟾蜍,用食指压住头部前端使头前俯,右手持刺蛙针从枕骨大孔向前刺入颅腔(图1-1),左右搅动捣毁脑组织,然后将刺蛙针退到枕骨大孔,不拔出而是将其尖转向后插入脊柱管中捣毁脊髓,插入椎管时,蟾蜍后肢立即失去紧张性,多数情况出现尿失禁。若脑脊髓破坏完全,可见蟾蜍四肢松软,呼吸消失。
2. 剪除上肢和内脏 在骶髂关节上0.5~1.0cm处用粗剪刀剪断脊柱。用镊子夹住后端脊柱,以剪刀沿脊柱两侧剪除所有内脏及头胸部,留下后肢、骶骨、后端脊柱及紧贴于脊柱两侧的坐骨神经(图1-2)。
3. 剥皮 左手用镊子或直接用手捏住脊柱断端(注意不要压迫神经),右手捏住断端边缘皮肤,向下剥去全部后肢皮肤(图1-3),将标本置于盛有任氏液的培养皿中。将手和用过的器械洗净后再进行以下步骤。
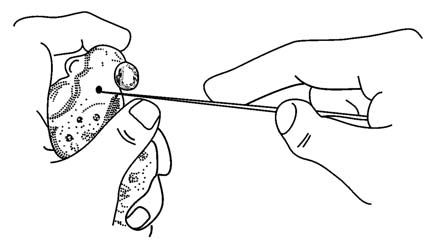
图1-1 破坏蟾蜍脑脊髓
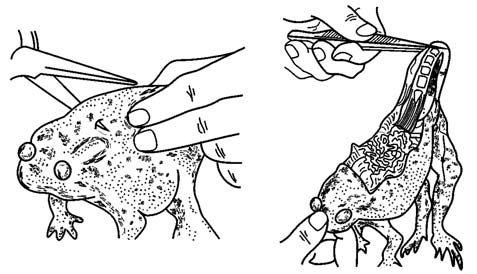
图1-2 剪除躯干和内脏
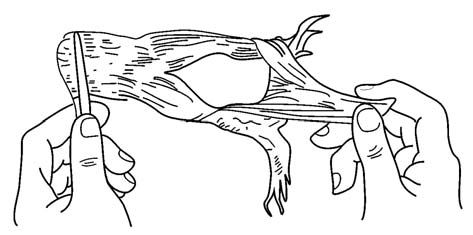
图1-3 剥除后肢皮肤
4. 分离两腿 用玻璃分针沿脊柱两侧游离出两条坐骨神经,并于近脊柱处各扎一细线,然
后在扎线与脊柱之间剪断神经。提着神经上的细线,将两条坐骨神经分别置于两条大腿上,左手持脊柱,将骶骨翘起,将下位脊柱全部剪除。捏着两侧骼骨向反方向分离,使耻骨联合脱臼后,沿耻骨联合正中将两下肢剪开,将一条腿浸于任氏液中备用,另一条置于浸有任氏液的玻璃板上。
5. 游离坐骨神经和剪断股骨 认清坐骨神经沟和腓肠肌的部位(图),用剪刀剪断梨状肌
及其周围的结缔组织,左手提着神经上的细线,右手持剪刀或玻璃分针沿坐骨神经沟细心剥离,直至将坐骨神经剥离到腘窝。将游离干净的坐骨神经放在下腿上,沿膝关节的周围将大腿的所有肌腱剪断,并用剪刀刮净股骨下段附着的肌肉,在股骨上三分之一处剪去上段股骨及所附的肌肉,这样制成的称为坐骨神经下腿标本(图1-4)。
6. 游离腓肠肌 在坐骨神经下腿标本的基础上,用剪刀将跟腱的下端剪断,在跟腱与肌肉
交界处扎一条细线,左手提线,右手用剪刀游离腓肠肌,直到膝关节。最后用粗剪刀在膝关节下将小腿剪去,留下的即为坐骨神经腓肠肌标本(图1-5)。做好的标本用锌铜
叉的两极轻轻接触坐骨神经,如腓肠肌立即收缩,表示标本的兴奋性良好,然后将标本放入任氏液中,待其兴奋性稳定后再进行实验。
椎骨
蛙板
玻璃板
坐骨神经
玻璃分针
坐骨神经
半膜肌
骨二头肌
腓肠肌 腓肠肌 股骨
图1-4 分离坐骨神经 图1-5 坐骨神经-腓肠肌标本
【注意事项】
1. 已剥离皮肤的组织避免接触皮肤毒液或其他不洁物。
2. 分离神经时,一定要用玻璃分针,不能随便用刀、剪进行操作。
3. 不能过分牵拉神经,以免造成损伤。
4. 标本制备过程中应适当地用任氏液湿润标本。
5. 避免用手指或金属器械接触或夹持标本的神经肌肉部分。
【思考题】
你制备的坐骨神经腓肠肌标本兴奋性如何?有哪些体会?
(毕辉 段玉斌)
