邻二氮菲分光光度法测定微量铁
目的要求
(1)熟悉紫外可见分光光度计的使用方法;
(2)掌握利用标准曲线进行微量成分分光光度测定的基本方法和有关计算。 基本原理
在 pH 为2-9 的溶液中,邻二氮菲(简写作phen)与Fe2+发生下列显色反应: Fe2++3phen==[Fe(phen)3]2+
生成的橙红色络合物非常稳定,lgK 稳=21.3(20?C),其溶液在510 nm 有最大吸
收峰,摩尔吸光系数ε510=1.1×104 L·cm–1·mol–1,利用上述反应可以测定微量铁。
显色反应的适宜pH 范围很宽(2-9),酸度过高(pH<2)反应进行较慢;若 酸度过低,Fe2+将水解。通常在pH 约为5 的HAc-NaAc 缓冲介质中测定。 邻二氮菲与Fe2+反应的选择性很高,相当于含铁量5 倍的Co2+和Cu2+,20 倍量的Cr3+, Mn2+, PO4
3–和VO3
–,甚至40 倍量的Al3+, Ca2+, Mg2+, SiO3
2–, Sn2+和
Zn2+都不干扰测定。
本实验以盐酸羟胺为还原剂,也可使用抗坏血酸将Fe3+还原为Fe2+。
利用分光光度计法进行定量测定时,一般是选择与被测物质(或经显色反应 后产生的新物质)最大吸收峰相应单色光的波长为测量吸光度的波长。显然,该 波长下的摩尔吸光系数ε 最大,测定的灵敏度也最高。为了找出物质的最大吸收
峰所在的波长,需测绘有关物质在不同波长单色光照射下的吸光度曲线,即吸收 曲线(或称吸收光谱);或者在紫外可见光波长范围内,对被测物质进行全波长 扫描后得到一张吸收光谱图,这个谱图上显示的波峰处所对应的波长就是该物质 的最大吸收波长。
通常采用标准曲线法进行定量测定,即先配制一系列不同浓度的标准溶液, 在选定的反应条件下使被测物质显色,并在选定的波长测得相应的吸光度,以浓 度为横坐标,吸光度为纵坐标绘制标准曲线(或称工作曲线)。另取试液经适当 处理后,在与上述相同的条件下显色和测定吸光度,由测得的吸光度从标准曲线 上求得被测物质的含量。
由于邻二氮菲与Fe2+的反应选择性高,显色反应所生成的有色络合物稳定, 测定结果的重现性好,因此在我国的国家标准(GB)中,测定钢铁、锡、铅焊 料、铅锭等冶金产品和工业硫酸、工业碳酸钠、氧化铝等化工产品中的铁含量, 都采用邻二氮菲显色的分光光度法。
一、仪器
UV-1100 型紫外可见分光光度计(上海美谱达)、比色皿、容量瓶、吸量管 等。
二、试剂与试样
铁标准溶液(0.0100 mg·mL-1)、1 g·L–1 邻二氮菲水溶液、10 g·L–1 盐酸羟胺
水溶液、HAc-NaAc 缓冲溶液(pH=4.6)、水样。
三、实验步骤
1. 标准曲线的绘制
用吸量管分别吸取0.0100 mg·m L-1 的铁标准溶液0 mL、1.00 mL、2.00 mL、 3.00 mL、4.00 mL、5.00 mL、6.00mL 和7.00 mL 于8 只50 mL 容量瓶中,一次 各加入2.5 mL 盐酸羟胺溶液、5 mL HAc-NaAc 缓冲溶液、5 mL 邻二氮菲溶液, 用蒸馏水稀释至刻度,摇匀,放置10 min。用1 cm 比色皿,以试剂空白溶液为 参比溶液,在510 nm 下,分别测量各溶液的吸光度。以吸光度为纵坐标,铁含 量为横坐标作标准曲线。
2. 水样测定
取水样5.00 mL,以同样步骤测定水样,根据标准曲线计算水中铁的含量
第二篇:实验一 邻二氮菲分光光度法测定微量铁
实验一 邻二氮菲分光光度法测定微量铁
一、实验目的
1.掌握邻二氮菲分光光度法测定微量铁的方法原理
2.熟悉绘制吸收曲线的方法,正确选择测定波长
3.学会制作标准曲线的方法
4.通过邻二氮菲分光光度法测定微量铁,掌握721型分光光度计的正确使用方法,并了解此仪器的主要构造。
二、实验原理
根据朗伯-比耳定律:A=εbc,当入射光波长λ及光程b一定时,在一定浓度范围内,有色物质的吸光度A与该物质的浓度c成正比。只要绘出以吸光度A为纵坐标,浓度c为横坐标的标准曲线,测出试液的吸光度,就可以由标准曲线查得对应的浓度值,即未知样的含量。同时,还可应用相关的回归分析软件,将数据输入计算机,得到相应的分析结果。
邻二氮菲(1,10—二氮杂菲),也称邻菲罗啉是测定微量铁的一个很好的显色剂。在pH2—9范围内(一般控制在5—6间)Fe2+与试剂生成稳定的橙红色配合物Fe(Phen)32+lgK=21.3,在510nm下,其摩尔吸光系数为1.1×104L/moL.cm, )。Fe3+与邻二氮菲作用生成蓝色配合物,lgK稳=14.1,稳定性较差,因此在实际应用中常加入还原剂盐酸羟胺,使Fe3+还原为Fe2+。其反应式如下:
2 Fe3+ + 2 NH2OH·HCl → 2Fe2+ + N2 + H2O + 4H+ + 2Cl-
本方法的选择性很高。相当于含铁量40倍的Sn、AI、Ca、Mg、Zn、Si,20倍的Cr、Mn、V、P和5倍的Co、Ni、Cu不干扰测定。
三、试剂与仪器
(一)仪器:
1.721型分光光度计
2.50mL容量瓶8个(5-6人/组),100mL1个,500mL1个
3.移液管:2 mL1支,10 mL1支
4.刻度吸管:10mL、5mL、1mL各1支
(二)试剂:硫酸铁铵、盐酸、盐酸羟胺、醋酸钠、醋酸、邻二氮菲。
(三)标准溶液配制
1) 100μg·mL-1铁标准溶液配制:准确称取0.4317g铁盐NH4Fe(SO4)2·12H2O,置于烧杯中,加入20mL 6 mol·L-1 HCl溶液和少量水,溶解后,定量转移至500 mL容量瓶中,加水稀释至刻度,充分摇匀,得100μg·mL-1储备液。
2) 10μg·mL-1铁标准溶液配制:用移液管吸取上述100μg·mL-1铁标准溶液10.00mL,置于100mL容量瓶中,加入2.0mL 6mol·L-1HCl溶液,用水稀释至刻度,充分摇匀。
3)HCI 6moL/L:100mL
4)盐酸羟胺10%(新鲜配制):100mL
5)邻二氮菲溶液0.1%(新鲜配制):200mL
6)HAc—NaAc缓冲溶液(pH=5)500 mL:称取136gNaAc,加水使之溶解,再加入120 mL冰醋酸,加水稀释至500 mL
四、实验步骤
1.绘制吸收曲线:用吸量管吸取铁标准溶液(10ug/mL)0.0、2.0、4.0 mL分别放入50 mL容量瓶中,加入1 mL10%盐酸羟胺溶液、2.0 mL0.1%邻二氮菲溶液和5 mL HAc—NaAc缓冲溶液,加水稀释至刻度,充分摇匀,放置5分钟,用3cm比色皿,以试剂溶液为参比液,于721型分光光度计中,在440—560nm波长范围内分别测定其吸光度A值。当临近最大吸收波长附近时应间隔波长5—10nm测A值,其他各处可间隔波长20—40nm测定。然后以波长为横坐标,所测A值为纵坐标,绘制吸收曲线,并找出最大吸收峰的波长。
2.标准曲线的绘制:用吸量管分别移取铁标准溶液(10ug/mL)0.0、1.0、2.0、4.0、6.0、8.0、10.0 mL依次放入7只50mL容量瓶中,分别加入10%盐酸羟胺溶液1 mL,稍摇动,再加入0.1%邻二氮菲溶液2.0 mL及5 mL HAc—NaAc缓冲溶液,加水稀释至刻度,充分摇匀,放置5分钟,用3cm比色皿,以不加铁标准溶液的试液为参比液,选择最大测定波长为测定波长,依次测A值。以铁的质量浓度为横坐标,A值为纵坐标,绘制标准曲线。
3.水样分析:
分别加入5.00mL(或10.00mL,铁含量以在标准曲线范围内为宜)未知试样溶液,按实验步骤2的方法显色后,在最大测定波长处,用3cm比色皿,以不加铁标准溶液的试液为参比液,平行测A值。求其平均值,在标准曲线上查出铁的质量,计算水样中铁的质量浓度。
五、数据记录与处理
1、吸收曲线
1)记录数据

2)绘制吸收曲线,确定最大吸收波长λmax= nm
2、标准曲线
1)记录数据
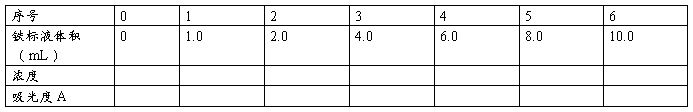
2)绘制标准曲线(列出标准曲线方程)
3、水样分析
计算未知溶液中CFe2+ = μg·mL-1
六、思考与讨论
1.邻二氮菲分光光度法测定微量铁时为什么要加入盐酸羟胺溶液?
2.吸收曲线与标准曲线有何区别?在实际应用中有何意义
