1.5 化学反应热效应的计算
1.5.1 状态函数法计算恒压与恒容反应热——赫斯(Hess)定律
不管恒压或恒容化学反应是一步完成还是分几步完成,它们的热效应相同。这就是赫斯定律,其本质为状态函数法。如:
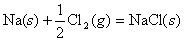 (1)
(1)
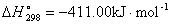


 是下面三个反应之和:
是下面三个反应之和:
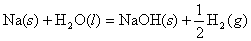 (2)
(2)
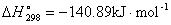


 (3)
(3)
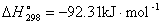



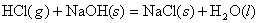 (4)
(4)

第一个反应的热效应也是后三个反应的热效应之和:
-411.00=(-140.89)+(-92.31)+(-177.80)
赫斯定律是赫斯在1840年从实验中总结出来的,当时热力学第一定律还未发现。热力学第一定律发现之后,这个定律就成了热力学第一定律的必然结果了,因恒压热效应 和恒容热效应
和恒容热效应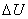 都是状态函数,它们只与体系的始末态有关,而与具体途径无关。
都是状态函数,它们只与体系的始末态有关,而与具体途径无关。
1.5.2 热化学数据的建立及应用
(1) 化合物的生成焓
定义:一定温度,由标准状态下最稳定的单质生成标准状态下指定相态的1mol化合物的焓变,叫该化合物的标准生成焓,用符号 表示(下标f来自formation)。如
表示(下标f来自formation)。如
标态下: 
 (1)
(1)
标态下: 
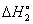 (2)
(2)
那么
 =
=
 =
=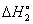
什么是最稳定的单质呢?如25℃,1atm.下,碳有石墨、无定型及金刚石三种相态,其中只有石墨是最稳定的相态,故生成反应中当涉及到最稳定的单质碳时必须是石墨。
根据定义,标准状态下最稳定的单质生成焓为0。
对于标态下反应

 (4)
(4)
的反应热为

或  (5)
(5)
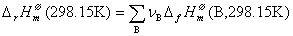 由生成热计算化学反应热:
由生成热计算化学反应热:
(2) 燃烧焓
定义:一定温度,在标准状态下,1mol指定相态的某物质,与氧进行完全燃烧所释放出来的热量,称为该物质的标准燃烧焓,用符号 表示(下标c来自combustion)。如
表示(下标c来自combustion)。如
标态下: 
 (6)
(6)
标态下: 
 (7)
(7)
那么


定义中的完全燃烧是指燃烧的产物不能再燃烧,如反应(6)为完全燃烧,但反应
标态下: 
不是完全燃烧。燃烧产物规定为 →
→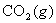 ,
, →
→ ,
, →
→ ,
, →
→ 。按定义,这些燃烧产物的燃烧焓为0。
。按定义,这些燃烧产物的燃烧焓为0。
例:利用燃烧焓求反应
标态下: 
 (8)
(8)
的反应热 。
。
解: 
=
=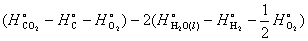
=
=
可见,一个反应的反应热等于生成物的燃烧焓之和减去反应物的燃烧焓之和的负值。
因此反应(4)的反应热如果用燃烧焓计算,则为
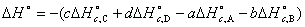
或
 (9)
(9)
 由燃烧热计算化学反应热:
由燃烧热计算化学反应热:
(3)离子标准生成热

(4)溶解热及稀释热
(1)溶解热:在指定条件(p,T)下, 1mol溶质溶于一定量溶剂,形成指定浓度溶液时的热效应。记为:△solHm。
(2)稀释热:在指定条件(p,T)下,将一定量的溶剂加到含 1mol溶质的溶液之中,形成指定浓度溶液时的热效应。记为:△dilHm。(积分~)
1.5.3 温度对反应热效应的影响
——基尔霍夫(Kirchhoff)定律
反应焓变值一般与温度关系不大。如果温度区间较大,在等压下虽化学反应相同,但其焓变值则不同。由数据库中的热力学数据可计算298K的化学反应热,其他温度下的反应热须使用基尔霍夫定律计算。在1858年首先由Kirchoff提出了焓变值与温度的关系式,所以称为Kirchoff定律。由状态函数法可以导出基尔霍夫定律。
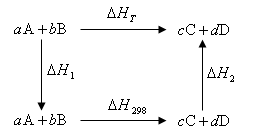 对于一定反应:
对于一定反应:



 这就是基尔霍夫公式。
这就是基尔霍夫公式。
微分上式,得

这就是基尔霍夫公式的微分形式。

DCp也是温度的函数,只要将Cp - T的关系式代入,就可从一个温度时的焓变求另一个温度下的焓变。
由微分式式知:化学反应热效应随温度而变是由于产物热容和与作用物热容和不相等(△Cp≠0)所致。
①若△Cp= 0, 则△rHm是与温度无关的常数
②若△Cp > 0, 对吸热反应(△rHm > 0), T↑, 吸热量↑
对放热反应(△rHm < 0), T↑, 放热量↓
③若△Cp < 0, 则情况与②相反
 在积分式计算过程,如有物质发生相变,就要进行分段积分:
在积分式计算过程,如有物质发生相变,就要进行分段积分:
作用物发生相变取“+”,产物发生相变取“-”
例1  按下式进行燃烧反应
按下式进行燃烧反应

在25℃和常压下每燃烧1mol 放热2020kJ,同样条件下2 mol元素硼燃烧生成1mol
放热2020kJ,同样条件下2 mol元素硼燃烧生成1mol 放热1264kJ,
放热1264kJ, 的生成焓为(-241.82 )kJ
的生成焓为(-241.82 )kJ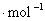 。求25℃时
。求25℃时 的标准生成焓。
的标准生成焓。
解 已知 


所以

 +3
+3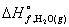 -
- =
=
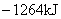
 -
- =
=
 =30.54
=30.54
例2:已知298K及pΘ下,丙烯腈CH=CH2-CN(l)、石墨和氢气的燃烧热分别为-1760.71、-393.51和-285.85 kJ·mol-1,丙烯腈的燃烧反应为:
CH=CH2-CN(l) + 3.75 O2(g) === 3C O2(g) +0.5N2(g) + 1.5 H2O(l)
已知298K及pΘ下CH=CH2-CN(l)的蒸发热为△vapHmΘ= 32.84kJ·mol-1,气态HCN(g)和C2H2(g)的生成焓分别为129.70和226.73 kJ·mol-1;求以下反应在298K和pΘ的热效应△rHmΘ。
C2H2(g) + HCN(g) == CH=CH2-CN( g)
解:反应C2H2(g) + HCN(g) == CH=CH2-CN( g) 的热效应△rHmΘ 与各反应物的生成热之间的关系为:
△rHmΘ = △fHmΘ[CH=CH2-CN( g)] -△fHmΘ[C2H2(g)] -△fHmΘ[HCN(g)]
根据CH=CH2-CN(l)的燃烧反应和CH=CH2-CN(l)的蒸发过程
CH=CH2-CN(l) + 3.75 O2(g) === 3CO2(g) +0.5N2(g) + 1.5 H2O(l)
△cHmΘ[CH=CH2-CN(l)]
CH=CH2-CN(l) === CH=CH2-CN( g) △vapHmΘ
得CH=CH2-CN(g )的燃烧反应热效应:
CH=CH2-CN(g ) + 3.75 O2(g) === 3CO2(g) +0.5N2(g) + 1.5 H2O(l)
△cHmΘ[CH=CH2-CN(g )] = △cHmΘ[CH=CH2-CN(l)]-△vapHmΘ= -1793.55 kJ·mol-1
CH=CH2-CN( g) 的生成反应为:
3C(s) +1.5 H2( g) + 0.5 N2(g) === CH=CH2-CN( g)
所以,△fHmΘ[CH=CH2-CN( g)]
= 3△cHmΘ[C(s)] +1.5△cHmΘ[H2( g)] -△cHmΘ[CH=CH2-CN(g)]
= 3×(-393.51) +1.5×(-285.85) -(-1793.55) = 184.245 kJ·mol-1
故反应C2H2(g) + HCN(g) == CH=CH2-CN( g) 的热效应为:
△rHmΘ = △fHmΘ[CH=CH2-CN( g)] -△fHmΘ[C2H2(g)] -△fHmΘ[HCN(g)]
= 184.245 -226.73-129.70 = -172.185 kJ·mol-1
例3: 已知373.15 K、 下,水的蒸发热为
下,水的蒸发热为 (H2O, l)=40.71 kJ·mol-1,在此温度范围内水和水蒸气的平均恒压热容分别为75.31J·mol-1·K-1及33.18 J·mol-1·K-1。求298.15K、
(H2O, l)=40.71 kJ·mol-1,在此温度范围内水和水蒸气的平均恒压热容分别为75.31J·mol-1·K-1及33.18 J·mol-1·K-1。求298.15K、 下的
下的 (H2O, l)。
(H2O, l)。
解:可设计如下过程,其中的ΔH (T2)即为所求:

ΔH (T2) =ΔH1+ΔH2(T1) +ΔH3
= Cp,m[H2O(l)]ΔT + 40710 + Cp,m [H2O(g)]ΔT
= 75.31×(373.15-298.15) + 40710 +33.18×(298.15-373.15)
= 43870 J = 43.87 kJ
或:ΔH (T2)=ΔH (T1)+ = 40710+
= 40710+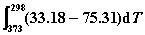 = 43869 J
= 43869 J
第二篇:化学反应热的计算
知识点一:盖斯定律1、盖斯定律的内容 不管化学反应是一步完成或分几步完成,其反应热是相同的.换句话说,化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。2、盖斯定律直观化 △H=△H1+△H23、盖斯定律的应用 (1)有些化学反应进行很慢或不易直接发生,很难直接测得这些反应的反应热,可通过盖斯定律获得它们的反应热数据。 例如:C(s)+0.5O2(g)=CO(g) 上述反应在O2供应充分时,可燃烧生成CO2、O2供应不充分时,虽可生成CO,但同时还部分生成CO2。因此该反应的△H无法直接测得。但是下述两个反应的△H却可以直接测得: C(S)+O2(g)=CO2(g) △H1=-393.5kJ/mol CO(g)+0.5 O2(g)=CO2(g) △H2=-283.0kJ/mol 根据盖斯定律,就可以计算出欲求反应的△H。 分析上述反应的关系,即知 △H1=△H2+△H3 △H3=△H1-△H2=-393.5kJ/mol--(-283.0kJ/mol)=-110.5kJ/mol 由以上可知,盖斯定律的实用性很强。 (2)在化学计算中,可利用热化学方程式的组合,根据盖斯定律进行反应热的计算。 (3)在化学计算中,根据盖斯定律的含义,可以根据热化学方程式的加减运算,比较△H的大小。知识点二:反应热的计算 根据热化学方程式、盖斯定律和燃烧热的数据,可以计算一些反应的反应热。反应热、燃烧热的简单计算都是以它们的定义为基础的,只要掌握了它们的定义的内涵,注意单位的转化即可。 热化学方程式的简单计算的依据: (1)热化学方程式中化学计量数之比等于各物质物质的量之比;还等于反应热之比。 (2)热化学方程式之间可以进行加减运算。【规律方法指导】有关反应热的计算依据归纳1、根据实验测得热量的数据求算 反应热的定义表明:反应热是指化学反应过程中放出或吸收的热量,可以通过实验直接测定。 例如:燃烧6g炭全部生成气体时放出的热量,如果全部被水吸收,可使1kg水由20℃升高到67℃,水的比热为4.2kJ/(kg·℃),求炭的燃烧热。 分析:燃烧热是反应热的一种,它是指在101Kpa时,1mol纯净可燃物完全燃烧生成稳定氧化物时所放出的热量。据题意,先求得1kg水吸收的热量:Q=cm△t=197.4kJ,由此得出该反应燃烧热为394.8KJ/mol。(△H=-394.8KJ/mol)2、根据物质能量的变化求算 根据能量守恒,反应热等于生成物具有的总能量与反应物具有的总能量的差值。当E1(反应物)>E2(生成物)时,△H<0,是放热反应;反之,是吸热
反应。 △H=ΣE生成物-ΣE反应物 如图所示: 3、根据反应实质键能的大小求算 化学反应的实质是旧键的断裂和新键的生成,其中旧键的断裂要吸收能量,新键的生成要放出能量,由此得出化学反应的热效应(反应热)和键能的关系:△H =E1(反应物的键能总和)-E2(生成物的键能总和)。 例如:根据下表数据,求H2(g)+Cl2(g)=2HCl(g)的反应热。 H2 Cl2 HCl 键能(KJ/mol) 436 243 431 分析:根据公式: △H =E1(反应物的键能总和)-E2(生成物的键能总和)=(436+243-2×431)KJ/mol=-183KJ/mol4、根据热化学方程式求算 热化学方程式中表明了化学反应中能量的变化。△H的大小与方程式中物质的系数大小成正比。 例如: H2 (g) + O2 (g) = H2O (g) △H = -241.8 KJ/ mol 则: 2 H2 (g) + O2 (g) = 2H2O (g) △H = ?KJ/ mol 分析:当物质的系数变为2倍时,反应热也同时变为2倍。 所以 △H=-483.6 KJ/ mol 5、根据盖斯定律的规律求算 盖斯定律是热化学中一个相当有实用价值的定律。其内容是不管化学反应过程是一步完成还是分几步完成,总过程的热效应是相同的,即一步完成的反应热等于分几步完成的反应热之和。利用这一规律,可以从已经测定的反应的热效应来计算难于测量或不能测量反应的热效应,它是间接求算反应热的常用方法。 具体计算方法是:通过热化学方程式的叠加,进行△H的加减运算。 例如:实验中不能直接计算出由石墨和氢气生成甲烷反应的反应热,但可测出CH4、石墨和氢气的燃烧热。试求出石墨生成甲烷的反应热。 ①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=-890.5KJ/mol ②C(石墨)+O2(g)=CO2(g) △H2=-393.5KJ/mol ③H2(g)+1/2O2(g)=H2O(l) △H3=-285.8KJ/mol ④C(石墨)+2H2(g)=CH4(g) △H4 分析:根据盖斯定律,可以通过反应①②③的叠加组合出反应④,则反应热的关系为: △H4=2△H3+△H2-△H1=2×(-285.8 KJ/mol)+(-393.5 KJ/mol)-(-890.5 KJ/mol)=-74.6 KJ/mol。【经典例题透析】 1已知1 g氢气在氧气中完全燃烧,生成气态水放出120.9KJ的热量,试计算1000L标准状况下的氢气完全燃烧所放出的热量。 解析: 解法一、根据热化学方程式进行计算 解:设氢气燃烧的热化学反应的反应热 △H = -Q KJ/ mol H2 (g) + O2 (g) H2O (g) △H = -Q KJ/ mol 2 g Q KJ 1 g 120.9 KJ = Q = 241.8 △H = -241.8 KJ/ mol
又设1000L标准状况下的氢气完全燃烧所放出的热量为Q1 H2 (g) + O2 (g) H2O (g) △H = -241.8 KJ/ mol 22.4 L 241.8KJ 1000 L Q1 = Q1 = 1.08×104 KJ 答:………(从略)。 解法二:关系式法:设1000L标准状况下的氢气完全燃烧所放出的热量为Q1 H2 (g) ―――――――――△H = -Q KJ/ mol ×22.4L/ mol 120.9 KJ 1000 L Q1 解得: Q1 = 1.08×104 KJ 答:………(从略)。 变式练习1: 25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量,下列表示该反应的热方程式正确的是 ( ) A、CH4O(l)+O2(g)==CO2(g)+2H2O(g) △H=—725.8kJ· mol—1 B、2CH4O(l)+3O2(g)==2CO2(g)+4H2O(l) △H=+1451.6kJ· mol—1 C、2CH4O(l)+3O2(g)==2CO2(g)+4H2O(l) △H=—22.68kJ· mol—1 D、CH4O(l)+O2(g)==CO2(g)+2H2O(l) △H=—725.8kJ· mol—1 解析:方程式中△H的大小与物质计量数成比例 答案:D 2 求 C (s) +O2 (g) = CO (g) △H1 …………① 已知:C (s) + O2 (g) = CO2 (g) △H2 = -393.5 KJ·mol-1 …………② CO ( g) + O2 (g) = CO2 (g) △H3 = -283.0 KJ·mol-1 …………③ 解析: 方法一:(组合法)用已知反应热的热化学方程式相互组合(加、减、乘等),得到未知反应热的热化学方程式,则相应的反应热作相同的组合(加、减、乘等数学计算)即为所求的反应热。 如:由②-③整理得① , 则△H1 = △H2-△H3=〔(-393.5)-(-283.0)〕=-110.5 KJ·mol-1 即: C (s)+O2 (g) = CO (g) △H1=-110.5 KJ·mol-1 方法二:热循环图式法 由热循环图示可知: H1 = △H2 - △H3 =(-393.5KJ·mol-1)-(-283.0KJ·mol-1) = -110.5 KJ·mol-1 C (s)+O2 (g)=CO (g) ;△H1 =-110.5 KJ·mol-1 变式练习2.盖斯根据一系列事实于1840年提出“不管化学过程是一步或分数步完成,这一过程热效应相同。” 换而言之:若一个反应可分成几步完成,则各步反应的反应热总和与该反应一次发生时反应热相同。 应用这条原理,解决下面问题: 已知:C(s)+O2(g)=CO2(g) △H=—393.5kJ· mol—1 CO(g)+ O2(g)=CO2(g) △H=—283kJ· mol—1 写出C(s)与O2(g)反应生成CO(g)
的,热化学方程式 。 【分析】先写出C(s)与O2(气)反应的化学方程式,由盖斯定律可知,碳完全燃烧生成CO2这个过程可分为两步完成。第一步是碳不完全燃烧生成CO,第二步是CO完全燃烧生成CO2。这两步的反应热之和应等于完全燃烧时的反应热。 【答案】依题知:C(s)+O2(g)=CO2(g) △H=—393.5kJ· mol—1……① CO(g)+ O2(g)=CO2(g) △H=—283kJ· mol—1……② 反应①-反应②得到 C(s)+ O2(g)=CO(g) △H=—110.5kJ· mol—1……③ 故答案为C(s)与O2(g)反应生成CO(g)的反应热为110.5kJ, 其热化学方程式为:③式。 【强调】正确书写热化学方程式要比判断正误档次要高。它要求学生全面掌握书写原则,无一疏漏。要认真细微进行计算,写出简明准确无误的热化学方程式。 变式练习3. 已知常温常压下,P2和P4燃烧的热化学方程式分别为: 2P2(g)+5O2(g)=P4O10(s) △H=-2695.4kJ/mol P4(g)+5O2(g)=P4O10(s) △H=-2925.1kJ/mol。则下列说法正确的是( ) A. 2P2(g) =P4(g) △H=-229.7kJ/mol B. P2制P4是放热反应 C. 等质量时,P2比P4具有的能量高 D. P2比P4更加稳定 解析:根据盖斯定律,2P2(g) =P4(g)的反应热△H=-2695.4-(-2925.1)=229.7(kJ/mol)>0,所以P2制P4是吸热反应;等质量时,P4具有更高的能量,进而可以推出P2比P4更加稳定。 答案:D 3. 在同温同压下,硫燃烧的热化学方程式如下: ①S(g)+O2(g)=SO2(l) △H1=a ②S(g)+O2(g)=SO2(g) △H2=b ③S(s)+O2(g)=SO2(g) △H3=c,则a、b、c的大小关系正确的是( ) A. a>b>c B. a<b<c C. b<c<a D. b>c>a 解析:对于相同条件下的同一物质来说,气态物质具有的能量最高,液态物质次之,固态物质具有的能量最低。根据△H=E产-E反,所以a=E[SO2(l)]-E[S(g)]-E[O2(g)],b=E[SO2(g)]-E[S(g)]-E[O2(g)],c=E[SO2(g)]-E[S(s)]-E[O2(g)],所以a-b=E[SO2(l)]-E[SO2(g)]<0,b-c=E[S(s)]-E[S(g)]<0,故a<b<c。 答案:B 变式练习4.在相同温度下,下列两个反应放出的热量分别用Q1和Q2表示, 2H2(g)+O2(g)===2H2O(g)+Q1; 2H2(g)+O2(g)===2H2O(l)+Q2,则Q1和Q2的关系是( ) A. Q1=Q2 B. Q1>Q2 C. Q1<Q2 D. 2Q2=Q1 【分析】物质的聚集状态不同,放出或吸收的热量不同。水从气态到液态要放热。 【答案】当物质由气态转变为液态时(水蒸气转变为液态水),分子间相互吸引力加强,要放出能量,所以选C。 【强调】物质的聚集状态不同,放出或吸收的热量不同,物质由一种状态转变为同温度下另一种状态
,而物质分子不发生变化的过程叫相变,变化过程中变化的能量叫做相变热。当物质由气态转变为液态时, [如H2O (g)→ H2O (l)],分子间相互吸引力加强,要放出能量;当物质由液态转变为气态时 [如H2O (l)→ H2O (g)],分子间相互排斥加强,要吸收能量。 4.已知:2H2(g)+O2(g)=2H2O(g)+Q1 2H2(g)+O2(g)=2H2O(l)+Q2 2CO(g)+O2(g)=2CO2(g)+Q3 欲得到相同的热量,所需CO和H2的体积比为 。 【分析】请仔细观察分析已知条件中的有关CO,H2分别燃烧的化学方程式,从中找出规律,便可得出正确结果。 【答案】因为CO和H2分别燃烧均为2mol,放出热量为Q3和Q1,所以Q3:Q1=n(CO):n(H2)=V(CO):V(H2) 故正确答案为Q3:Q1 【强调】抓CO、H2分别完全燃烧的特征是速解此题的捷径。 变式练习5.已知下列两个热化学方程式: 2H2(g)+O2(g)=2H2O(l) △H=—571.6kJ· mol—1 C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=—2220.0kJ· mol—1 实验测得H2与C3H8的混合气体共5mol,完全燃烧时放热3847kJ,则混合气体中H2与C3H8体积比是 A. 1:3 B. 3:1 C. 1:4 D. 1:1 【分析】可根据所给热化学方程式及反应热数值分别求出1mol H2和1mol C3H8完全燃烧各自放出的热量,然后再求混合物的组成。 【答案】 设H2的物质的量为x,则C3H8的物质的量为5-x,则(571.6÷2)x +2220×(5-x)=3847 所以x=3.75mol,由体积之比等于物质的量之比3.75:(5-3.75)=3:1 选B
