实验二 化学反应摩尔焓变的测定
一、实验目的
1.了解化学反应焓变或反应热效应测定的原理和方法。
2.学习用作图外推的方法处理实验数据。
3.练习准确浓度溶液配制的基本操作。
二、教学形式
1.讲解与提问
(1)用量热计测定化学反应焓变或反应热效应的简单原理和方法。
(2)试验中所用的锌粉为什么可用台秤称量,而所需CuSO4·5H2O却要在分析天平上称 取?所用的锌粉为什么要过量?
(3)怎样用减量法称取CuSO4·5H2O试样?如何配制250mL约0.2000mol/LCuSO4溶液?
(4)移液管和容量瓶的使用
(5)本实验成败的关键是什么?
2.基本操作与实验技能示范
(1)量热计装置的要求:
以盖上盖后能搅拌自如,温度计插至量热计较深处而不与量热计底及搅拌器相碰。
(2)讲解测定过程及作图法外推求ΔT值的方法及其必要性。
(3)介绍移液管的使用和溶液的配制方法。
3.注意事项与可能发生的问题
(1)测定所用的量热器必须洁净干燥,若有水珠可用滤纸擦干。
(2)溶解CuSO4·5H2O需用小烧杯,每次加水需少量多次。
(3)用移液管移取CuSO4溶液前,需先洗净移液管,并用所配制的CuSO4溶液洗涤3次,方可移液,并要将溶液倒入小烧杯中移液。以免因水带入而使CuSO4溶液的浓度变小,引起测定误差。
(4)锌粉倒入溶液中时,动作要迅速,并立即将盖盖紧,同时进行搅拌,揿下秒表计时。
4.测定时,反应速度转慢,为保证反应体系的均匀性,搅拌必须充分,因而搅拌器的环圈(搅拌浆或搅拌子)要适当大些以保证搅拌效果,反应完毕溶液应无蓝色。
5.本实验应用1/10度刻度温度计,读至小数点后二位。
6.根据实验数据用坐标纸作图时要注意比例尺的选择,使其与测量精度一致。所作之图应为一条光滑的曲线,而有些同学易将标上的各点画成连接各点的折线。
三、教学检查
1.两人合配一个溶液,测定一组时间对温度的数据,根据测定数据各自作图计算ΔH和Cp,独立完成实验报告。
2.锌与硫酸铜溶液的置换反应热ΔH=-216.8kJ/mol,ΔH的测定值要求-206.0~-228.0kJ/mol
本实验测得的ΔH的绝对值一般偏小,主要原因是由于量热计的绝热效果不佳,致使热量散失,另外操作不慎造成溶液外溢等。
四、思考题
1.为什么实验中锌粉用台秤称量,而CuSO4·5H2O要用分析天平称量?
2.实验中所用量热计、移液管和容量瓶各应如何洗涤?
第二篇:化学反应焓变的计算
一、课题:反应焓变的计算 二、课型:复习课
三、课程标准与考纲要求:
1、掌握盖斯定律,并会计算反应焓变。
2、培养学生学习化学的兴趣,培养创新精神和实践能力。
四、知识要点扫描:
中华第一考P234四、反应焓变的计算
五、考点解析与典例精讲:
考点一、焓变的计算
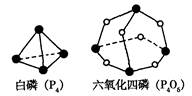 例1、化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量。已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(KJ·mol–1)P–P:198 P–O:360 O–O:498 则反应P4(白磷)+ 3O2→P4O6 的反应热△H为( )
例1、化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量。已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(KJ·mol–1)P–P:198 P–O:360 O–O:498 则反应P4(白磷)+ 3O2→P4O6 的反应热△H为( )
A.+1638KJ·mol–1 B.–1638KJ·mol–1
C.+126KJ·mol–1 D.–126KJ·mol–1
解析:
考点二、盖斯定律
例2、盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:___________________
解析:
考点三、综合应用
例4、火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为 。
(2)又已知H2O(l) = H2O(g) ΔH= +44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
解析:
六、当堂训练:
1.下列叙述正确的是( )
A.电能是二次能源 B. 水力是二次能源C.天然气是二次能源 D. 水煤气是一次能源
2.下列说法正确的是( )
A.物质发生化学变化都伴随着能量变化 B.任何反应中的能量变化都表现为热量变化
C.伴有能量变化的物质变化都是化学变化
D.即使没有物质的变化,也可能有能量的变化
3.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
4.下列各组热化学方程式中,△H1>△H2的是( )
①C(s)+O2(g)===CO2(g) △H1 C(s)+O2(g)===CO(g) △H2
②S(s)+O2(g)===SO2(g) △H1 S(g)+O2(g)===SO2(g) △H2
③H2(g)+O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
④CaCO3(s)===CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)===Ca(OH)2(s) △H2
A.① B.④ C.②③④ D.①②③
5.已知H2(g)+Cl2(g)=2HCl(g) △H=―184.6kJ·mol-1, 则反应HCl(g)=1/2H2(g)+1/2Cl2(g)的△H为( )
A.+184.6kJ·mol-1 B. ―92.3kJ·mol-1 C. ―369.2kJ·mol-1 D. +92.3kJ·mol-1
6.下列反应中生成物总能量高于反应物总能量的是( )
A.碳酸钙受热分解 B.乙醇燃烧 C.铝粉与氧化铁粉末反 D.氧化钙溶于水
7.25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )。
A.2H2(g)+O2(g)==2H2O(1) △H= ―285.8kJ/mol
B.2H2(g)+ O2(g)==2H2O(1) △H= +571.6 kJ/mol
C.2H2(g)+O2(g)==2H2O(g) △H= ―571.6 kJ/mol
D.H2(g)+ O2(g)==H2O(1) △H = ―285.8kJ/mol
O2(g)==H2O(1) △H = ―285.8kJ/mol
8.氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:
H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ/mol
CO(g)+1/2O2(g)=CO2(g) △H=-283.0kJ/mol
C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(l) △H=-5518kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-89.3kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( )
A. H2(g) B. CO(g) C. C8H18(l) D. CH4(g)
七、反思与总结:
一课一练
1、已知热化学方程式:SO2(g)+  O2(g)
O2(g)  SO3(g) △H = ―98.32kJ/mol
SO3(g) △H = ―98.32kJ/mol
在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为 ( )。
A. 196.64kJ B. 196.64kJ/mol C. < 196.64kJ D. > 196.64kJ
2、已知:CH4(g)+2O2(g)==CO2(g)+2H2O(1) △H = ― Q1 KJ/mol
2H2(g)+O2(g)==2H2O(g) △H = ―Q2 KJ/mol
2H2(g)+O2(g)==2H2O(1) △H = ―Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则放出的热量为( )KJ。
A. 0.4Q1+0.05Q3 B. 0.4Q1+0.05Q2 C. 0.4Q1+0.1Q3 D. 0.4Q1+0.1Q2
3、石墨和金刚石都是碳的单质,石墨在一定条件下可转化为金刚石。已知把石墨完全转化为金刚石时,要吸收能量,下列说法正确的是( )
A.石墨不如金刚石稳定 B.金刚石不如石墨稳定
C.等质量的金刚石与石墨完全燃烧,放出的能量一样多
D.等质量的金刚石与石墨完全燃烧,石墨放出的能量少
4、25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是( )
A.C(s)+ O2(g)=CO(g) △H= ―393.5 kJ/mol
O2(g)=CO(g) △H= ―393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(l) △H= +571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= ―890.3 kJ/mol
D.C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) △H= ―2800 kJ/mol
5、根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H =―Q1 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l) △H =―Q2 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g) △H =―Q3 kJ/mol
判断Q1、Q2、Q3三者关系正确的是( )
A. Q1>Q2>Q3 B. Q1>Q3>Q2 C. Q3>Q2>Q1 D. Q2>Q1>Q3
6、在36 g 碳不完全燃烧所得气体中,CO占1/3体积,CO2占2/3体积,且
C(s) +1/2O2(g) = CO(g) △H = -110.5 kJ/mol
CO(g) + 1/2O2(g) = CO2(g) △H = -283 kJ/mol
与这些碳完全燃烧相比,损失的热量是( )
A.172.5 kJ B. 1149 kJ C. 283kJ D. 517.5 kJ
7、完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是( )
A. 0.2Q B. 0.1Q C. 5Q D. 10Q
答案
例2、(1)N2H4(l)+2H2O2(l) = N2(g) +4H2O(g) △H=-644.25 KJ/mol
(2)410.125 (3)产物不会造成环境污染。
例3、CO(g)+FeO(s) == Fe(s)+CO2(g) △H=―218.0kJ/mol

