实验 2-7 盐酸标准溶液的配制与标定
 一、实验目的
一、实验目的
1.掌握盐酸标准溶液的配制与标定方法;
2.熟悉甲基橙指示剂的使用条件以及指示滴 定终点的判断。
二、实验原理
配制方法:间接配制法,先配制近似浓度,再进行标定。 因 HCl易挥发
标 定方法:基准物质:Na2CO3,指示剂 :甲基橙,变色范围 pH值为 3. 1(黄色)~4.4(红
色),溶液由黄色刚变至橙色。
三、实验试剂
2 3
用, 一周内有效)。
2.HCI溶液:6mol.L 。
3.甲基橙指示剂:1 g.L 。
四、实验操作复习
1.容量瓶的操作
(1)检漏:盛水到刻度附近 ,塞好瓶塞,按紧瓶塞,使瓶倒立,观赛是否漏水。
(2)溶解:在小烧杯溶解完 全。
(3)定量转移:借助玻 棒,将烧杯的溶液沿玻棒转移入容量瓶。溶液转移后 ,将烧杯沿玻
棒微 微上提,同进使烧杯直立,避免沾在 杯口的液滴流到杯外,再将玻棒放回 烧杯。用洗瓶渔
翁洗 烧杯内壁和玻棒,并转移入容量瓶内,反复四、五次, 以保证转移完全。
(4)定容:加入蒸馏水至 大半瓶,摇动,再加到离刻度 0.5cm处,再 用小滴管滴加至弯月
面 相切。盖好瓶 塞,左手食指压 住塞子,其余四 指握住颈部,右 手(五只手指)将容量瓶 托住并
反复 倒置,摇荡使溶液完全均匀.。
2.移液管操作复习(提问 )
(1)操作姿势:哪个手拿 移液管,哪个手拿吸耳球?
(2)吸液操作:移液管垂 直,调整液面时移液管嘴贴容器的内壁。
(3)放液操作:移液管 垂直,移液管嘴贴接受容器的内壁,不用吹。
3.滴定管操作复习(提问 )
(1)锥形瓶与操作台、 滴定管的位置。
(2)操作姿势:哪个手 拿锥形瓶。哪个手控制滴液?
(3)控制活塞或玻璃珠 的操作。
(4)摇动锥形瓶的操作 。
(5)加入标准溶液的操作,每次滴 定前要重新加入标准溶液,并调节 液面到上一次相近的
位置。
(6)读数操作:用手垂直拿滴定管,读数准确 至 0.01mL,即 2个刻度之间分为 10个小格
进行读数。
五、实验步骤
1. HCl溶液(0.1mol.L)的配制
用 lOmL量筒量取 6mol.L HCl 8.3mL。倾人玻瑞试剂瓶中,用水荡洗 量筒数次,洗液并
人上 述试剂瓶中,加水稀释至 500ml.摇匀后备用。
2. HCl溶液(0.1mol.L)浓度的标定
(1) Na2CO3 标 准 溶液 (0.05mol.L )的 配制 用减 量 法在 分 析天 平 上 称取 无 水 Na2CO3
1.3g(精确至 0.1mg)于 100 mL烧杯中,加人约 50 mL水,用玻瑞棒轻轻搅拌至完全溶解后,转
移至 250mL容量瓶中,用水定 容,备用。根据所称 Na2CO3 基准物的质量计算出自配的 Na2CO3
1(实验 2-7)

 标准 溶液的准确浓度。
标准 溶液的准确浓度。
(2) HC1溶液的标定
用 25mL移液管移取 25.00mL上述 Na2
CO3
标准溶液,置入 250mL
锥形 瓶中,加入 1~2滴甲基橙指示剂,用待标定的 HCl溶液滴定至溶液由 黄色刚变为橙色为
终点 ,记录消耗 HCl溶液的体积。平行测定 3次,计算所配制 HC1溶液的浓度。
(3)贴上标签,写上姓名、班别和“保存到 20##年 10月 31日”,放在实验柜中,留到“实
验 2-9 工业碳酸钠总碱量的测定”和“实验 2-10 混合碱的组成及各组 分含量的测定——双指
示剂法 ”的实验使用。
五 、数据处理
参 照下表记录实验数据并计算 HCl溶液的浓度
Na
2CO
3
 溶液浓度的计算公式如 下:
溶液浓度的计算公式如 下:
2 3
=
m
Na2CO
3
M
Na2CO3
´V
Na2CO3
七、思考与讨论
最少要提出和回答 1个问题。
2(实验 2-7)
第二篇:实验二 盐酸标定溶液的配制和标定
实验二 盐酸标准溶液的配制和标定,NaOH溶液浓度的测定
一、原理
首先配制约0.1mol/L的盐酸溶液,然后以甲基橙作指标剂,用已知准确浓度的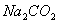 标准溶液来标定盐酸的准确浓度。利用此HCl溶液测定NaOH溶液的浓度。
标准溶液来标定盐酸的准确浓度。利用此HCl溶液测定NaOH溶液的浓度。

二、试剂
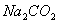 基准物:分析纯; 浓盐酸(比重1.19,):分析纯; 0.1%甲基橙:称取0.1g甲基橙,溶于100mL蒸馏水中。
基准物:分析纯; 浓盐酸(比重1.19,):分析纯; 0.1%甲基橙:称取0.1g甲基橙,溶于100mL蒸馏水中。
三、测定步骤
(一)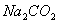 标准溶液的配制——直接法
标准溶液的配制——直接法
在分析天平上,用差减法称取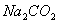 约1.2g~1.4g(准确至0.0001g)于小烧杯中,加入约50mL蒸馏水,用玻璃棒搅拌,使其完全溶解,然后全部转移到250mL容量瓶中,用水稀释到刻度。盖好瓶塞,摇匀。
约1.2g~1.4g(准确至0.0001g)于小烧杯中,加入约50mL蒸馏水,用玻璃棒搅拌,使其完全溶解,然后全部转移到250mL容量瓶中,用水稀释到刻度。盖好瓶塞,摇匀。
 (mol/L)
(mol/L)
式中: m——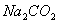 的重量(g)
的重量(g)
M——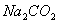 的分子量;
的分子量;
V——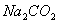 的溶液的体积,即容量瓶的体积(mL)
的溶液的体积,即容量瓶的体积(mL)
(二)0.1mol/L HCl溶液的配制及标定——间接法
HCl溶液的配制:
用小量筒量取浓盐酸约4.5mL于500mL清洁的试剂瓶,加蒸馏水至500mL。
HCl溶液浓度的标定:
用移液管准确吸取25.00mL已知准确浓度的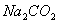 溶液于250ml锥形瓶中,加入甲基橙指标剂两滴,用HCl溶液滴定至溶液颜色由黄色变为橙红色且摇动不消失即为滴定终点,记录滴定管的终点读数,终点读数与起始读数之差,即为滴定所用HCl溶液的体积。平行做三份,滴定的相对平均偏差不应超过0.2%。
溶液于250ml锥形瓶中,加入甲基橙指标剂两滴,用HCl溶液滴定至溶液颜色由黄色变为橙红色且摇动不消失即为滴定终点,记录滴定管的终点读数,终点读数与起始读数之差,即为滴定所用HCl溶液的体积。平行做三份,滴定的相对平均偏差不应超过0.2%。
(三)NaOH溶液的浓度的测定
取25.00mlNaOH溶液三份分别置于250ml锥形瓶中,加入1~2滴甲基橙指示剂,用HCl标准溶液滴定至橙色即为终点。滴定的相对平均偏差不应超过0.2%。
四、原始数据及数据处理
1.HCl溶液浓度的计算

2.NaOH溶液浓度的计算(要计算结果的平均值及相对平均偏差)
请大家注意,做《HCl溶液的配制、标定及测定NaOH浓度》这个实验时,要求一个大桌四个组的数据(NaOH浓度,4*3=12个)集中起来做数据处理,计算结果包括平均值、标准偏差、置信区间,还要考虑可疑值的剔除。
