有机化学实验指导
《有机化学实验》是食品科学与工程、生物工程和环境工程等专业一门重要的实验课程,是实践教学不可缺少的一个重要环节。
其主要内容包括有机化学实验的一般知识、基本操作和实验技术、有机化合物的制备及有机化合物的性质实验,天然产物的分离提取等。
实验课的任务不仅是验证、巩固和加深理论性教学所学到的基本理论知识,更重要的是培养学生实验操作能力,综合分析问题和解决问题的能力,养成严肃认真、事实求是的科学态度和严谨的工作作风,从而使学生在科学方法上得到初步的训练。
一、 有机化学实验课程的目的要求
1、有机化学实验的目的:
通过实验,获得感性认识,以建立对有机化学中某些基本概念,基本理论的深入理解;掌握有机实验的基本知识和操作技能;掌握重要有机化合物的制备方法;培养严谨的科学态度,良好的实验素养,以及分析问题和解决问题的能力,并为有关的后续课和将来走上工作岗位奠定良好的基础。
2、有机化学实验的要求:
通过实验要求学生较牢固地掌握常见有机化合物的主要性质;掌握主要有机化合物的制备原理、方法和技能;掌握有机实验中的一些基本操作,正确使用某些玻璃仪器和测量仪器,具备安装实验装置和使用精密仪器的初步能力;了解重要天然有机物的提取、纯化技术。加深对有机化学中的一些基本概念和基本原理的理解。
3、开设的实验个数与总教学时数:
总学时数:18学时
实验总数:6个
二、面向专业、年级
有机化学实验面向食品科学与工程、生物工程、环境工程等专业。在一年级的第二学期或二年级的第一学期与有机化学理论课同步开设。
三、实验内容和课时安排

四、教学原则和教学方法
有机化学实验课程在教师指导下进行。每位学生一套磨口仪器,各自独立完成实验内容。每个标准实验班人数为15人。
五、成绩考核方法
有机化学实验成绩实行等级制,考核方式合计分实行“基础化学实验课考试方法”。具体计分为:
平时实验成绩占40%,期末实验考核占30%,期末理论知识考核占30%。
实验考核主要包括以下几个部分:实验预习、实验操作、实验结果、实验报告。
六、实验教材及主要参考书目
教 材:
兰州大学、复旦大学有机化学教研室主编《有机化学实验》,高等教育出版社,1994年版。
主要参考书:
(1)曾昭琼主编《有机化学实验》,高等教育出版社,1987年4月第二版。
(2)高复兴等主编《有机化学实验》,河南大学出版社,1999年第一版。
(3)刘约权 李贵深主编《实验化学》,高教出版社、1999年10月第一版
有机化学实验的一般知识
有机实验规则
为了保证有机化学实验课正常,有效,安全地进行,保证实验课的教学质量,学生必须 遵守下列规则: 1.认真预习 在进入有机实验室之前,必须认真阅读本章内容,了解进入实验室后应注意的事项及有关规定.每次做实验前认真预习实验教材,复习有机化学教材中的有关章节,明确实验的目的和要求,弄清原理和操作步骤,了解实验的关键和注意事项。
2.注意安全 实验室是学生进行化学知识学习和科学研究的场所,必须严肃、认真。做化学实验期间必须穿工作服,不准穿拖鞋。了解实验室水、电、气(煤气)总开关的地方,了解消防器材(消火栓、灭火器等)、紧急急救箱装置的摆放位置和正确使用方法以及安全通道。禁止在实验室内吃食品、喝水、咀嚼口香糖等。在实验内不允许嬉闹、高声喧华,也不允许带耳机边听边做实验。任何有关实验安全问题,皆可询问指导老师。出现意外情况,应立即报告指导教师,即时处理。
3.规范操作 实验时要听从老师指导,严格按操作规程进行操作,不得随意改动,若因客观条件不同需要改动,须事先取得指导教师同意。及时、如实地在专用记录本或记录纸上记录观察到的现象并做出科学的解释。
4.保持实验室整洁 实验室的废弃物要按指导教师要求放在指定的废物收集器内。实验完毕要将实验仪器清洗干净,关好水电、气开关和做好清洁卫生。实验结束后,由指导老师签字,方可离开实验室。
实验室安全知识
(一)、实验者到实验室进行实验前,应首先熟悉仪器设备和各项急救设备的使用方法,了解实验楼的楼梯和出口,实验室内的电气总开关、灭火器具和急救药品在什么地方,以便一旦发生事故能及时采取相应的防护措施。
(二)、大多数化学药品都有不同程度的毒性,原则上应防止任何化学药品以任何方式进入人体。必须注意,有许多化学药品的毒性,是在相隔很长时间以后才会显示出来的;不要将使用小量、常用化学药品的经验,任意移用于大量化学药品的情况;更不应将常温、常压下试验的经验,在进行高温、高压、低温、低压的试验时套用;当进行有危险性或在严酷条件下的反应时,应使用防护装置,戴防护面罩和眼镜。
(三)、美国职业安全与健康事务管理局(OSHA)颁布了有致癌变性能的化学物质[见Chemistry and Engineering News,p.20,July 31,(1978)]。因此实验时应尽量少与这些物质接触,实在需要使用时应带好防护手套,并尽可能在通风橱中操作。这些物质中特别要注意的是苯、四氯化碳、氯仿等常见溶剂,所以实验时通常用甲苯代替苯,用二氯甲烷代替四氯化碳和氯仿。
(四)、许多气体和空气的混合物有爆炸组分界限,当混合物的组分介于爆炸高限与爆炸低限之间时,只要有一适当的灼热源(如一个火花,一根高热金属丝)诱发,全部气体混合物便会瞬间爆炸。某些气体与空气混合的爆炸高限和低限,以其体积分数表示,列表如表1。因此实验时应尽量避免能与空气形成爆鸣混合气的气体散失到室内空气中,同时实验室工作时应保持室内通风良好,不使某些气体在室内积聚而形成爆鸣混合气。实验需要使用某些与空气混合有可能形成爆鸣气的气体时,室内应严禁明火和使用可能产生电火花的电器等,禁穿鞋底上有铁钉的鞋子。
表1 与空气混合的某些气体的爆炸极限(20℃,p0)

(五)、在化学实验中,实验者要接触和使用各类电气设备,因此必须了解使用电气设备的安全防护知识:
1.实验室所用的市电为频率50Hz的交流电。人体感觉到触电效应时电流强度约为1mA,此时会有发麻和针刺的感觉。通过人体的电流强度到了6.9mA,一触就会缩手。再高电流,会使肌肉强烈收缩,手抓住了带电体后便不能释放。电流强度达到50 mA时,人就有生命危险,因此使用电气设备安全防护的原则,是不要使电流通过人体。
2.通过人体的电流强度大小,决定于人体电阻和所加的电压。通常人体的电阻包括人体内部组织电阻和皮肤电阻。人体内部组织电阻约1000Ω,皮肤电阻约为1kΩ(潮湿流汗的皮肤)到数万欧姆(干燥的皮肤)。因此我国规定36V 50Hz的交流电为安全电压,超过45V都是危险电压。
3.电击伤人的程度与通过人体电流大小、通电时间长短、通电的途径如何有关。电流若通过人体心脏或大脑,最易引起电击死亡。所以实验时不要用潮湿有汗的手去操作电器,不要用手紧握可能荷电的电器,不应以两手同时触及电器,电器设备外壳均应接地。万一不慎发生触电事故,应立即切断电源开关,对触电者采取急救措施。
有机实验室常用仪器设备与使用
一般来说,有机实验室里常用的玻璃仪器和设备,可分为公共和个人使用两大类。若进一步划分,又可分为玻璃仪器和非玻璃仪器。玻璃仪器容易打碎,一般都由个人使用。公用的玻璃仪器,如旋转蒸发仪等,都是比较笨重和结实的。无论从经济角度还是从方便使用角度看,都应不要损坏仪器和设备。
玻璃仪器
有机化学实验室玻璃仪器可分为普通玻璃仪器和磨口玻璃仪器。
标准接口玻璃仪器是具有标准化磨口或磨塞的玻璃仪器。由于仪器口塞尺寸的标准化、系统化、磨砂密合,凡属于同类规格的接口,均可任意连接,各部件能组装成各种配套仪器。与不同类型规格的部件无法直接组装时,可使用转换接头连接。使用标准接口玻璃仪器,既可免去配塞子的麻烦手续,又能避免反应物或产物被塞子玷污的危险,口塞磨砂性能良好,使密合性可达较高真空度,对蒸馏尤其减压蒸馏有利,对于毒物或挥发性液体的实验较为安全。
标准接口玻璃仪器,均按国际通用的技术标准制造,当某个部件损坏时,可以选购。
标准接口仪器的每个部件在其口塞的上或下显著部位均具有烤印的白色标志,表明规格。常用的有10,12,14,16,19,24,29,34,40等。
下面是标准接口玻璃仪器的编号与大端直径:

有的标准接口玻璃仪器有两个数字,如10/30,10表示磨口大端的直径为10mm,30表示磨口的高度为30mm。
使用标准接口玻璃仪器应注意以下几点:
(1)磨口塞应经常保持清洁,使用前宜用软布揩拭干净,但不能附上棉絮。
(2)使用前在磨砂口塞表面涂以少量凡士林或真空油脂,以增强磨砂口的密合性,避免磨面的相互磨损,同时也便于接口的装拆。
(3)装配时,把磨口和磨塞轻轻地对旋连接,不宜用力过猛。但不能装得太紧,只要达到润滑密闭要求即可。
(4)用后应立即拆卸洗净。否则,对接处常会粘牢,以致拆卸困难。
(5)装拆时应注意相对的角度,不能在角度偏差时进行硬性装拆,否则极易造成破损。
磨口套管和磨塞应该是由同种玻璃制成的。
实验一 蒸馏和沸点的测定
【实验目的】
1. 了解测定沸点的意义和蒸馏的意义
2. 掌握常量法(即蒸馏法)测定沸点的原理和方法。
【实验原理】
1. 纯净的液体有机物在一定压力下具有固定的沸点。沸点是液体有机化合物的物理常数之一,因此通过测定沸点可以鉴别有机化合物并判断其纯度。
2. 利用蒸馏可将沸点相差较大(如相差30℃)的液体混合物分开。液体混合物加热后沸点较低者先蒸出、沸点较高者随后蒸出、不挥发的留在蒸馏瓶内,这样可以达到分离提纯的目的。
【课堂内容】
通过提问检查学生预习情况,提问内容如下:
1)测沸点有何意义?
2)什么是沸点?纯液态有机化合物的沸程是多少?
3)什么是蒸馏?蒸馏的意义?
4)什么是爆沸?如何防止爆沸?
5)沸石为什么能防止爆沸?
6)蒸馏的用途?
7)何时用常量法测沸点何时用微量法测沸点?
8)有机实验室常用的热源?加热的方式有几种?
11)热浴的方式有几种?
12)安装、拆卸仪器装置的顺序是什么?
13)冷凝管的种类有几种?
14)蒸馏物的体积是多少?
16)蒸馏装置中温度计的位置是怎样的?
【实验仪器及设备】
1. 150mL圆底烧瓶19#
2. 蒸馏头19#×3或19#×2×14#
3. 温度计套管19# 或14#
4. 温度计100℃
5. 直形冷凝管(短的)19#×2
6. 接尾管19#×2
7. 100 mL三角瓶1个
8. 100 mL烧杯1个
9. 100 mL量筒
10. 沸点管,温度计100 ℃,胶塞,沸石,乳胶套圈
11. 升降架2个
12. 250 mL加热套,三角架,s扣,夹子。
【药品】
1. 工业酒精75ml/人
【实验装置图】

【实验内容】
常量法测乙醇的沸点,蒸馏75ml工业酒精。
【测得结果】 乙醇的沸程为:77~79 ℃(理论值78.4 ℃)
【注意事项】
1. 仪器安装要严密、正确。
2. 注意安装拆卸的顺序。
3. 加热前放沸石,通冷凝水。
4. 准确量取75ml工业酒精,蒸馏速度1-2 d/s
5. 不许蒸干,否则易发生事故(瓶碎裂等)
6. 液体沸点在80 ℃以下的液体用水浴加热蒸馏。
【实验要求】
回收产品,教师验收产品的回收量。上交实验报告。
*实验二 溴乙烷
【实验目的】
学习以醇为原料制备溴乙烷的实验原理和方法,学习低沸点蒸馏的基本操作,巩固分液漏斗的使用方法。
【实验原理】
主反应:

副反应:

【仪器与药品】
仪器:有机合成制备仪器
100 mL圆底烧瓶2个;150 mL锥形瓶2个;空心塞1个;500 mL烧杯1个;真空接液管1个;75°弯头;蒸馏头;直形冷凝管;温度计100 ℃ 1个;温度计套管;分液漏斗2个;量筒10 mL ;加热套250 mL,滴管。
药品:95 %乙醇,浓硫酸,溴化钠固体。
【实验装置图】
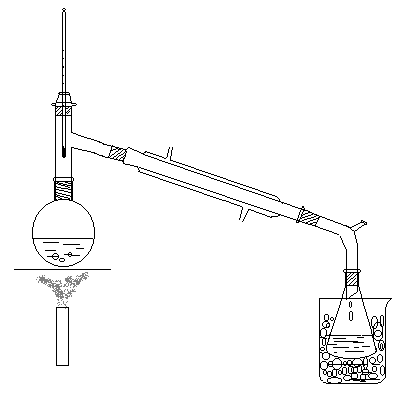
【物理常数】

【实验步骤】
在100 mL 园底烧瓶中加入10 mL 95% 乙醇,及9 mL 水,在不断振摇和冷水冷却下,漫漫加入19 mL 浓硫酸,冷至室温后,在冷却下加入15g 研成细粉状的溴化钠,稍加振摇混合后,加入几粒沸石,安装成常压蒸馏装置(参见装置图)。接受器内外均应放入冰水混合物,以防止产品的挥发损失。接液管的支管用橡皮管到入下水道或室外。将反应混合物在石棉网上小火加热蒸馏,使反应平稳发生,直至无油状物馏出为止。
将馏出液倒入分液漏斗中,分出的有机层置于150mL干燥的锥形瓶中,在冰水浴中,边振摇边滴加浓硫酸,直至锥形瓶底分出硫酸层为止。用干燥的分液漏斗分去硫酸液,将溴乙烷粗产品倒入干燥的蒸馏瓶中,水浴加热蒸馏,接受器外冰水浴冷却,收集37~40 ℃的馏分。称量、计算产率。
纯溴乙烷的b.p. 38.4 ℃, 1.4239。
1.4239。
【课堂提问内容】
1.已学过的制备卤代烃的方法有哪些?
2.合成溴乙烷时加水的目的是什么?
3.接引管的支口用橡皮管导入下水道或室外,为什么?
4.为什么用小火加热使反应平稳发生?
5.在精制与制备产品时应注意的事项有哪些?
【注意事项】
1.装置要严密。
2.加浓硫酸要边加边摇变冷却,充分冷却后(在冰水浴中)再加溴化钠,
以防反应放热冲出。
3.加热要先小火,逐渐稍大,使反应平稳发生,避免大火,否则产物损
失,并有副产物生成。
4.精制时要先彻底分去水,冷却下加硫酸,否则加硫酸产生热量使产物挥
发损失。
5.最后蒸馏注意干燥。
6.产物验收质量或体积及折光率。
【讨论】
溴乙烷产量低的原因?
【实验要求】
测产物的折光率,计算产率,上交实验报告。
实验三 乙酸乙酯的制备
【实验目的】
掌握实验室制备乙酸乙酯的原理与方法,初步掌握低沸点易燃液体的操作要点。
【实验原理】
主反应:

副反应:


【仪器与药品】
仪器:
加热套;250 mL三口瓶;75°弯头;直形冷凝管;真空接尾管;150 mL锥形瓶;真空塞;125 mL滴液漏斗(以上均为19#);温度计(200℃、100℃); 500 mL烧杯2个;量筒(10mL、100mL);125mL分液漏斗;蒸馏头19#。
药品:
95%乙醇;浓硫酸;饱和碳酸氢钠溶液;饱和氯化钠溶液;饱和氯化钙溶液;无水硫酸镁。
【物理常数】

【实验装置图】

【实验步骤】
1. 合成
在100 mL干燥的三颈瓶19# 中加入9 mL 95 %乙醇,将烧瓶浸入冰水入中
冷却,缓慢加入12mL浓硫酸混匀,在滴液漏斗内加入由14mL 95 %乙醇和14.3ml冰醋酸组成的混合液,漏斗脚末端与温度计的水银球必须浸入液面以下距瓶底约0.5~1cm,加入2 粒沸石,接受器浸入冰水中冷却,接尾管的支管接橡皮管通入下水道。
先向三颈瓶中加入3-4mL混合液,然后将三颈瓶用加热套小心加热至110-120℃左右,这时蒸馏口应有液体流出,再自滴液漏斗慢慢滴加其余的混合液,控制滴加速度与馏出速度大致相等(1d/s),维持反应温度在110~125 ℃,约0.5 h滴加完毕,再继续加热,直到温度上升到130 ℃不在有馏出液为止,去掉热源停止反应。
2. 精制
用10 mL饱和碳酸氢钠溶液中和到无二氧化碳气体逸出,酯层用10 mL饱和NaCl溶液、10mL×2饱和CaCl2溶液洗涤。无水硫酸镁干燥0.5 h,在水浴中蒸馏,收集沸点在73~78 ℃的馏分。
【注意事项】
1.分批加浓硫酸,边加边摇边冷却,防止乙醇氧化。
2.装置要严密,反应完后要先停火,稍冷却后再拆下接受器,防止产物挥发。
3.控制好反应温度及滴加乙醇的速度1d/s。
4.洗涤时注意顺序,室内无明火。
5.分净水后用无水硫酸镁干燥约20~30分钟。
6.产品验收体积和沸点。
【实验要求】
测定产品的折光率,计算产率,上交实验报告。
实验四 重结晶提纯法
【实验目的】
1.学习重结晶法提纯固体有机化合物的原理和方法。
2.掌握固体有机物的提纯操作方法。
3.掌握抽滤、热过滤操作和扇形滤纸的折叠方法。
【实验原理】
意义:从有机合成反应分离出来的固体粗产物往往含有未反应的原料、副产物及杂质,必须加以分离纯化,重结晶是分离提纯纯固体化合物的一种重要的、常用的分离方法之一。
适用范围:它适用于产品与杂质性质差别较大、产品中杂质含量小于5 %的体系。
原理:利用混合物中各组分在某种溶剂中溶解度不同或在同一溶剂中不同温度时的溶解度不同而使它们相互分离。
【复习并提问】
① 液体有机化合物分离提纯的方法有哪些?(已学过的)。
② 固体化合物纯度检验方法是什么?
③ 液体化合物的检验方法是什么?
④ 重结晶的意义是什么?
⑤ 重结晶提纯法的一般过程是什么?
⑥ 理想溶剂必须具备的条件是什么?
⑦ 常用的溶剂及混合溶剂有哪些?
⑧ 溶剂选择的原理是什么?
⑨ 溶剂选择的方法是什么?
⑩ 使用活性炭脱色应该注意哪些问题?
【实验装置图】


图1. 重结晶热过滤装置 图2. 抽滤装置
【实验内容】
提纯粗制的乙酰苯胺
【实验步骤】
将2 g粗制的乙酰苯胺及计量的水加入100 mL的烧杯中,加热至沸腾,直到乙酰苯胺溶解(若不溶解可适量添加少量热水,搅拌并热至接近沸腾使乙酰苯胺溶解)。取下烧杯稍冷后再加入计量的活性炭于溶液中,煮沸5~10分钟。
趁热用热水漏斗和扇形滤纸进行过滤,用一烧杯收集滤液。在过滤过程中,热水漏斗和溶液均应用小火加热保温以免冷却。
滤液放置彻底冷却,待晶体析出,抽滤出晶体,并用少量溶剂(水)洗涤晶
体表面,抽干后,取出产品放在表面皿上晾干或烘干,测试熔点及红外光谱。
【注意事项】
1. 1. 用活性炭脱色时,不要把活性炭加入正在沸腾的溶液中。
2. 2. 滤纸不应大于布氏漏斗的底面。
3. 3. 停止抽滤时先将抽滤瓶与抽滤泵间连接的橡皮管拆开,或者将安全瓶上的活塞打开与大气相通,再关闭泵,防止水倒流入抽滤瓶内。
【思考题】
1. 简述重结晶过程及各步骤的目的。
2. 加活性炭脱色应注意哪些问题?
3. 如何选择重结晶溶剂?
4. 母液浓缩后所得到的晶体为什么比第一次得到的晶体纯度要差?
5. 使用有毒或易燃的溶剂进行重结晶时应注意哪些问题?
6. 样品量分别在多少时用常量法或半微量法进行重结晶?
7. 用水重结晶纯化乙酰苯胺时(常量法),在溶解过程中有无油珠状物出现?这是什么?如有油珠出现应如何处理?
8. 如何鉴定重结晶纯化后产物的纯度?
【实验要求】
上交产品及实验报告。
*实验五 萃取
【实验目的】
学习萃取的原理与方法,掌握分液漏斗的使用及影响萃取效率的因素。
【实验原理】
萃取:是利用物质在两种互不相溶(或微容)溶剂中溶解度或分配比的不同来达到分离提纯或纯化的一种操作。
 分配定律:
分配定律:

 = K(分配系数)
= K(分配系数)
若被萃取溶液的体积为V,被萃取溶液中溶质的总质量为W0,每次萃取所用溶剂B的体积均为S,经过n次萃取后溶质在溶剂A中的剩余量为Wn,则:

因为 KV∕KV+S恒小于1
所以 n越大, Wn越小。一般n = 3~5,即萃取3~5次。
萃取的目的:分离和提纯有机化合物,从液体中萃取常用分液漏斗。
【药品和仪器】
仪器:分液漏斗;锥形瓶2个 ;碱式滴定管。
药品:冰醋酸与水的混合溶液(冰醋酸:水 = 1:19);乙醚;0.2 mol/L NaOH; 酚酞指示剂。
【物理常数】

【药品用量】
① 取25 mL待萃取液。
② 一次萃取用乙醚10mL∕次,进行多次萃取用乙醚量为10mL∕次×3次。
【课堂提问内容】
1.萃取?意义?
2.萃取包括液—液萃取和液—固萃取,萃取常用的器皿?分液漏斗
3.分液漏斗的主要用途?分液漏斗的种类?
4.使用分液漏斗前应注意什么?
5.使用分液漏斗时应注意什么?
6.使用分液漏斗后应注意什么?
【增补内容】
1.具体操作
① 分液漏斗的选择:比待处理液体积大1-2倍。
② 将含有有机物的水溶液和萃取溶剂依次自上口倒入分液漏斗。
③ 萃取溶剂一般为溶液体积的1/3。
④ 放气、分离彻底,上层液体从分液漏斗倒出。
⑤ 萃取次数一般为3-5次。
⑥ 合并萃取液加入合适的干燥剂干燥,然后除去干燥剂,蒸去溶剂,即得到粗产品,再用重结晶或蒸馏等方法纯化。
【注意事项】
1.使用分液漏斗前要检查玻赛和活塞是否紧密,使用前要先打开玻塞再开启活塞。
2.漏斗向上倾斜,朝无人处放气。
3.分液要彻底,上层物从上口放出,下层物从下口放处。
【讨论】
影响萃取效率的因素有哪些?
【实验要求】上交实验报告
实验六 糖类物质的性质
【实验目的】
1.验证和巩固糖类物质的主要化学性质
2.熟悉糖类物质的某些鉴定方法。
【药品和仪器】
酒精灯、试管夹、试管、表面皿、坩埚。
葡萄糖、蔗糖、果糖、麦芽糖、乳糖、淀粉、费林试剂、本尼迪克试剂、硝酸银、氨水、氢氧化钠、α-萘酚乙醇试剂、硫酸、间苯二酚-盐酸试剂、盐酸碘试剂、棉花、硝酸、乙醇、乙醚、滤纸。
【实验步骤】
1.Molish试验—α-萘酚试验出糖
在试管中加入1ml 5%葡萄糖,滴入2滴10%α-萘酚和95%乙醇溶液,将试管倾斜450,沿管壁慢慢加入1ml浓硫酸,观察现象?若无颜色,可在水浴中加热,再观察结果?
试样:5%葡萄糖、果糖、麦芽糖、蔗糖、淀粉液、滤纸浆
2. 间苯二酚试验
在试管中加入间苯二酚2ml,加入5%葡萄糖溶液1ml,混匀,沸水浴中加热1-2min,观察颜色有何变化?加热20min后,再观察,并解释。
试样:5%葡萄糖、果糖、麦芽糖、蔗糖
3. Benedict试剂、Tollen试剂检出还原糖
(1)与Benedict试剂反应:取6支试管分别加入1ml Benedict试剂,微热至沸,分别加入5%葡萄糖溶液,在沸水中加热2-3min,放冷观察现象。
试样:5%葡萄糖、果糖、麦芽糖、蔗糖、乳糖、淀粉
(2)与Tollen试剂反应:取6支洁净的试管分别加入1.5mlTollen试剂,分别加入0.5ml5%葡萄糖溶液,在60-800C热水浴中加热,观察并比较结果,解释为什么?
试样:5%葡萄糖、果糖、麦芽糖、蔗糖、淀粉液、滤纸浆
4.糖脎的生成
取5支试管分别加入2ml苯肼试剂,分别加入5%葡萄糖、果糖、乳糖、麦芽糖、蔗糖液,沸水浴中加热,检查晶体形成及所需时间。
5. 淀粉水解
取1支试管加入3ml 淀粉溶液,加0.5ml稀盐酸,煮沸5min,冷却后,用10% NaOH中和,用此水解液作Fehling试验。
【实验要求】上交实验报告
实验七 旋光度的测定
【实验要求】
1. 了解旋光仪的构造。
2. 掌握使用旋光仪测定物质的旋光度。
3. 学习比旋光度和光学纯度的计算。
【计算公式】
比旋光度是物质特性常数之一,测定旋光度,可以检验旋光性物质的纯度和含量。
纯液体的比旋光度=[а]tλ=
溶液的比旋光度=[а]tλ=
样品的光学纯度=[а]tλ观测值/[а]tλ理论值*100%
【仪器与药品】
葡萄糖、容量瓶、旋光仪
【实验步骤】
1.接通电源,5min后钠光灯发光正常,即可开始测定。
2.旋光仪零点的校正:在测定样品前,需要先校正旋光仪的零点。
①将样品管洗好,左手拿住管子把它竖立,装上蒸馏水,使液面凸出管口。
②将玻璃盖沿管口边缘轻轻平推盖好,不能带入气泡,旋上螺丝帽盖,漏水,不要过紧。
③将样品管擦干,放入旋光仪内罩上盖子,,将标天盘调至零点左右,旋转粗动、微动手轮,使视场内Ⅰ和Ⅱ部分的亮度均一,记下读数。
④重复操作至少5次,取平均值,若零点相差太大时,应把仪器重新校正。
4. 旋光度的测定:准确称取0.1-0.5g样品(如葡萄糖)配成一定浓度的溶液,依上法测定其旋光度,这时所得的读数与零点之间的差值即为该物质的旋光度。
实验八 从茶叶中提取咖啡因
【实验目的】
1.通过从茶叶中提取咖啡因,掌握一种从天然产物中提取纯有机物的方法
2.学会使用索氏提取器和升华的基本操作。
【实验原理】
咖啡因具有刺激心脏、兴奋大脑和利尿作用,是心脏、呼吸器官和神经的兴奋剂。它是止痛片复方阿司匹林——APC(即阿司匹林—非那西汀—咖啡因)的一个组分。
咖啡因又称咖啡碱,是茶叶中含量较多的生物碱,化学名称为1,3,7—三甲基—2,6—二氧嘌呤,构造式如下:

咖啡因是弱碱性化合物,味苦,能溶于氯仿(室温时饱和浓度为12.5%),微溶于水和乙醇等。它为白色针状晶体,在100℃时失去结晶水,并开始升华,120℃时升华相当显著,178℃时迅速升华。
茶叶中含有多种生物碱,其中咖啡碱约占1%-5%,此外还合色素、纤维素、蛋白质等。在实验室从茶叶中提取咖啡因,常用索氏提取器连续提取。
【仪器与药品】
索氏(Soxhlet)提纯器、蒸发皿、茶叶、乙醇
【实验装置图】

【实验步骤】
1.Soxhlet提取法:称取10g茶叶,放入150ml Soxhlet提纯器中,在圆底烧瓶中加入80-100ml95%乙醇,水浴加热回流提取。直到提取液颜色较浅为止,待冷凝液刚刚虹吸下去时,即可停止加热。稍冷却后,改成蒸馏装置,把提取液中大部分乙醇蒸出(回收),趁热把瓶中剩余液倒入蒸发皿中,留作升华法提取咖啡因。
2.升华法提取咖啡因:向提取液中加入4g生石灰粉,搅成浆状,在蒸汽浴上蒸干,除去水分,使成粉状,然后移至石棉网上用酒精灯小火加热,焙炒片刻,除去水分。在蒸发皿上盖一张刺有许多小孔且孔刺向上的滤纸,再罩一个合适漏斗,漏斗颈部塞一小团疏松棉花,用酒精灯隔着石棉网小心加热,适当控温,当发现有棕色烟雾时,即升华完毕,停止加热。冷却后,取下漏斗,轻轻揭开滤纸,刮下咖啡因,残渣经搅拌后,用较大火再加热片刻,使升华完全。合并几次升华的咖啡因。
【注意事项】
(1)脂肪提取器的虹吸管极易折锻,装置仪器和取拿时须特别小心。
(2)滤纸套大小既要紧贴器壁,又能方便取放,其高度不得超过虹吸管,滤纸包茶叶末时要严谨,防止漏出堵塞虹吸管,纸套上面折成凹形,以保证回流液均匀浸润被提取物。
(3)若提取液颜色很淡时,即可停止提取。
(4)瓶中乙醇不可蒸得太干,否则残液很粘,转移时损失较大。
【思考题】
(1)提取咖啡因时用到生石灰,它起什么作用?
(2)从茶叶中提取出的咖啡因有绿色光泽,为什么?
【实验要求】上交实验报告
