南京水平测试2013.2
一、单项选择题(本大题共23小题,每小题3分,共69分。在每小题的四个选项中,只有一个选项是符合要求的)
1.燃放烟花爆竹增强春节喜庆,但也造成大气严重污染。烟花中含有的KNO3属于( )
A.氧化物 B.酸 C.碱 D.盐
2.下列为人体提供能量的营养物质中,属于高分子化合物的是 ( )
A.蛋白质 B.油脂 C.葡萄糖 D.蔗糖
3.从海带中提取碘的实验要用到过滤、萃取实验操作,该两项操作不需要的仪器是( )
A.烧杯 B.烧瓶 C.玻璃棒 D.分液漏斗
4.下列气体能使品红溶液褪色的是 ( )
A.O2 B.CO2 C.SO2 D.CO
5.下列物质属于离子化合物且含有共价键的是 ( )
A.HCl B.CaCl2 C.H2O D.NaOH
6.某溶液中存在大量的H+、Cl-、SO42-,该溶液中还可能大量存在的是 ( )
A.OH- B.Ba2+ C.Fe3+ D.CO32-
7.20##年6月24日,“蛟龙号”下潜到深海7 020 m,创造了我国载人深潜新纪录。“蛟龙号”的耐压舱用钛合金制造。下列有关钛原子(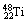 )的说法正确的是 ( )
)的说法正确的是 ( )
A.质子数为48 B.中子数为48
C.质量数为22 D.原子序数为22
8.以下物质间的转化不能通过一步反应实现的是 ( )
A.HClO→O2 B.SiO2→H2SiO3
C.CO2→CaCO3 D.Cu→CuSO4
9.下列关于Fe2O3和Al2O3性质和用途的说法符合事实的是 ( )
A.都可与盐酸反应 B.都可溶于水
C.都常用作耐火材料 D.都可与氢氧化钠溶液反应
10.下列化学用语正确的是 ( )
A.CH4的比例模型
B.HCl的电子式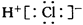
C.S的结构示意图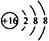
D.Fe2(SO4)3的电离方程式:Fe2(SO4)3==2Fe2++3SO42-
11.设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.28 g N2含有的原子数为NA
B.标准状况下22.4 L水中含有的H2O分子数为NA
C.1 mol Zn与足量盐酸反应失去的电子数为2NA
D.0.1 L 2 mol·L-1 NaCl溶液中含有Na+个数为2NA
12.下列实验装置、试剂选用或操作正确的是 ( )
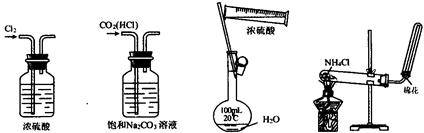
A.干燥Cl2 B.除去CO2中的HCl
C.稀释浓硫酸 D.制取少量氨气
13.甲烷、乙烯是重要的化工原料。下列叙述正确的是 ( )
A.甲烷、乙烯是同分异构体
B.可用酸性高锰酸钾溶液来区别甲烷和乙烯
C.甲烷与氯气在光照条件下发生置换反应
D.乙烯与水在一定条件下发生取代反应生成乙醇
14.下列关于氮的化合物的性质及用途叙述正确的是 ( )
A.可用铁制容器储存稀硝酸
B.实验室可用氨水与硫酸铝溶液反应制取氢氧化铝
C.实验室用排空气集气法收集NO气体
D.NO2与水发生化合反应生成硝酸
15.20##年6月18 ,“神舟九号”飞船上的宇航员成功进入“天宫一号”太空实验室,标志着我国航天事业新的飞跃。火箭和飞船飞行所需的巨大能量可由下列化学反应提供:C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O有关该反应的说法正确的是 ( )
A.由于化学键断裂,放出能量 B.氮元素的化合价不变
C.碳元素被氧化 D.还原剂是N2O4
16.下列有关离子(或物质)的检验及结论正确的是 ( )
A.用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中含有K+
B.向无色溶液中加入BaCl2溶液有白色沉淀出现,则溶液中含有SO42-
C.用一束光照射氯化铁溶液和氢氧化铁胶体,都出现丁达尔现象
D.向黄色溶液中加入淀粉,溶液变蓝色,则溶液中含有I2
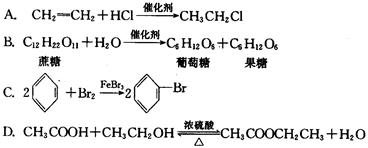
17.下列有机化学方程式书写错误的是 ( )
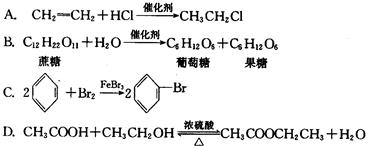
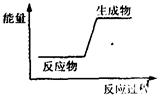 18.下列反应前后物质的总能量变化可用右图表示的是( )
18.下列反应前后物质的总能量变化可用右图表示的是( )
A.石灰石在高温下的分解反应
B.生石灰和水的反应
C.盐酸与氢氧化钠溶液的反应
D.木炭在氧气中燃烧
19.下列离子方程式正确的是 ( )
A.钠和水反应:Na+H2O==Na++OH-+H2↑
B.铜片和氯化铁溶液反应:Cu+Fe3+==Cu2++Fe2+
C.少量二氧化硫与烧碱溶液反应:SO2+2OH-==SO32-+H2O
D.氯气和冷的氢氧化钠溶液反应:2Cl2+2OH-==3Cl-+ClO-+H2O
20. 是工业上制造硫酸的重要反应。下列关于该反应的说法正确的是 ( )
是工业上制造硫酸的重要反应。下列关于该反应的说法正确的是 ( )
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3
21.下列关于化学能转化为电能的四种装置的说法正确的是 ( )

A.电池I中锌是正极
B.电池Ⅱ是一次电池
C.电池Ⅲ工作时,氢气发生还原反应
D.电池Ⅳ工作时,电子由锌通过导线流向碳棒
22.A、B、C、D、E为短周期主族元素,且原子序数依次增大。A原子的最外层电子数是其电子层数的3倍,B原子的半径在同周期主族元素的原子中最大,A、E同主族,D原子的最高正价与负价的绝对值相等。下列说法正确的是 ( )
A.原子半径:D>C
B.氢化物的稳定性:E>A
C.氢氧化物的碱性:C>B
D.最高价氧化物对应水化物的酸性:E>D
23.在硫酸铝、硫酸和硫酸镁的混合溶液200 mL中,c(A3+)=0.2 mol·L-1,当加入等体积1.6 mol·L-1 KOH溶液时,生成的沉淀最多,再加入过量的KOH溶液后,经过滤、洗涤、干燥,得白色沉淀2.32 g。则反应前的混合溶液中c(H2SO4)是 ( )
A.0.20 mol·L-1 B.0.30 mol·L-1
C.0.40 mol·L-1 D.0.60 mol·L-1
第Ⅱ卷(非选择题共31分)
二、非选择题:本部分共3小题,共31分。
24.本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基
础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》(15分)
(1)(3分)关注食品安全,关爱身体健康。
①下列维生素中,可用于防治坏血病的是 (填字母)。
a.维生素A b.维生素B c.维生素C
②在食品加工或餐饮业中,特别要严加控制用量的物质是 (填字母)。
a.氯化钠 b.碳酸氢钠 c.亚硝酸钠
③青霉素适合治疗的疾病是 (填字母)。
a.感冒发烧 b.细菌感染 c.胃酸过多
(2)(5分)合理使用材料,改善人类生活。
①钢铁是人类生产和生活中非常重要的材料,但每年因锈蚀而损失的数量十分惊人。金属腐蚀分为化学腐蚀和电化学腐蚀,两者的微观本质都是发生 的过程。为防止轮船船体在海水中被腐蚀,一般在船身连接 (填“锌块”或“铜块”)。
②在普通玻璃制造过程中,碳酸钙与二氧化硅在高温下发生反应的化学方程式是 。橡胶是制造轮胎的重要原料,天然橡胶通过硫化措施,使它的分子转化为 结构,从而增大橡胶的强度。
(3)(7分)中共十八大报告提出:“大力推进生态文明建设”。
①燃煤是增加大气PM2.5数值、形成雾霾天气的罪魁祸首之一。煤的气化是高效、清洁地利用煤炭的重要途径,写出灼热的焦炭与水蒸气反应的化学方程式: 。
②餐饮业产生的“地沟油”的主要成分是油脂。综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取高级脂肪酸和 (填名称)。将废弃塑料进行 处理,可以获得乙烯、丙烯等化工原料。
③防治重金属污染是20##年全国环保工作的重点。向含有Hg2+的废水中加入Na2S,可以使Hg2+转变成沉淀,离子反应方程式为 。
④我国生活垃圾一般可分为以下四大类:可回收垃圾、厨余垃圾、有害垃圾和其他垃圾。以下物质属于可回收垃圾的是 (填字母)。
a.废报纸 b.废铝制易拉罐 c.过期药品 d.渣土
B.《有机化学基础》(15分)
(1)(3分)根据官能团可以对有机物进行分类、鉴别和除杂。
①下列有机物属于烃的是 (填字母)。
a.乙炔 b.乙醇 c.乙酸
②区分甲苯和苯酚,不可用的试剂是 (填字母)。
a.FeCl3溶液 b.酸性KMnO4溶液 c.溴水
③除去乙酸乙酯中的乙酸,可用的试剂是 (填字母)。
a.NaOH溶液 b.NaCl溶液 c.饱和Na2CO3溶液
(2)(5分)异丙苯是一种重要的有机化工原料。异丙苯的结构简式为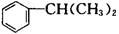 。
。
①异丙苯中至多有 个碳原子共平面。
②异丙苯有多种同分异构体,其中一溴代物种类最少的芳香烃的是 (填结构简式)。
③由异丙苯制备对溴异丙苯的化学方程式为 。
(3)(7分)化合物Ⅲ是一种重要的医药合成中间体,其合成路线如下:
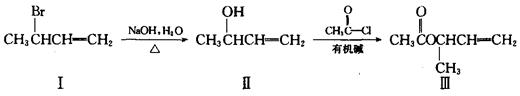
①该合成路线中第二步反应属于 (填反应类型)。
②在一定条件下,I、Ⅱ、Ⅲ3种化合物中的 (填序号)可发生消去反应生成不含甲基的产物。
③化合物Ⅲ的一种同分异构体X能发生银镜反应且能水解,X的核磁共振氢谱图显示分子中有3种不同化学环境的氢。X的结构简式为 。
④请写出区分化合物I和化合物Ⅱ的实验方法和现象 。
25.(6分)在下图所示的物质转化关系中,A是用于制造汽车发动机的耐高温陶瓷材料,A由两种元素组成,且两种元素化合价的绝对值相等。常温下,C、F、K是无色无味的气体单质,D、H是固体单质。E是常见的两性氧化物。B、G是汽车尾气中的主要污染气体,所含元素均为第二周期元素。反应②常用于汽车尾气的处理。
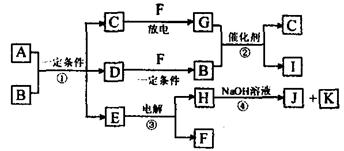
(1)C的电子式: 。
(2)A的化学式: 。
(3)反应③的化学方程式: 。
(4)反应④的离子方程式: 。
26.(10分)化合物A[KxFe(C2O4)y·zH2O,其中铁元素为+3价]是一种重要的光化学试剂。
(1)制备化合物A的实验流程如下:
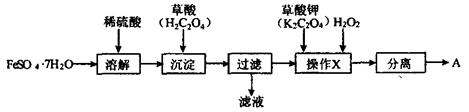
(2)上述流程中,检验“过滤”后的固体已洗涤干净的方法是 。
(3)上述流程“操作X”中加入H2O2的目的是 。
(4)测定化合物A的化学式实验步骤如下:
a.准确称取A样品4.91 g,干燥脱水至恒重,残留物质的质量为4.37 g;
b.将步骤a所得固体溶于水,加入还原铁粉0.28 g,恰好完全反应;
c.另取A样品4.91 g置于锥形瓶中,加入足量的3 mol·L-1的H2SO4溶液和适量蒸馏水,再加入0.50 mol·L-1的KMnO4溶液24.0 mL,微热,恰好完全反应:
2KMnO4+5H2C2O4+3H2SO4==2MnSO4+K2SO4+10CO2↑+8H2O
请通过计算填空:
①4.91g A样品中含结晶水的物质的量为 mol。
②A样品中 = 。
= 。
③A的化学式为 。

第二篇:20xx.2南京水平测试
南京水平测试2013.2
一、单项选择题(本大题共23小题,每小题3分,共69分。在每小题的四个选项中,只有一个选项是符合要求的)
1.燃放烟花爆竹增强春节喜庆,但也造成大气严重污染。烟花中含有的KNO3属于( )
A.氧化物 B.酸 C.碱 D.盐
2.下列为人体提供能量的营养物质中,属于高分子化合物的是 ( )
A.蛋白质 B.油脂 C.葡萄糖 D.蔗糖
3.从海带中提取碘的实验要用到过滤、萃取实验操作,该两项操作不需要的仪器是( )
A.烧杯 B.烧瓶 C.玻璃棒 D.分液漏斗
4.下列气体能使品红溶液褪色的是 ( )
A.O2 B.CO2 C.SO2 D.CO
5.下列物质属于离子化合物且含有共价键的是 ( )
A.HCl B.CaCl2 C.H2O D.NaOH
6.某溶液中存在大量的H+、Cl-、SO42-,该溶液中还可能大量存在的是 ( )
A.OH- B.Ba2+ C.Fe3+ D.CO32-
7.20##年6月24日,“蛟龙号”下潜到深海7 020 m,创造了我国载人深潜新纪录。“蛟龙号”的耐压舱用钛合金制造。下列有关钛原子(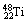 )的说法正确的是 ( )
)的说法正确的是 ( )
A.质子数为48 B.中子数为48
C.质量数为22 D.原子序数为22
8.以下物质间的转化不能通过一步反应实现的是 ( )
A.HClO→O2 B.SiO2→H2SiO3
C.CO2→CaCO3 D.Cu→CuSO4
9.下列关于Fe2O3和Al2O3性质和用途的说法符合事实的是 ( )
A.都可与盐酸反应 B.都可溶于水
C.都常用作耐火材料 D.都可与氢氧化钠溶液反应
10.下列化学用语正确的是 ( )
A.CH4的比例模型
B.HCl的电子式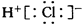
C.S的结构示意图
D.Fe2(SO4)3的电离方程式:Fe2(SO4)3==2Fe2++3SO42-
11.设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.28 g N2含有的原子数为NA
B.标准状况下22.4 L水中含有的H2O分子数为NA
C.1 mol Zn与足量盐酸反应失去的电子数为2NA
D.0.1 L 2 mol·L-1 NaCl溶液中含有Na+个数为2NA
12.下列实验装置、试剂选用或操作正确的是 ( )
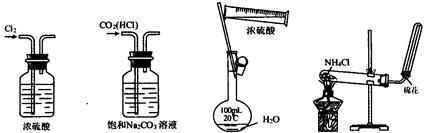
A.干燥Cl2 B.除去CO2中的HCl
C.稀释浓硫酸 D.制取少量氨气
13.甲烷、乙烯是重要的化工原料。下列叙述正确的是 ( )
A.甲烷、乙烯是同分异构体
B.可用酸性高锰酸钾溶液来区别甲烷和乙烯
C.甲烷与氯气在光照条件下发生置换反应
D.乙烯与水在一定条件下发生取代反应生成乙醇
14.下列关于氮的化合物的性质及用途叙述正确的是 ( )
A.可用铁制容器储存稀硝酸
B.实验室可用氨水与硫酸铝溶液反应制取氢氧化铝
C.实验室用排空气集气法收集NO气体
D.NO2与水发生化合反应生成硝酸
15.20##年6月18 ,“神舟九号”飞船上的宇航员成功进入“天宫一号”太空实验室,标志着我国航天事业新的飞跃。火箭和飞船飞行所需的巨大能量可由下列化学反应提供:C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O有关该反应的说法正确的是 ( )
A.由于化学键断裂,放出能量 B.氮元素的化合价不变
C.碳元素被氧化 D.还原剂是N2O4
16.下列有关离子(或物质)的检验及结论正确的是 ( )
A.用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中含有K+
B.向无色溶液中加入BaCl2溶液有白色沉淀出现,则溶液中含有SO42-
C.用一束光照射氯化铁溶液和氢氧化铁胶体,都出现丁达尔现象
D.向黄色溶液中加入淀粉,溶液变蓝色,则溶液中含有I2
17.下列有机化学方程式书写错误的是 ( )
 18.下列反应前后物质的总能量变化可用右图表示的是( )
18.下列反应前后物质的总能量变化可用右图表示的是( )
A.石灰石在高温下的分解反应
B.生石灰和水的反应
C.盐酸与氢氧化钠溶液的反应
D.木炭在氧气中燃烧
19.下列离子方程式正确的是 ( )
A.钠和水反应:Na+H2O==Na++OH-+H2↑
B.铜片和氯化铁溶液反应:Cu+Fe3+==Cu2++Fe2+
C.少量二氧化硫与烧碱溶液反应:SO2+2OH-==SO32-+H2O
D.氯气和冷的氢氧化钠溶液反应:2Cl2+2OH-==3Cl-+ClO-+H2O
20. 是工业上制造硫酸的重要反应。下列关于该反应的说法正确的是 ( )
是工业上制造硫酸的重要反应。下列关于该反应的说法正确的是 ( )
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3
21.下列关于化学能转化为电能的四种装置的说法正确的是 ( )
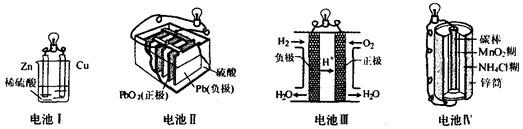
A.电池I中锌是正极
B.电池Ⅱ是一次电池
C.电池Ⅲ工作时,氢气发生还原反应
D.电池Ⅳ工作时,电子由锌通过导线流向碳棒
22.A、B、C、D、E为短周期主族元素,且原子序数依次增大。A原子的最外层电子数是其电子层数的3倍,B原子的半径在同周期主族元素的原子中最大,A、E同主族,D原子的最高正价与负价的绝对值相等。下列说法正确的是 ( )
A.原子半径:D>C
B.氢化物的稳定性:E>A
C.氢氧化物的碱性:C>B
D.最高价氧化物对应水化物的酸性:E>D
23.在硫酸铝、硫酸和硫酸镁的混合溶液200 mL中,c(A3+)=0.2 mol·L-1,当加入等体积1.6 mol·L-1 KOH溶液时,生成的沉淀最多,再加入过量的KOH溶液后,经过滤、洗涤、干燥,得白色沉淀2.32 g。则反应前的混合溶液中c(H2SO4)是 ( )
A.0.20 mol·L-1 B.0.30 mol·L-1
C.0.40 mol·L-1 D.0.60 mol·L-1
第Ⅱ卷(非选择题共31分)
二、非选择题:本部分共3小题,共31分。
24.本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基
础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》(15分)
(1)(3分)关注食品安全,关爱身体健康。
①下列维生素中,可用于防治坏血病的是 (填字母)。
a.维生素A b.维生素B c.维生素C
②在食品加工或餐饮业中,特别要严加控制用量的物质是 (填字母)。
a.氯化钠 b.碳酸氢钠 c.亚硝酸钠
③青霉素适合治疗的疾病是 (填字母)。
a.感冒发烧 b.细菌感染 c.胃酸过多
(2)(5分)合理使用材料,改善人类生活。
①钢铁是人类生产和生活中非常重要的材料,但每年因锈蚀而损失的数量十分惊人。金属腐蚀分为化学腐蚀和电化学腐蚀,两者的微观本质都是发生 的过程。为防止轮船船体在海水中被腐蚀,一般在船身连接 (填“锌块”或“铜块”)。
②在普通玻璃制造过程中,碳酸钙与二氧化硅在高温下发生反应的化学方程式是 。橡胶是制造轮胎的重要原料,天然橡胶通过硫化措施,使它的分子转化为 结构,从而增大橡胶的强度。
(3)(7分)中共十八大报告提出:“大力推进生态文明建设”。
①燃煤是增加大气PM2.5数值、形成雾霾天气的罪魁祸首之一。煤的气化是高效、清洁地利用煤炭的重要途径,写出灼热的焦炭与水蒸气反应的化学方程式: 。
②餐饮业产生的“地沟油”的主要成分是油脂。综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取高级脂肪酸和 (填名称)。将废弃塑料进行 处理,可以获得乙烯、丙烯等化工原料。
③防治重金属污染是20##年全国环保工作的重点。向含有Hg2+的废水中加入Na2S,可以使Hg2+转变成沉淀,离子反应方程式为 。
④我国生活垃圾一般可分为以下四大类:可回收垃圾、厨余垃圾、有害垃圾和其他垃圾。以下物质属于可回收垃圾的是 (填字母)。
a.废报纸 b.废铝制易拉罐 c.过期药品 d.渣土
B.《有机化学基础》(15分)
(1)(3分)根据官能团可以对有机物进行分类、鉴别和除杂。
①下列有机物属于烃的是 (填字母)。
a.乙炔 b.乙醇 c.乙酸
②区分甲苯和苯酚,不可用的试剂是 (填字母)。
a.FeCl3溶液 b.酸性KMnO4溶液 c.溴水
③除去乙酸乙酯中的乙酸,可用的试剂是 (填字母)。
a.NaOH溶液 b.NaCl溶液 c.饱和Na2CO3溶液
(2)(5分)异丙苯是一种重要的有机化工原料。异丙苯的结构简式为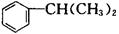 。
。
①异丙苯中至多有 个碳原子共平面。
②异丙苯有多种同分异构体,其中一溴代物种类最少的芳香烃的是 (填结构简式)。
③由异丙苯制备对溴异丙苯的化学方程式为 。
(3)(7分)化合物Ⅲ是一种重要的医药合成中间体,其合成路线如下:
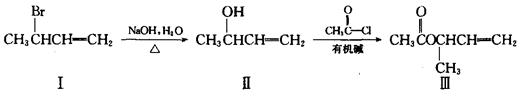
①该合成路线中第二步反应属于 (填反应类型)。
②在一定条件下,I、Ⅱ、Ⅲ3种化合物中的 (填序号)可发生消去反应生成不含甲基的产物。
③化合物Ⅲ的一种同分异构体X能发生银镜反应且能水解,X的核磁共振氢谱图显示分子中有3种不同化学环境的氢。X的结构简式为 。
④请写出区分化合物I和化合物Ⅱ的实验方法和现象 。
25.(6分)在下图所示的物质转化关系中,A是用于制造汽车发动机的耐高温陶瓷材料,A由两种元素组成,且两种元素化合价的绝对值相等。常温下,C、F、K是无色无味的气体单质,D、H是固体单质。E是常见的两性氧化物。B、G是汽车尾气中的主要污染气体,所含元素均为第二周期元素。反应②常用于汽车尾气的处理。

(1)C的电子式: 。
(2)A的化学式: 。
(3)反应③的化学方程式: 。
(4)反应④的离子方程式: 。
26.(10分)化合物A[KxFe(C2O4)y·zH2O,其中铁元素为+3价]是一种重要的光化学试剂。
(1)制备化合物A的实验流程如下:
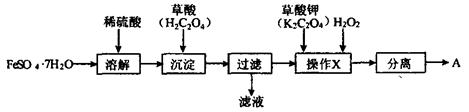
(2)上述流程中,检验“过滤”后的固体已洗涤干净的方法是 。
(3)上述流程“操作X”中加入H2O2的目的是 。
(4)测定化合物A的化学式实验步骤如下:
a.准确称取A样品4.91 g,干燥脱水至恒重,残留物质的质量为4.37 g;
b.将步骤a所得固体溶于水,加入还原铁粉0.28 g,恰好完全反应;
c.另取A样品4.91 g置于锥形瓶中,加入足量的3 mol·L-1的H2SO4溶液和适量蒸馏水,再加入0.50 mol·L-1的KMnO4溶液24.0 mL,微热,恰好完全反应:
2KMnO4+5H2C2O4+3H2SO4==2MnSO4+K2SO4+10CO2↑+8H2O
请通过计算填空:
①4.91g A样品中含结晶水的物质的量为 mol。
②A样品中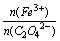 = 。
= 。
③A的化学式为 。

