
材料科学与工程学院
材料科学与工程专业实验报告
(建筑材料工程方向)
课程名称:无机材料科学基础
班 级:
姓 名:
学 号:
成 绩:
实验一、试样制备、显微镜的构造与操作
一、 实验内容
二、 实验目的
三、 实验原理
四、 实验仪器与设备
五、 实验步骤
六、 实验数据与结果分析
七、 思考题
根据自己的实践体会,在制备金相试样时应注意哪些事项?
实验二、淬冷法研究相平衡
一、实验内容
二、实验目的
三、实验原理
四、实验仪器与设备
五、实验步骤
六、实验数据与结果分析
七、思考题
淬冷法研究相平衡的优缺点是什么?
实验三、陶瓷材料的成型、烧结及性能
一、实验内容
二、实验目的
三、实验原理
四、实验仪器与设备
五、实验步骤
六、实验数据与结果分析
七、思考题
1、陶瓷材料在烧结过程中发生那些变化?
2、影响烧结的因素有哪些?
第二篇:无机材料科学基础第四章
第四章 表面与界面
第一节 晶界类型
一、根据相邻晶粒的位向差分:根据相邻晶粒的位向差分:
位向差大——大角度晶界
位向差小——小角度晶界
1.小角度晶界:小角度晶界:亚晶界
单晶体中“单晶体中“镶嵌结构”镶嵌结构”产生小角度晶界。产生小角度晶界。小角度晶界位向差小,小角度晶界位向差小,晶界很薄。小角度晶界形成原因是单晶体在成长过程中受热或机械应力界很薄。
或表面张力作用产生的。或表面张力作用产生的。
同号位错在同一滑移面上相互排斥
异号位错在同一滑移面上相互吸引。异号位错在同一滑移面上相互吸引。
o同号位错不在同一滑移面上相互吸引。( >45同号位错不在同一滑移面上相互吸引。 >45) 倾向于刃型位错自上而下排列,倾向于刃型位错自上而下排列,形成小角度晶界。形成小角度晶界。
2.大角度晶界:大角度晶界:多晶材料之间的晶界,多晶材料之间的晶界,其结构为无定型结构,其结构为无定型结构,厚度较大。
二、根据晶面两侧晶格的吻合程度分1.共格界面:界面两侧具有相近的原子排列和原子间距,越过晶面原共格界面:界面两侧具有相近的原子排列和原子间距,子排列是连续的,子排列是连续的,即界面上的原子同时处于相邻的晶列的晶格结点上。
共格界面,其上结点属于界面两侧两个晶粒,但两侧的晶粒晶格常数共格界面,其上结点属于界面两侧两个晶粒,
略有差别,略有差别,通过弹性变形来协调。通过弹性变形来协调。
孪晶(孪晶(双晶)双晶)间界面为共格晶界,间界面为共格晶界,可通过堆垛层错产生。可通过堆垛层错产生。 A
B
B
A
2.半共格晶界 晶格间距失配度太大,晶格间距失配度太大,弹性变形不能协调,插入刃型位错,插入刃型位错,在界面上插入附加的半平面(插入附加的半平面(引入刃型位错)引入刃型位错)形成半共格界面。形成半共格界面。
3.非共格晶界面:非共格晶界面:
晶界两侧结构相差太大, 晶界两侧结构相差太大,此时晶界结构为无定形的,此时晶界结构为无定形的,为非共格晶面。为非共格晶面。二、晶界能
晶界比晶体内部具有过剩的能量。晶界比晶体内部具有过剩的能量。
晶界能:晶界能:大角度晶界 > 小角度晶界
非共格晶界 > 半共格晶界 > 共格晶界
三、晶界应力
晶体各向异性,晶界两侧位向不同,两侧晶体沿晶界同一方向上晶体各向异性,晶界两侧位向不同,
弹性模量、弹性模量、热膨胀系数不同,热膨胀系数不同,会产生晶界应力,会产生晶界应力,若应力过大,若应力过大,晶界开裂,有裂纹出现。有裂纹出现。
第二节 晶体的表面结构
表面是指晶体与真空(表面是指晶体与真空(或与本身蒸汽)或与本身蒸汽)之间的界面。之间的界面。
一、表面对键强分布的影响:表面对键强分布的影响:
表面的存在会影响晶体内部键强的分布。表面的键强两极分化最强表面的存在会影响晶体内部键强的分布。表面的键强两极分化,分化,键、最弱键都分布在表面,最弱键都分布在表面,随离开表面距离的增大,随离开表面距离的增大,键增强、键增强、减弱的程度减小,程度减小,表面的影响程度越来越弱,表面的影响程度越来越弱,到离开表面足够远的地方,到离开表面足够远的地方,键强已经不受表面影响了。强已经不受表面影响了。
二、离子晶体的表面双电层
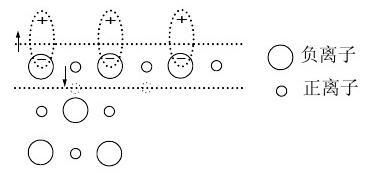
产生表面双电层的原因是极化,半径小、电价高的正离子对半径大的产生表面双电层的原因是极化,半径小、
负离子极化作用大,易形成表面双电层,双电层的厚度也与极化大小负离子极化作用大,易形成表面双电层,
有关。有关。由于表面被负离子所屏蔽,由于表面被负离子所屏蔽,因而表面呈负电性。因而表面呈负电性。
形成表面双电层后表面能降低,而且表面双电层厚度越大,表面形成表面双电层后表面能降低,而且表面双电层厚度越大,能降低越多。能降低越多。因为表面双电层产生后,因为表面双电层产生后,正离子受力比较均衡,正离子受力比较均衡,而且最表面负离子之间产生共价键结合,表面负离子之间产生共价键结合,释放能量,释放能量,使表面能量降低。使表面能量降低。
第三节 晶体的表面能
一、 表面能定义
每增加单位表面体系自由焓的增量——(比)表面自由焓(比表面能、比表面能、表面能),是指每单位面积表面比内部过剩的自由焓表面能),是指每单位面积表面比内部过剩的自由焓。是指每单位面积表面比内部过剩的自由焓。
二、晶体表面能的理论计算
设Ub:质点在晶体内时与最近邻质点的相互作用能
Us:质点在表面时与最近邻质点的相互作用能 Us≈ Ub
nb:质点在晶体时周围最近邻的质点数
ns:质点在表面时周围最近邻的质点数 nb > ns
把一个质点从内部移出需要断键数量比从表面移出把一个质点从内部移出需要断键数量比从表面移出需要断键数比从表面移出需要断键数量多,量多,因而需要能量大因而需要能量大,要能量大,高出的能量为Δ高出的能量为ΔU。表面质点本身可动性大,表面质点本身可动性大,说明表面质点本身能量高,说明表面质点本身能量高,ΔU就是表面质点比内部质点过剩的能量。
ΔU = UU = Ub nb/2-/2- Us ns/2 /2
= Ub nb/2(1- ns/ nb)
= U晶/N0(1- ns/ nb)
设表面密度:设表面密度:Ls(单位面积表面拥有的质点数)单位面积表面拥有的质点数)
Ls·ΔU = Ls·U晶/ N0(1- ns/ nb)
Ls·ΔU代表单位面积表面比内部过剩的能量代表单位面积表面比内部过剩的能量,过剩的能量,即表面内能。即表面内能。 自由焓:自由焓:G = U-G = U-TS,
0K时,G = U = LsG = U = Ls·U晶/ N0(1- ns/ nb)
由此式可知:由此式可知:
(1)当T升高时,升高时,表面自由焓小于表面内能。表面自由焓小于表面内能。
(2)表面自由焓和晶格能成近似正比关系。表面自由焓和晶格能成近似正比关系。
(3)表面能是各向异性的
(4)表面能随温度T升高而降低
①T↑,质点间键力↓质点间键力↓,将质点转到表面的能量↓将质点转到表面的能量↓,表面能↓表面能↓。 ② T↑,熵所引起的作用↑熵所引起的作用↑,所以表面能↓所以表面能↓。
三、表面能与表面张力的关系
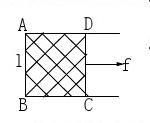
力图使表面缩小。由,力图使表面缩小。,所以表面张力的数值等于表面所以表面张力的数值不等于表面,所以表面张力的数值不等于表面能。
四、固体的表面活性
表面质点能量高,表面质点能量高,活性大,活性大,因此,因此,物料的比表面积越大,物料的比表面积越大,活性就越大,就越大,也就是需要的活化能越小。也就是需要的活化能越小。物料粉磨时,物料粉磨时,由于高分散度的物料体系自由焓高,料体系自由焓高,不稳定,不稳定,倾向于自发聚结,倾向于自发聚结,所以粉磨到到一定程度后比表面积很难再增加,后比表面积很难再增加,但即使如此,但即使如此,物料活性仍在增加,物料活性仍在增加,因为物料的晶格缺陷随粉磨的进行在增加。的晶格缺陷随粉磨的进行在增加。
五、界面能:界面能:
当两相化学性质相似时,当两相化学性质相似时,界面能小。界面能小。
如果两相化学性质相差较大但有强烈吸引力, 如果两相化学性质相差较大但有强烈吸引力,也会使界面能小。也会使界面能小。
第四节 表面力
一、 表面力
处于内部的质点,处于内部的质点,受力是均衡的,受力是均衡的,而处在表面的质点,而处在表面的质点,由于力场由于力场不平衡,不平衡,因此有剩余键力,因此有剩余键力,使表面有吸附作用。使表面有吸附作用。这种固体表面和被吸附质点之间的作用力称为表面力。附质点之间的作用力称为表面力。
二、表面力的种类:表面力的种类:
1、物理力,物理力,即范德华力。即范德华力。
2、化学力:化学力:固体表面和被吸附质点之间发生了电子转移。固体表面和被吸附质点之间发生了电子转移。
第五节 表面行为
一、 表面吸附
表面吸附是一个自发过程,表面吸附是一个自发过程,放热过程。放热过程。
可以利用吸附来进行表面改性,可以利用吸附来进行表面改性,所谓表面改性,所谓表面改性,是指通过各种表面处理改变固体表面结构和性质,面处理改变固体表面结构和性质,以适应各种预期要求。以适应各种预期要求。
表面活性剂是指加入少量就能显著降低表面能的物质。表面活性表面活性剂是指加入少量就能显著降低表面能的物质。
剂一般有具有“剂一般有具有“两亲结构”两亲结构”,一端亲水、一端亲水、一端亲油,一端亲油,所以可以改性。所以可以改性。 二、润湿
1.润湿的度量
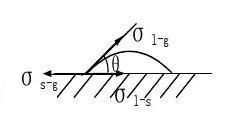
0 θ>90σsg=σlgcosθ+σsl
cosθ=(σsg-σls)/σlg
2.润湿过程
(1)润湿类型
①附着润湿(附着润湿(粘附润湿)粘附润湿) 不润湿
由原来的液体表面和固体表面变成固液界面。由原来的液体表面和固体表面变成固液界面。
G始-G终 =σlg+σsg-σl s= W粘附
W粘附 —把固液界面拆开需要环境做的最小功,把固液界面拆开需要环境做的最小功,反映两相之间结合程度。W↑,结合牢固。结合牢固。
②浸渍润湿(浸渍润湿(浸润)浸润)
固液界面代替原来固体表面。固液界面代替原来固体表面。
G始-G终 =σsg-σls = W浸渍
W浸渍—反映了在固体表面上液体取代气体能力的大小。反映了在固体表面上液体取代气体能力的大小。
W浸渍 = 浸润张力F =σsg-σls =σlg cosθ
③铺展润湿(铺展润湿(铺展)铺展)
在液体在固体表面铺展的同时,液气界面也在。即扩展固液界面和液在液体在固体表面铺展的同时,液气界面也在。
气表面代替固气界面。气表面代替固气界面。
G始- G终=σsg-σls-σlg= S(铺展系数)铺展系数)
当S≥0时,液体就可以在固体表面铺展。液体就可以在固体表面铺展。
S =σsg-σls-σlg = F-= F-σlg 当润湿张力大于σ当润湿张力大于σlg时可以铺展。时可以铺展。
(2)不同润湿过程发生的条件:不同润湿过程发生的条件:
①能量判据:能量判据:
附着润湿:附着润湿:W粘= F+σlg lg
浸渍润湿:浸渍润湿:W浸= F = F
铺展润湿:铺展润湿:S = F-S = F-σlg
②接触角判据:接触角判据:
W粘=σlg(1+cosθ)≥0 θ≤180O
W浸=σlgcosθ ≥0 θ≤90O
S =σlg(cosθ-1)≥0 θ≤0
3.表面粗糙度对润湿的影响
根据热力学原理,根据热力学原理,物系平衡条件:物系平衡条件:dG/dS=0 dG/dS=0
σls · dS- dS-σsg·dS +σlg·dS cosθ= 0 = 0
∴σls-σsg+σlg cosθ=0 =0
cosθ =(σls-σsg)/σlg
实际表面从微观上看是凹凸不平的实际表面从微观上看是凹凸不平的。从微观上看是凹凸不平的。
θn—表观接触角。表观接触角。
给定粗糙系数n = 真实表面积/表观表面积。表观表面积。n总是大于1。 当表观表面积增加dS,则:
nσls · dS - dS - nσsg·dS +σlg·dS cosθn = 0 n = 0
∴nσls-nσsg+σlg cosθn = 0 n = 0
cosθn = n(σls-σsg)/σlg
当σls<σsg, cosθn > 0, n↑, cosθn↑, θn↓
因此,因此,如果本来就润湿,如果本来就润湿,表面越粗糙,表面越粗糙,则越有利于润湿。则越有利于润湿。 当σls>σsg, cosθn<0,n↓,cosθn↓, θn↑
本来不润湿本来不润湿,表面越粗糙,表面越粗糙,就越不容易润湿。就越不容易润湿。
4. 润湿对材料微观结构的影响
(1)固-液系统
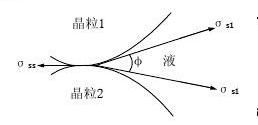
固界面能和固-液界面能的比值。液界面能的比值。 sl
当σss/σsl = 1, cos(φ/2)=1/2, φ=1200
当σss/σsl>1, cos(φ/2)<1/2, φ>1200
当σss/σsl = 2, cos(φ/2)=1, φ=0 =0
3
当σss/σsl=,cos(φ/2)=2, φ=600
3
当σss/σsl>,cos(φ/2)>2, φ<600
微观结构分为:
①固-固直接结合结构:固直接结合结构:φ大,σss/σsl小。 如需要耐高温的耐火材料,如需要耐高温的耐火材料,则固固直接结 合的结构好。合的结构好。
②固-液-固结合结构:固结合结构:φ小,σss/σsl大。
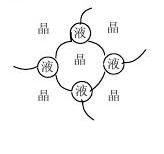
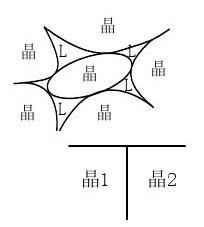
(2)固-气系统
气孔分布状况由固-固界面能和固体表面能比值决定。固界面能和固体表面能比值决定。
此现象称为热腐蚀现象。 此现象称为热腐蚀现象。其中φ其中φ称为沟槽角,称为沟槽角,又叫槽角或热腐蚀角。又叫槽角或热腐蚀角。
第六节 弯曲表面效应
一、 毛细现象
在毛细管中,在毛细管中,由于液体的弯曲表面产生的力,由于液体的弯曲表面产生的力,称为毛细管力。称为毛细管力。弯曲表面上的饱和蒸汽压与曲率半径的关系如下式所示面上的饱和蒸汽压与曲率半径的关系如下式所示:
ln
P22σM11
=(?)P1ρRTr2r1
开尔文公式:开尔文公式:
其中:其中:M—分子量 ρ—密度 σ—表面张力 P—表面上的饱和蒸汽压
r1、r2—曲率半径
平表面)时,lP平当r1= r2= ∞(平表面)nP弯=2σMρRTr弯
弯曲表面为凸面:弯曲表面为凸面:r弯>0,P>0,P凸>P平,r↑, (P凸-P平) ↑
弯曲表面为凹面:弯曲表面为凹面:r弯<0,P<0,P凹<P平,r↓, (P凹-P平) ↓
∴P凸> P平> P凹
由于弯曲表面上的饱和蒸汽压受曲率半径的影响,由于弯曲表面上的饱和蒸汽压受曲率半径的影响,微小晶体的溶解度增大, 熔点降低。熔点降低。
第七节 粘土-水系统
粘土-水系统中,水系统中,粘土粒子为分散相,粘土粒子为分散相,粒度一般均在0.1?10 um范围(,分散于水当中实际上是悬浮体与胶体的混合物范围(有时更粗有时更粗),分散于水当中实际上是悬浮体与胶体的混合物,分散于水当中实际上是悬浮体与胶体的混合物,但它具有许多胶体的性质。但它具有许多胶体的性质。
Ⅰ粘土-水系统中粘土颗粒表面带电的原因
粘土—水系统中,水系统中,粘土颗粒表面带电。粘土颗粒表面带电。
把平行于复网层的表面称为板面,而垂直于复网层的表面称为边面。 把平行于复网层的表面称为板面,而垂直于复网层的表面称为边面。一、板状表面带电的原因----板面总是带负电的。板面总是带负电的。
粘土矿物晶体结构中的晶格置换造成了板面带负电。原来复网层粘土矿物晶体结构中的晶格置换造成了板面带负电。
中晶格置换造成的负电由复网层间进入的正离子来平衡,当黏土分散中晶格置换造成的负电由复网层间进入的正离子来平衡,
于水中后,于水中后,原来平衡电荷的正离子进入水中,原来平衡电荷的正离子进入水中,使板面带负电。使板面带负电。
高岭石其结构为单网层,理论上没有晶格置换,所以理论上板面高岭石其结构为单网层,理论上没有晶格置换,
不带电,但实际上由于微量的晶格置换使得板面也带负电,但带电量带电,但实际上由于微量的晶格置换使得板面也带负电,
少;伊利石的晶格置换比蒙脱石严重,单位面积板面的负电量应该比伊利石的晶格置换比蒙脱石严重,
蒙脱石多,但伊利石结构中复网层之间是钾离子,而且钾离子可以牢蒙脱石多,但伊利石结构中复网层之间是钾离子,
固地把两个复网层连接在一起,固地把两个复网层连接在一起,不易解理,不易解理,分散度小,分散度小,成为板面的层面少,面少,比表面积小,比表面积小,所以相同质量的伊利石带负电量比蒙脱石少;所以相同质量的伊利石带负电量比蒙脱石少;三种矿物带负电量多少顺序为蒙脱石>伊利石>高岭石。高岭石。
二、边表面的带电机理
以高岭石为例分析边表面的带电机理。以高岭石为例分析边表面的带电机理。
边表面是指垂直于复网层的表面,当产生边表面时必然会出现很多断边表面是指垂直于复网层的表面,
(3-n)+(4-n)+(2-n)-n)-、Si(4-、O(2-(其中n指未断裂的键的键,也就会出现以下Al(3-
价数,,这些离子对周围的水施加了一个电场价数,如果全部断裂则n=0),这些离子对周围的水施加了一个电场
+-+的作用,的作用,电场作用于水,电场作用于水,则水会电离形成H和OH,这些离子与H或
OH-结合形成过渡表面化合物。过渡表面化合物在适当的PH值条件下,结合形成过渡表面化合物。值条件下,会发生解离,。 会发生解离,解离后使黏土边面带电,解离后使黏土边面带电,该机理称为“该机理称为“破键机理”破键机理”
+(4-n)+(3-n)+(2-n)-n)- 过渡表面化合物有Si(4----- OH-;Al(3----- OH-;O(2-----H---- ---- ----H。
-当溶液的pH > 7时,过渡表面化合物H+脱落,脱落,和溶液中的OH反应生
++成水,成水,H脱落后使得粘土边表面带负电脱落后使得粘土边表面带负电;土边表面带负电;当溶液的pH > 7时, H脱落,和溶液中的OH-反应生成水,反应生成水,H+脱落后使得粘土边表面带负电。脱落后使得粘土边表面带负电。
-(3-n)+过渡表面化合物Al(3----- OH---- OH的解离有两种情况:的解离有两种情况:
+pH <7时,OH-脱落,脱落,使得粘土边表面带正电,使得粘土边表面带正电,pH >7时,H脱落后使
得粘土边表面带负电。由此可见,边表面可以带正电,也可以带负电。得粘土边表面带负电。由此可见,边表面可以带正电,也可以带负电。粘土的边表面所带电性取决于溶液的pH 值,即pH >7带负电,<7带负电,pH 带正电。带正电。
粘土表面所带的正电荷和负电荷的代数和就是粘土的净电荷。由粘土表面所带的正电荷和负电荷的代数和就是粘土的净电荷。于粘土所带的负电荷一般都远大于正电荷,于粘土所带的负电荷一般都远大于正电荷,所以粘土的净电荷是负所以粘土的净电荷是负的,因此通常认为粘土是带负电的粒子。因此通常认为粘土是带负电的粒子。
Ⅱ粘土的离子吸附和离子交换
粘土表面既然带电,它就会吸附溶液中带有相反电荷的离子,而粘土表面既然带电,它就会吸附溶液中带有相反电荷的离子,这些被吸附的带有相反电荷的离子又可以被溶液中的其它离子所交换。
吸附氢离子的黏土称为H-粘土,吸附钠离子的黏土称为Na-吸粘土,Na-粘土,粘土,附钙离子的黏土称为Ca-Ca-粘土。粘土。
Na Na + 粘土+Ca2+→Ca-Ca-粘土+2Na
Na Na Na
一.阳离子交换----边面和板面上都可以发生
粘土表面带负电,吸附的反离子为阳离子,而吸附的阳离子又可粘土表面带负电,吸附的反离子为阳离子,
以与溶液中其它的正离子发生交换以与溶液中其它的正离子发生交换,中其它的正离子发生交换,称为阳离子交换。称为阳离子交换。
1.阳离子交换容量
阳离子交换容量用100克干粘土所吸附离子的毫克当量数来表示。
吸附阳离子交换容量的大小取决于表面带电量的多少。表面带电量越吸附阳离子交换容量的大小取决于表面带电量的多少。
高,吸附的离子越多,吸附的离子越多,阳离子交换容量就越高。阳离子交换容量就越高。
主要粘土矿物的阳离子交换容量如下:主要粘土矿物的阳离子交换容量如下:
蒙脱石 80—150 毫克当量/100G干粘土
伊利石 10—40 毫克当量/100G干粘土
高岭石 3—15 毫克当量/100G干粘土
由此可知,由此可知,根据阳离子交换容量可以区别黏土的矿物类型。根据阳离子交换容量可以区别黏土的矿物类型。 带电量的多少主要是看板面带电量的多少带电量的多少主要是看板面带电量的多少,量的多少主要是看板面带电量的多少,而三种矿物板面的带电量为: 量为:蒙脱石>伊利石>高岭石,高岭石,所以,所以,它们的阳离子交换容量如上。它们的阳离子交换容量如上。
2.影响阳离子交换容量的因素(影响阳离子交换容量的因素(除了矿物组成外)除了矿物组成外)
(1)分散度
分散度越高,系统中固体的比表面积越大,阳离子交换容量越大。 分散度越高,系统中固体的比表面积越大,阳离子交换容量越大。
(2)溶液的pH值
溶液的pH值大于7时边表面带负电,pH值大小会影响边表面的时边表面带负电,
所带负电量, 所带负电量, pH值越大,值越大,所带负电量越多,所带负电量越多,阳离子交换容量越大。阳离子交换容量越大。
(3)粘土矿物的结晶程度
结晶程度越差,结晶程度越差,阳离子交换容量越大。阳离子交换容量越大。
结晶程度越差,结晶程度越差,粘土矿物中晶格置换越多,粘土矿物中晶格置换越多,带负电量越多,带负电量越多,吸附的阳离子越多,的阳离子越多,因此阳离子交换容量也越大。因此阳离子交换容量也越大。
2. 阳离子交换顺序
阳离子交换顺序由粘土表面和阳离子间吸引力的大小来决定。阳离子交换顺序由粘土表面和阳离子间吸引力的大小来决定。在浓度相同的条件下,与粘土表面吸引力大的阳离子会交换与粘土表面浓度相同的条件下,
吸引力小的阳离子。吸引力小的阳离子。
一般情况下对同价离子,一般情况下对同价离子,离子半径越小,离子半径越小,离子的水化能力越强,离子的水化能力越强,水化离子半径也越大,水化离子半径也越大,粘土表面对它的吸引力就越小。粘土表面对它的吸引力就越小。因此,因此,粘土表面对对一价离子吸引力的大小顺序为:Li+ < Na+ < K+;对二价离子吸
2+ 引力的大小顺序为:Mg2+ < Ca2+ < Sr2+ < Ba2+
对不同价离子,电价越高,水化能力越强,水化离子半径虽越大,对不同价离子,电价越高,水化能力越强,水化离子半径虽越大,但是电价高对吸引力的影响更大,所以价数越高最终造成粘土表面对但是电价高对吸引力的影响更大,
M2+ < 其吸引力越大。因此粘土表面对各离子的吸引力大小顺序为:M+ < 其吸引力越大。
M3+。
可将粘土的阳离子交换顺序排列如下,: 可将粘土的阳离子交换顺序排列如下,称为“称为“霍夫曼斯特顺序”霍夫曼斯特顺序” H+ > Al3+ > Ba2+ > Sr2+ > Ca2+ > Mg2+ > NH4+ > K+ > Na+ > Li+
氢离子由于没有核外电子,也就没有电子云的斥力,而且离子半径小,氢离子由于没有核外电子,也就没有电子云的斥力,而且离子半径小,体积小,体积小,电荷密度大,电荷密度大,所以占据交换吸附的首位。所以占据交换吸附的首位。
利用霍夫曼斯特顺序可以比较相同浓度下离子的交换能力,相同浓度利用霍夫曼斯特顺序可以比较相同浓度下离子的交换能力,
下排在前面的离子能够交换出排在后面的离子,但必须注意其前提条下排在前面的离子能够交换出排在后面的离子,
件是在相同的浓度下来比较。如果把钠离子的浓度提高到一定程度就件是在相同的浓度下来比较。
可以交换排在它前边的钙离子。可以交换排在它前边的钙离子。
二、阴离子交换-----只能发生在边面上
因为pH〈 7时,边表面带正电,边表面带正电,吸附负离子,吸附负离子,会与溶液中的阴离子发生阴离子交换。离子发生阴离子交换。
Ⅲ 粘土的胶团结构
胶核一般具有晶体结构,其表面有电位离子,吸附溶液中的带有胶核一般具有晶体结构,其表面有电位离子,
相反电荷的反离子,相反电荷的反离子,构成胶团。构成胶团。粘土的胶团结构可表示为:粘土的胶团结构可表示为:
{[胶核]电位离子:电位离子:吸附层反离子}扩散层反离子
胶体粒子(胶体粒子(带电)带电)
胶团(胶团(电中性)电中性)
胶团在电场中的行为类似于电解质。在外电场的作用下,粘土颗胶团在电场中的行为类似于电解质。在外电场的作用下,粒与一部分吸附牢固的反离子随一起移动,粒与一部分吸附牢固的反离子随一起移动,这部分反离子构成吸附层;而另一部分反离子离固相表面较远,而另一部分反离子离固相表面较远,吸引力较小,吸引力较小,在电场中则会向另一方向移动,这些反离子属于扩散层。固液相相对移动时滑动面向另一方向移动,这些反离子属于扩散层。
上的电位称为动电位或ζ上的电位称为动电位或ζ电位,电位,即扩散层的电位差。即扩散层的电位差。
胶体系统的稳定性取决于ζζ电位越大,胶体越稳定,胶体系统的稳定性取决于ζ电位的大小,电位的大小,电位越大,胶体越稳定,因为ζ因为ζ电位大,电位大,胶体粒子之间的排斥力大胶体粒子之间的排斥力大,胶体粒子不易聚集沉降。胶体粒子不易聚集沉降。 H- H-粘土加水拌合成泥浆。粘土加水拌合成泥浆。在H-粘土泥浆中加入其他电解质(粘土泥浆中加入其他电解质(如:
+,对其钠盐,,对其ζ对其ζ电位的影响如下图:电位的影响如下图: 钠盐,即引入Na)
ζ电位
电解质加入量(电解质加入量(%) 当[Na+]大于[H+]时,Na+开始交换H+,Na+与胶核表面的吸引力比
++H+与胶核表面的吸引力要小,与胶核表面的吸引力要小,而Na本身又在做热运动,本身又在做热运动,有更多的Na
+进入扩散层,进入扩散层,而吸附层的Na减少,减少,使ζ电位升高;电位升高;直到ζ直到ζ电位达到
最大值,最大值,此时H+全部被Na+交换;交换;之后继续加入Na+,Na+位于胶团外部,随液相中[Na+]越来越大,越来越大,对双电层有所压迫,对双电层有所压迫,迫使扩散层中的反离子进入吸附层,反离子进入吸附层,ζ电位减小。电位减小。
Ⅳ 粘土与水的作用
一.溶剂化作用
由于胶核表面带电,由于胶核表面带电,就会吸引极性水分子围绕着胶核作定向排
列,越往外,越往外,排列的规则性越差,排列的规则性越差,称为溶剂化作用。称为溶剂化作用。
黏土—水系统中的水可分为三类:水系统中的水可分为三类:
⑴ 牢固结合水(,位于胶核外完全定向排列牢固结合水(3?10个水分子厚)个水分子厚),位于胶核外完全定向排列的水,。牢固结合水的水,由它构成的水膜称为溶剂化膜(由它构成的水膜称为溶剂化膜(或吸附层水膜)或吸附层水膜)。牢固结合水的粘度、的粘度、密度都较大。密度都较大。
,位于牢 ⑵ 松结合水(松结合水(牢固结合水外、牢固结合水外、离开胶核表面200?内),位于牢固结合水外定向排列程度较差的水,固结合水外定向排列程度较差的水,它的粘度和密度都比牢固结合水要小。要小。
⑶ 自由水(,指粘土自由水(离开胶核表面200?以外)以外),指粘土-水系统中胶团以外的完全是无规则排列的普通的水。的完全是无规则排列的普通的水。
二、影响结合水量的因素
1.矿物组成
矿物组成影响分散度,矿物组成影响分散度,影响比表面积,影响比表面积,影响结合水量的大小。影响结合水量的大小。
2.分散度
3.被吸附阳离子的性质
如果被吸附的阳离子是同价离子,如果被吸附的阳离子是同价离子,阳离子半径越小,阳离子半径越小,水化程度越大,水化程度越大,结合水量也就越大。结合水量也就越大。所以结合水量大小排列顺序为:所以结合水量大小排列顺序为:
Li+ > Na+ > K+ ;
Mg2+ > Ca2+ > Sr2+ >Ba2+.
+2+3+在不同价离子之间,在不同价离子之间,电价越低,电价越低,结合水量越大,结合水量越大,即M>M>M。其原因
如下:如下:①电价越高,电价越高,与胶核表面吸引力大,与胶核表面吸引力大,反而把由于溶剂化作用带来的水挤出去一部分,使得由于溶剂化作用吸附的水少;②由于胶核来的水挤出去一部分,使得由于溶剂化作用吸附的水少;
3+表面吸附反离子的个数与反离子的电价有关,表面吸附反离子的个数与反离子的电价有关,如吸附1个M可以换
成吸附3个M+,而虽然1个M3+带的水比1个M+带的水要多,带的水要多,但是3个M+所带的水量要比1个M3+多。
Ⅴ 粘土泥浆的流变特性
一、流变学基础
流体在流动的时候,流体在流动的时候,相临的两层间就会产生内摩擦力F。F的大小正比于A*dv/dy, A*dv/dy, 即F∝A*dv/dy,其中A指两层间的接触面积。指两层间的接触面积。把这一关系写成等式,。F/A关系写成等式,引入一个系数η引入一个系数η,称之为粘度系数(称之为粘度系数(简称粘度)简称粘度)称为剪切应力σ称为剪切应力σ。
σ= F/A =η* dv/dy 该式称为牛顿定律,该式称为牛顿定律,即剪应力和速度梯度成正比,。不符合此正比,符合这一关系的流体称为牛顿流体(符合这一关系的流体称为牛顿流体(或粘性流体)或粘性流体)。不符合此规律的为非牛顿流体。规律的为非牛顿流体。
二、粘土泥浆的流动性
粘土泥浆的流动性好则粘度要小,因此就要采用电解质稀释泥浆以获粘土泥浆的流动性好则粘度要小,
得更好的流动性。得更好的流动性。
1.电解质稀释泥浆的原理
电解质通常采用钠盐,电解质通常采用钠盐,如纯碱Na2CO3,水玻璃Na2SiO3等。
钠盐稀释泥浆的机理钠盐稀释泥浆的机理:泥浆的机理:
(1)通过增大ζ通过增大ζ电位,电位,增厚水膜,增厚水膜,达到稀释目的。达到稀释目的。
+自然界中大多为ζCa-自然界中大多为ζ电位比较小的Ca-Ca-粘土。粘土。Ca-粘土与Na进行离子交
+换后变为Na-Na-粘土,粘土,Na与胶核的吸附力小,与胶核的吸附力小,从而ζ从而ζ电位升高,电位升高,粒子间
+2+排斥力大;的结合水量,所以Na-Na-粘土排斥力大;又因为Na的结合水量 > Ca的结合水量,
的粘土颗粒包裹的水膜较厚,从而有利于粒子间的相互滑动,因此流的粘土颗粒包裹的水膜较厚,从而有利于粒子间的相互滑动,
动性增加。但如果钠盐加入少,不能交换,加入过多,ζ电位又减小,动性增加。但如果钠盐加入少,不能交换,加入过多,电位又减小,钠盐加入量不易控制,因此要对所加的钠盐有所要求,必须加入少量钠盐加入量不易控制,因此要对所加的钠盐有所要求,
也能发生交换反应。也能发生交换反应。如采用纯碱,如采用纯碱,其交换反应式如下:其交换反应式如下:
Na Na Na
Ca-Ca-粘土+Na2CO3 → 粘土+CaCO3 ↓
Na Na
所以应该选择与粘土中有害离子交换后能形成不溶性物质的钠盐,这所以应该选择与粘土中有害离子交换后能形成不溶性物质的钠盐,
,水玻样的钠盐才可用来交换。样的钠盐才可用来交换。一般在工厂中常用的为纯碱(Na2CO3)
璃(mNa2O ? nSiO2 ? xH2O)等。
(2)通过稀释自由水达到稀释目的
一般情况当系统中自由水含量增加时,一般情况当系统中自由水含量增加时,泥浆的流动性就好。泥浆的流动性就好。 粘土一般是在酸性介质中成矿的,因此粘土中加水调制成泥浆后,粘土一般是在酸性介质中成矿的,因此粘土中加水调制成泥浆后,板面带负电,板面带负电,边面通常带正电,边面通常带正电,边—板面间会出现静电引力板面间会出现静电引力,出现静电引力,形成片架状结构(,该结构的空腔内封闭成片架状结构(也称卡片结构或纸牌结构)也称卡片结构或纸牌结构),该结构的空腔内封闭着自由水,着自由水,使得自由水不能活动,使得自由水不能活动,也就是自由水失去了帮助流动的作用,的作用,因此出现了絮凝。因此出现了絮凝。加入钠盐的目的就是为了释放这部分自由水。自由水。那么为什么加入钠盐就可以释放这部分自由水呢?那么为什么加入钠盐就可以释放这部分自由水呢?其原因如下:因如下:
当加入的钠盐通过离解或水解形成强碱性溶液,当加入的钠盐通过离解或水解形成强碱性溶液,使得边面由带正电转向带负电,带正电转向带负电,与带负电的板面互相排斥,与带负电的板面互相排斥,因此会拆开边面和板面结合的结构,和板面结合的结构,使封闭的自由水释放出来,使封闭的自由水释放出来,恢复了自由水的
流动功能,流动功能,达到了稀释泥浆的目的。达到了稀释泥浆的目的。
2.稀释剂必须具备的条件
(1)电解质中必须有1价的碱金属离子,去交换原价的碱金属离子(通常为钠离子)通常为钠离子)来粘土中吸附的离子,来粘土中吸附的离子,使ζ电位升高,电位升高,水膜增厚。水膜增厚。
(2)稀释剂中的阴离子要能与粘土中的有害离子形成难溶的盐类,稀释剂中的阴离子要能与粘土中的有害离子形成难溶的盐类,或者形成稳定的螯合物。或者形成稳定的螯合物。
使系统呈(3)电解质还应该能够直接离解或水解而提供足够的OH-,
碱性, 碱性,从而使边面带负电,从而使边面带负电,拆开卡片结构,拆开卡片结构,恢复自由水的自由活动。恢复自由水的自由活动。 一般情况下泥浆稀释采用水玻璃比Na2CO3要好。要好。一方面CaSiO3溶解度要比CaCO3小,此外还因为粘土粒子可以从溶液中吸附硅酸,此外还因为粘土粒子可以从溶液中吸附硅酸,而硅酸有保护胶体的作用。而硅酸有保护胶体的作用。
3.聚合阴离子的作用
聚合阴离子除了要满足一般阴离子应有的作用外聚合阴离子与聚合阴离子除了要满足一般阴离子应有的作用外,子应有的作用外,
粘土的边表面几何位置相适应,易吸附在边表面上,可以加强边表面粘土的边表面几何位置相适应,易吸附在边表面上,
负电荷,负电荷,甚至可以使边表面从带正电到带负电。甚至可以使边表面从带正电到带负电。
三、粘土泥浆的触变性
1.触变性定义
粘土泥浆静置以后逐渐的变稠凝固,粘土泥浆静置以后逐渐的变稠凝固,但一经搅拌就重新恢复流动性,动性,这样可以重复无数次,这样可以重复无数次,这就叫粘土泥浆的触变性。这就叫粘土泥浆的触变性。
2.触变机理
黏土泥浆中粒子之间存在有各种力:静电力和范氏力。在力的作黏土泥浆中粒子之间存在有各种力:静电力和范氏力。
用下粒子之间会形成一定的结构。如果发生板面—边面结合或边面—用下粒子之间会形成一定的结构。
边面结合,边面结合,即形成卡片结构,即形成卡片结构,水封闭于结构内,水封闭于结构内,泥浆就絮凝。泥浆就絮凝。这种絮凝靠的是物理力,凝靠的是物理力,一经搅动,一经搅动,卡片结构被打散,片结构被打散,原来被封闭的水又释放出来,放出来,恢复流动性。恢复流动性。可以经过无数次的反复,可以经过无数次的反复,这就是触变机理。这就是触变机理。
3.影响触变性的因素
触变性大,触变性大,静置时越容易变稠凝固,静置时越容易变稠凝固,搅拌时越不容易拆散。搅拌时越不容易拆散。
(1) 溶液的pH值
pH < 7,溶液呈现酸性,溶液呈现酸性,边表面带正电,边表面带正电,边面与板面有静电引力,边面与板面有静电引力,再加上边面与边面间的范氏引力的作用,此时易形成卡片结构,触变再加上边面与边面间的范氏引力的作用,此时易形成卡片结构,性好。性好。pH值越小,值越小,边面与板面有静电引力越大,边面与板面有静电引力越大,越容易形成卡片结构,卡片结构越牢固,卡片结构越牢固,触变性越好。触变性越好。
(2) 粘土泥浆的含水量
含水量越多,粒子之间距离越远,越不易相互搭接,触变性越小。 含水量越多,粒子之间距离越远,越不易相互搭接,触变性越小。
(3) 粘土矿物的组成粘土矿物的组成
分散度好,分散度好,粒子数多,粒子数多,粒子间越易搭接,粒子间越易搭接,触变性越大。触变性越大。 如:蒙脱石分散性好,蒙脱石分散性好,最容易形成卡片状结构,最容易形成卡片状结构,触变性好,触变性好,而伊利石分散性差,利石分散性差,触变性也差。触变性也差。
Ⅵ 粘土泥料的可塑性
一、可塑性定义
可塑性指物料在超过一定大小的外力作用下开始变形而不开裂,可塑性指物料在超过一定大小的外力作用下开始变形而不开裂,外力撤除后保持变形后的形状而不复原的能力。外力撤除后保持变形后的形状而不复原的能力。
可塑性的大小取决于泥料的屈服值和开裂前达到的最大应变量乘积的大小。乘积的大小。
二、泥料可塑性产生的原因
粘土颗粒之间吸引力始终大于排斥力,即吸引力始终占优势,才粘土颗粒之间吸引力始终大于排斥力,即吸引力始终占优势,能产生可塑性。能产生可塑性。
泥料中吸引力的来源主要有泥料中吸引力的来源主要有:要有:
1) 毛细管力:毛细管力:粘土颗粒周围形成一层连续水膜,粘土颗粒周围形成一层连续水膜,由于毛细管力作用,使得两个颗粒紧紧连在一起。毛细管力是产生吸引力的细管力作用,使得两个颗粒紧紧连在一起。
主要来源。主要来源。
2)反离子为两个胶核所共同吸引
3)pH小于7时,边面带正电,边面带正电,板面带负电,板面带负电,边面-板面产生静电引力。
4)胶核之间存在着范氏引力。胶核之间存在着范氏引力。
泥料中排斥力的来源:泥料中排斥力的来源:
1) 同号胶体粒子之间存在着静电斥力。同号胶体粒子之间存在着静电斥力。
2) 两个胶粒中的反离子之间相互排斥。两个胶粒中的反离子之间相互排斥。
三、影响泥料可塑性的因素
1.泥料中的含水量
干粘土中加入水,干粘土中加入水,首先满足形成牢固结合水,首先满足形成牢固结合水,其次形成松结合水,其次形成松结合水,再次才以自由水形式存在。次才以自由水形式存在。
当加水量过少时,不能在粘土颗粒周围形成连续水膜则无可塑当加水量过少时,不能在粘土颗粒周围形成连续水膜,在粘土颗粒周围形成连续水膜,性。随着加水量增多,随着加水量增多,能在粘土颗粒周围形成连续水膜,能在粘土颗粒周围形成连续水膜,则有毛细管力F(F=2σ/r)。牢固结合水量越小,牢固结合水量越小,毛细管径越小,毛细管径越小,毛细管力越大。毛细管力越大。即毛细管径小,粒子间吸引力大,泥料变形所需的力就大,屈服值高,即毛细管径小,粒子间吸引力大,泥料变形所需的力就大,屈服值高,
但可塑性的大小取决于屈服值和开裂前最大应变量的乘积,如果开裂但可塑性的大小取决于屈服值和开裂前最大应变量的乘积,前的最大应变量小,前的最大应变量小,可塑性不一定高。可塑性不一定高。继续加入水,继续加入水,又增加了松结合水,松结合水相当于起了润滑剂的作用,松结合水相当于起了润滑剂的作用,胶粒间易滑动,胶粒间易滑动,泥料的延展性好,性好,但松结合水不能太多,但松结合水不能太多,否则毛细管半径增加,否则毛细管半径增加,毛细管力减小,毛细管力减小,又使可塑性降低。又使可塑性降低。因此,因此,含有部分松结合水时,含有部分松结合水时,泥料的可塑性最好泥料的可塑性最好。的可塑性最好。其厚度大约为离开胶核表面100?,相当于约30个水分子层厚。如果个水分子层厚。再加入水到出现自由水时,再加入水到出现自由水时,可塑性就向流动状态过渡了。可塑性就向流动状态过渡了。
2.反离子的性质
主要是看反离子对屈服值和对开裂前最大应变量的影响。主要是看反离子对屈服值和对开裂前最大应变量的影响。 例如:例如:比较钠高岭和氢高岭可塑性的大小:比较钠高岭和氢高岭可塑性的大小:
假定二者分散度一样,则比表面积一样;假定排斥力主要来源于假定二者分散度一样,则比表面积一样;
ζ电位造成;电位造成;假定吸引力主要来源于毛细管力。假定吸引力主要来源于毛细管力。
相同水量的条件下,相同水量的条件下,比表面积一样,比表面积一样,说明水膜厚度一样,说明水膜厚度一样,二者开裂前最大应变量的大小相近。裂前最大应变量的大小相近。水膜厚度一样,水膜厚度一样,毛细管力相等,毛细管力相等,吸引力一样,一样,而ζNa-大于ζH-高岭 ,所以Na-Na-高岭粒子间排斥力比H-高岭粒Na-高岭大于ζ
子间排斥力大,子间排斥力大,则H-高岭中吸引力大于排斥力的程度比Na-Na-高岭的大,说明施加外力时,说明施加外力时,H-高岭越不易变形,高岭越不易变形,H-高岭的屈服值就高。高岭的屈服值就高。因此,H-高岭的可塑性比Na-Na-高岭的好。高岭的好。
调节水量,调节水量,使得二者的屈服值相同,使得二者的屈服值相同,由于ζ由于ζH-高岭小于ζ小于ζNa-Na-高岭,H-
高岭粒子间的排斥力小于 Na-而二者吸引力大 Na-高岭粒子间的排斥力,高岭粒子间的排斥力,
于排斥力的程度相同(,所以于排斥力的程度相同(即屈服值相同)即屈服值相同),所以H-高岭粒子间的吸引力小,H-高岭的毛细管力就可以小一些,高岭的毛细管力就可以小一些,H-高岭的毛细管径可大些,高岭的毛细管径可大些,H-
高岭水膜厚度可大些,H-高岭的粒子间容易滑动,H-高岭开裂前的最高岭水膜厚度可大些,岭的粒子间容易滑动,
大应变量大,大应变量大,所以H-高岭的可塑性比Na-Na-高岭好。高岭好。
3.颗粒的形状和大小
假定有适当的松结合水的前提下,假定有适当的松结合水的前提下,颗粒分散度高,颗粒分散度高,比表面积大;比表面积大;水量一定时,水量一定时,毛细管径越小,毛细管径越小,毛细管力越大,毛细管力越大,吸引力越大,吸引力越大,屈服值增加,可塑性好。可塑性好。
黏土颗粒相同体积不同形状时,黏土颗粒相同体积不同形状时,比表面积不同,比表面积不同,板状要大于其它形状,板状要大于其它形状,一定的水量下,一定的水量下,比表面积大,比表面积大,毛细管径小,毛细管径小,毛细管力大。毛细管力大。而且,而且,板状颗粒之间的接触机会多,颗粒之间的接触机会多,粒子间易搭接,粒子间易搭接,变形前易搭接,变形前易搭接,变形时易搭接,变形后易搭接,变形后易搭接,所以可塑性提高。所以可塑性提高。
例:比较伊利石,比较伊利石,高岭石,高岭石,蒙脱石三种粘土矿物的可塑性蒙脱石三种粘土矿物的可塑性。可塑性。
蒙脱石的分散度大于高岭石大于伊利石,分散度越大,可获得更多蒙脱石的分散度大于高岭石大于伊利石,分散度越大,
的粒子,的粒子,且又是板状粒子,且又是板状粒子,所以可塑性为蒙脱石最好,所以可塑性为蒙脱石最好,高岭石大于伊利石。利石。
