一、授课计划

二、课时教学内容

第二篇:实验1 滴定分析基本操作练习
实验1 滴定分析基本操作练习
一、实验目的
1.学习、掌握滴定分析常用仪器的洗涤和正确使用方法。
2.通过练习滴定操作,初步掌握甲基橙、酚酞指示剂终点的确定。
二、实验原理
0.1mol·L—1 HCl溶液(强酸)和0.1mol·l—1 NaOH(强碱)相互滴定时,化学计量点时的pH为7.0,滴定的pH突跃范围为4.3~9.7,选用在突跃范围内变色的指示剂,可保证测定有足够的准确度。甲基橙(简写为MO)的pH变色区域是3.1(红)~4.4(黄),酚酞(简写为PP)的pH变色区域是8.0(无色)~9.6(红)。
在指示剂不变的情况下,一定浓度的HCl溶液和NaOH溶液相互滴定时,所消耗的体积之比值VHCl/VNaOH应是一定的,改变被滴定溶液的体积,此体积之比应基本不变。借此,可以检验滴定操作技术和判断终点的能力。
三、主要试剂和仪器
1.HCl溶液 6mol·L—1。
2.固体NaOH。
3.甲基橙溶液 1 g·L—1。
4.酚酞溶液 2 g·L—1 乙醇溶液。
四、实验步骤
1.溶液配制
(1)0.1 mol·L—1 HCl溶液
用洁净量杯量取约17 mL 6mol·L—1 HCl溶液,倒人装有约980 mL水的1 L试剂瓶中,加水稀释至1 L,盖上玻璃塞,摇匀。
(2)0.1mol·L—1 NaOH溶液
称取固体NaOH 4g (如何算得的?), 置于250mL烧杯中,马上加入蒸馏水使之溶解,稍冷却后转入试剂瓶中①,加水稀释至1 L,用橡皮塞塞好瓶口,充分摇匀
2.酸碱溶液的相互滴定
(1)用0.1 mol·L-1 NaOH溶液润洗碱式滴定管2,3次,每次用5~10mL溶液润洗。然后将滴定剂倒人碱式滴定管中,滴定管液面调节至0.00刻度。
(2)用0.1 mol·L-1盐酸溶液润洗酸式滴定管2~3次,每次用5~10mL溶液,然后将盐酸溶液倒人滴定管中,调节液面到0.00刻度。
(3)在250mL锥瓶中加入约20mL NaOH溶液,2滴甲基橙指示剂,用酸管中的HCl溶液进行滴定操作练习。
务必熟练掌握操作。练习过程中,可以不断补充NaOH和HCl溶液,反复进行,直至操作熟练后,再进行(4)、(5)、(6)的实验步骤。
(4)由碱管中放出NaOH溶液20~25 mL于锥形瓶中,放出时以每分钟约10mL的速度,即每秒滴入3~4滴溶液,加入2滴甲基橙指示剂,用0.1 mol·l—1 HCl溶液滴定至黄色转变为橙色③。记下读数。平行滴定三份。数据按下列表格记录。计算体积比VHCl/VNa0H,要求相对偏差在±0.3%以内。
(5)用移液管吸取25.00 mL 0.1 mol·L—1 HCl溶液于250mL锥瓶中,加2~3滴酚酞指示剂,用0.1 mol·L—1 NaOH溶液滴定溶液呈微红色,此红色保持30s不褪色即为终点。如此平行测定三份,要求三次之间所消耗Na0H溶液的体积的最大差值不超过±0.04 mL。
(6)同(5)操作,改变指示剂,选用百里酚蓝—甲酚红混合指示剂。平行测定三份,所消耗Na0H溶液的体积,三次之间的最大差值要求≤±0.04mL。
3.滴定记录表格
(1)HCl溶液滴定Na0H溶液(指示剂:甲基橙)

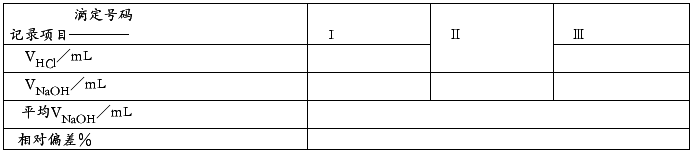
(2)NaOH溶液滴定HCl溶液(指示剂:酚酞)
五、思考题
1.配制NaOH溶液时,应选用何种天平称取试剂?为什么?
2.HCl和NaOH溶液能直接配制准确浓度吗?为什么?
3.在滴定分析实验中,滴定管、移液管为何需要用滴定剂和要移取的溶液润洗几次?滴定中使用的锥形瓶是否也要用滴定剂润洗?为什么?
4.HCl溶液与NaOH溶液定量反应完全后,生成NaCl和水,为什么用HCl滴定NaOH时采用甲基橙作为指示剂,而用NaOH滴定HCl溶液时使用酚酞(或其它适当的指示剂)?
