摘 要
本文以年产25万吨苯乙烯为生产目标,由乙苯脱氢制苯乙烯方法,对整个工段进行工艺设计和设备选型。同时对苯乙烯的新老生产工艺、国内外发展情况做出了一定的总结,并通过了对比选取了较为适宜的工艺,最后确定了Lummus的“SMART”乙苯脱氢工艺作为本设计的详细生产工艺。在计算上,依据物料守恒、能量守恒对整个工艺流程进行了物料衡算和热量衡算,并做出了流程图,依据衡算结果,通过计算对塔设备进行了详细的选型。也对公用工程和车间布置做出了一定的陈述,最后对“三废”处理和安全事项做出了总结。在整个设计中达到了预期要求,完成各个工艺段的设计。
关键字:苯乙烯,工艺计算,设备选型
ABSTRACT
The annual output of 250,000 tons of styrene production targets, the entire section in the process design and equipment selection by the dehydrogenation of ethylbenzene to styrene . Styrene old and new production processes at the same time , the development at home and abroad to make a certain conclusion , and by contrast to select a more appropriate process to finalize the Lummus' " SMART " ethylbenzene dehydrogenation process as the design production process.In the calculation , based on material conservation , energy conservation , the entire process , material balance and heat balance , and made a flow chart , based on accounting results , by calculating the tower equipment , carried out a detailed selection . Public works and plant layout to make a certain statement , and finally made a summary of the " three wastes" treatment and safety matters . Throughout the design to achieve the desired requirements to complete the design of various processes .
Keywords Styrene,Process calculation,equipment selection
目 录
摘 要...................................................................... I
ABSTRACT.................................................................. II
1 绪论.................................................................... 1
1.1 苯乙烯的性质和用途................................................. 1
1.2 苯乙烯常见生产方法................................................. 1
1.2.1 环球化学∕鲁姆斯法............................................ 1
1.2.2 Fina∕Badger法............................................... 3
1.2.3 巴斯夫法...................................................... 3
1.2.4 Halcon法..................................................... 3
1.2.5 裂解汽油萃取分离法............................................ 3
1.2.6 环氧丙烷联产法................................................ 3
2 生产工艺................................................................ 5
2.1 本工艺设计说明..................................................... 5
2.1.1 生产任务...................................................... 5
2.1.2 生产方法...................................................... 5
2.1.3 生产控制参数及具体操作........................................ 5
2.2 生产工艺的反应历程................................................. 6
2.2.1 反应方程式.................................................... 6
2.2.2 生产过程...................................................... 7
2.3 原料、产品及半成品................................................. 8
2.3.1 产品.......................................................... 8
2.3.2 原料.......................................................... 8
2.3.3 半成品........................................................ 8
2.3.4 催化剂........................................................ 8
2.3.5 阻聚剂........................................................ 8
2.4 生产方式的选取..................................................... 9
3 生产工艺计算.......................................................... 10
3.1 物料衡算.......................................................... 10
3.1.1 生产能力的计算............................................... 10
3.1.2 质量守恒定律................................................. 11
3.1.4物料流程图................................................... 15
3.2 热量衡算.......................................................... 15
3.2.1 热量衡算..................................................... 15
3.2.2热量衡算表................................................... 18
4 设备设计计算与选型................................................... 19
4.1 苯∕甲苯精馏塔的设计计算......................................... 19
4.1.1精馏塔的数据确定............................................. 19
4.1.2精馏塔的物料衡算............................................. 19
4.1.3塔板数的确定................................................. 19
4.1.5精馏塔的塔体工艺尺寸计算..................................... 25
4.1.6塔板主要工艺尺寸的计算....................................... 26
4.1.7塔版流体力学验算............................................. 28
4.1.8塔板负荷性能图............................................... 29
4.2冷凝器的设计....................................................... 32
4.3 油水分离器........................................................ 32
4.4过热蒸汽炉......................................................... 33
5 设备一览表及公用工程................................................ 34
5.1 设备............................................................... 34
5.2 公用工程规格...................................................... 34
5.2.1 电........................................................... 34
5.2.2 冷却水....................................................... 35
5.2.3 加热蒸汽..................................................... 35
6 车间布置设计.......................................................... 36
6.1 车间布置设计重要性................................................ 36
6.2 车间生产要求...................................................... 36
6.3 车间安全要求...................................................... 36
6.4 车间发展要求...................................................... 36
7 “三废”处理和安全事项.............................................. 37
7.1 废水............................................................... 37
7.2 废气............................................................... 37
7.3 废渣............................................................... 37
7.4 副产品处理一览表.................................................. 37
7.5 废物处理一览表.................................................... 38
7.6 安全事项.......................................................... 38
结论....................................................................... 39
参 考 文 献............................................................... 40
谢辞....................................................................... 41
1 绪论
1.1 苯乙烯的性质和用途
苯乙烯,分子式 ,结构式
,结构式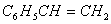 ,是不饱和芳烃最简单、最重要的成员,广泛用作生产塑料和合成橡胶的原料。如结晶型苯乙烯、橡胶改性抗冲聚苯乙烯、丙烯腈-丁二烯-苯乙烯三聚体(ABS)、苯乙烯-丙烯腈共聚体(SAN)、苯乙烯-顺丁烯二酸酐共聚体(SMA)和丁苯橡胶(SBR)。苯乙烯(SM)是含有饱和侧链的一种简单芳烃,是基本有机化工的重要产品之一。苯乙烯为无色透明液体,常温下具有辛辣香味,易燃。苯乙烯难溶于水,25℃时其溶解度为0.066%。苯乙烯溶于甲醇、乙醇、乙醚等溶剂中[1-3]。
,是不饱和芳烃最简单、最重要的成员,广泛用作生产塑料和合成橡胶的原料。如结晶型苯乙烯、橡胶改性抗冲聚苯乙烯、丙烯腈-丁二烯-苯乙烯三聚体(ABS)、苯乙烯-丙烯腈共聚体(SAN)、苯乙烯-顺丁烯二酸酐共聚体(SMA)和丁苯橡胶(SBR)。苯乙烯(SM)是含有饱和侧链的一种简单芳烃,是基本有机化工的重要产品之一。苯乙烯为无色透明液体,常温下具有辛辣香味,易燃。苯乙烯难溶于水,25℃时其溶解度为0.066%。苯乙烯溶于甲醇、乙醇、乙醚等溶剂中[1-3]。
作为合成高分子工业的重要单体,苯乙烯不但能自聚为聚苯乙烯树脂,也易与丙烯腈共聚为AS塑料,与丁二烯共聚为丁苯橡胶,与丁二烯、丙烯腈共聚为ABS塑料,还能与顺丁烯二酸酐、乙二醇、邻苯二甲酸酐等共聚成聚酯树脂等。由苯乙烯共聚的共聚物可加工成为各种日常生活用品和工程塑料,用途极为广泛。目前,全世界苯乙烯生产总量的三分之二用于生产聚苯乙烯,三分之一用于生产各种塑料和橡胶。世界苯乙烯生产能力在1996年已达1900万吨,目前全世界苯乙烯产能约为3000万吨左右[4-5]。
苯乙烯在空气中允许浓度为0.1ml/L,有毒,浓度过高、接触时间过长则对人体的呼吸道造成危害。苯乙烯在高温下容易裂解和燃烧。苯乙烯蒸汽与空气混合能形成爆炸性混合物,其爆炸范围为1.1~6.01%(体积分数)。
1.2 苯乙烯常见生产方法[6-9]
1.2.1 环球化学∕鲁姆斯法
以乙苯为原料,采用脱氢反应器,由开始的单级轴向反应器,中间经历开发了双级轴向反应器到双径向反应器再到双级径向反应器的各种组合优化的多种反应器;反应器的操作压力有开始的正压发展到今天的负压;汽油比有开始的2.5:1发展到今天1.3:1;蒸汽消耗由开始的10kg∕kgSM发展到今天的4kg∕kgSM。UOP∕Lummus的Classic SM流程中乙苯脱氢工艺装置主要有蒸汽过热炉、绝热型反应器、热回收器、气体压缩机和乙苯∕苯乙烯分离塔。过热炉将蒸汽过热至800℃而作为热引入反应器。乙苯脱氢的工艺操作条件为550~650℃,常压或减压,蒸汽∕乙苯质量比为1.0~2.5。
UOP∕Lummus的“SMART” SM工艺是在Classic SM工艺基础上发展的一项新工艺,即在工艺Classic SM工艺的脱氢反应中引入了部分氧化技术。可提高乙苯单程转化率达80%以上。
“SMART”技术的优点在于,通过提高乙苯转化率, 减少了未转化乙苯的循环返回量,使装置生产能力提高,减少了分离部分的能耗和单耗;以氢氧化的热量取代中间换热,节约了能量;甲苯的生成需要氢,移除氢后减少了副反应的发生;采用氧化中间加热,由反应物流或热泵回收潜热,提高了能量效率,降低了动力费用,因而经济性明显优于传统工艺。该技术可用于原生产装置改造,改造容易且费用较低。目前采用“SMART”工艺SM装置有3套在运行。
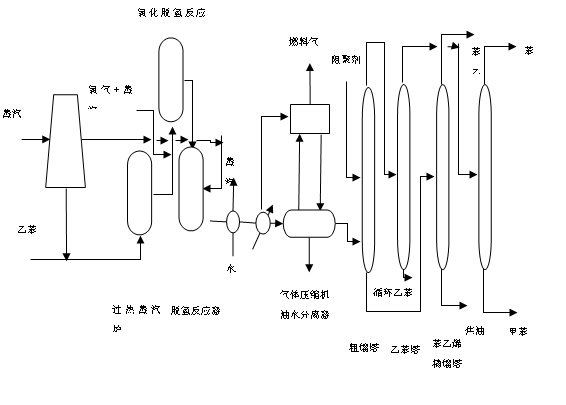
图1.1Lummus的SMART乙苯脱氢工艺流程图
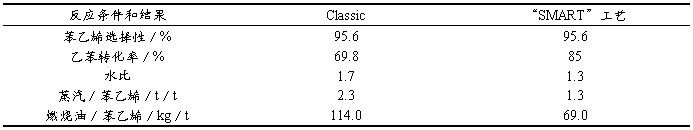
表1.1“SMART”与 Classic比较
1.2.2 Fina∕Badger法
Badger工艺采用绝热脱氢,蒸汽提供脱氢需要的热量并降低进料中乙苯的分压和抑制结焦。蒸汽过热至800~900℃,与预热的乙苯混合再通过催化剂,反应温度为650℃,压力为负压,蒸汽∕乙苯比为1.5%~2.2%。
1.2.3 巴斯夫法
巴斯夫法工艺特点是用烟道气加热的方法提供反应热,这是与绝热反应的最大不同。
1.2.4 Halcon法
Halcon法又称PO-SM联产法。Halcon法公司开发,于1973年在西班牙实现工业化。反应过程中乙苯在液相反应器中用氧化成过氧化物,反应条件为压力0.35MPa,温度141℃,停留时间4h,生成的乙苯过氧化物经提浓度到17%后,进入环氧化工序。环氧化温度为110℃、压力为4.05MPa。环氧化反应液经蒸馏得环氧丙烷。环氧化另一产物甲基苄醇在260℃、常压下脱水得苯乙烯。
1.2.5 裂解汽油萃取分离法
日本日本东丽公司开发了Stex法裂解汽油萃取分离苯乙烯技术,同时还开发了专用萃取剂,可分离出纯度大于99.7%的苯乙烯,同时可生产对二甲苯,并降低裂解汽油加氢负荷,生产成本仅为乙苯脱氢法的一半。
1.2.6 环氧丙烷联产法
环氧烷联产法是先将乙苯氧化成乙苯氢过氧化物,再使之在Mo、W催化剂存在下与丙烯反应生成环氧丙烷和 -苯乙醇,后者脱水可得到苯乙烯。其优点是克服了
-苯乙醇,后者脱水可得到苯乙烯。其优点是克服了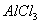 法有污染、腐蚀和需要氯资源的特点;缺点是流程长、投资大,对原料质量要求较高,操作条件严格,联产品多,每吨苯乙烯联产0.45t左右的环氧丙烷,因此不适宜建中小型装置。目前世界上拥有该技术的有阿尔科化学、壳牌和德士古化学。
法有污染、腐蚀和需要氯资源的特点;缺点是流程长、投资大,对原料质量要求较高,操作条件严格,联产品多,每吨苯乙烯联产0.45t左右的环氧丙烷,因此不适宜建中小型装置。目前世界上拥有该技术的有阿尔科化学、壳牌和德士古化学。
2 生产工艺
2.1 本工艺设计说明
2.1.1 生产任务
年产25万吨精苯乙烯,纯度≥99.8%。
2.1.2 生产方法
鲁姆斯(UOP∕Lummus)经典苯乙烯单体生产工艺是全世界生产苯乙烯(SM)单体中最成熟和有效的技术,所以本次参照鲁姆斯(Lummus)公司生产苯乙烯的技术,以乙苯脱氢法生产苯乙烯。鲁姆斯(Lummus)公司经典苯乙烯单体生产工艺技术采用深度减压,绝热乙苯脱氢等几个常见工艺。
蒸汽在脱氢反应中占有很重要的地位,蒸汽的热量可使并维持催化剂处于适当的氧化状态。蒸汽既加热反应进料、减少吸热反应的温度降,同时蒸汽也降低产品的分压使反应平衡向着苯乙烯方向进行,且又可以连续去除积炭以维持催化剂的一定活性。
为达到较好的平衡曲线,系统应该在高温、高压蒸汽稀释和低反应系统压力下进行,对乙苯转化为苯乙烯有利,为了提高转化率,采用两个绝热反应器进行反应,由此乙苯的总转化率可达到70%~85%。新鲜乙苯和循环乙苯先与一部分蒸汽混合,然后在一个用火加热的蒸汽过热器内进行过热,再与过热蒸汽相混合,在一个两段、绝热的径向催化反应系统内进行脱氢。热反应产物在一个热交换器内冷却以回收热量并冷凝。不凝气(主要是氢气)压缩后,经回收烃类后再用作蒸汽过热器的燃料,而冷凝液体分为冷凝水和脱水有机混合物(DM)。
为了减少聚合而损失苯乙烯(SM)单体,在脱水有机混合物(DM)(苯乙烯、未反应乙苯、苯、甲苯和少量高沸物)中加入了一种不含硫的阻聚剂(NSI),然后在乙苯/苯乙烯单体(EB/SM)分馏塔进行分离,塔顶轻组分(EB及轻组分(苯/甲苯)从塔顶取得)去乙苯分离塔,从而从乙苯分离出苯和甲苯,回收的乙苯返回脱氢反应器原料中。EB/SM塔底物(苯乙烯单体和高沸物)在最后苯乙烯分馏塔内进行分馏,塔顶产品即为苯乙烯(SM)单体产品,少量的塔底焦油用作蒸汽过热器的燃料,蒸汽过热器所需大部分燃料来自脱氢废气和苯乙烯焦油[6-9]。
2.1.3 生产控制参数及具体操作
1 投料配比
水蒸气:乙苯=3:1(质量比)
2 温度、压强和时间
脱氢温度控制在600℃左右,负压;
多塔分离控制在常温,常压。
3 具体操作
在脱氢反应器600℃条件下,加入定量的水蒸气、乙苯和氧气混合气体,反应完全后;排除多余的蒸汽;通到冷凝器进行冷凝、降温;输送到气体压缩机油水分离器将有机相和无机相分离,氢气等可燃气体排出成为燃料气;保持恒温20℃左右;和阻聚剂一起加到粗馏塔中,初步分离,塔顶为乙苯、苯和甲苯,塔底为苯乙烯、焦油;将其送至乙苯塔和苯乙烯精制塔,乙苯塔分离出乙苯和甲苯、苯,把乙苯送回脱氢反应器,还将甲苯和苯送到苯∕甲苯塔分离,分离出甲苯和苯。生产工艺流程见Lummus的“SMART”乙苯脱氢工艺流程图。
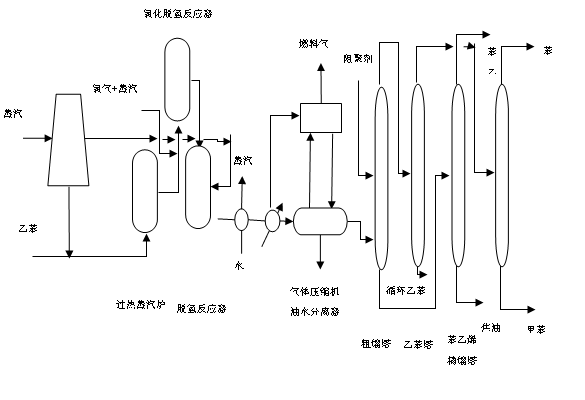
Lummus的SMART乙苯脱氢工艺流程图
2.2 生产工艺的反应历程
2.2.1 反应方程式
 (1)脱氢主反应
(1)脱氢主反应
乙苯(EB)通过强吸热脱氢反应生成苯乙烯(SM):
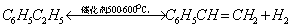
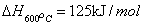
乙苯 苯乙烯 氢气
(2)副反应
乙苯/苯乙烯混合物还会发生某些不受平衡限制的一次反应。这些反应主要是脱烷基反应,反应式为:
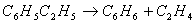
乙苯 苯 乙烯
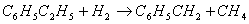
乙苯 氢 甲苯 甲烷
其它反应生成少量的α-甲基苯乙烯和高沸物。
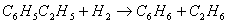
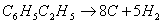
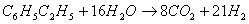
为了减少在催化剂上的结炭,需要在反应器进料中加入高温水蒸气,从而发生下述反应:

脱氢反应式1mol乙苯生成2mol产品(苯乙烯和氢气),因此加入蒸气也可使苯乙烯在系统中的分压降低,有利于提高乙苯的转化率。催化剂以三氧化二铁为主,加上氧化铬、氧化铜、氧化钾等助催化剂涂于氧化铁或碳酸钾等载体上,投料比为水蒸气:乙苯=2~3:1(质量比),反应所得的气体混合物经冷凝、油水分离、多塔分离和精制,制得苯乙烯[10-12]。
2.2.2 生产过程
1预处理过程
蒸汽和乙苯按一定的质量比混合。在脱氢反应器中,水蒸气用量和反应温度对苯乙烯的产率有较大影响。水蒸气用量太少或反应温度太低,会导致反应不完全,产率低;水蒸气用量过多或反应温度过高,催化剂会炭化而降低产率。将原料中的水蒸气(按比例过量)有助于反应向右移,也要严格控制反应温度。
2 脱氢过程
乙苯和蒸汽在脱氢反应器中完成脱氢过程,同时少量的发生其他副反应。
3 冷凝过程
在冷凝器中,将脱氢反应的产物冷凝,降低其温度。
4 油水分离过程
冷凝后,因反应中的水蒸气变为水,通过气体压缩机和油水分离器,将有机相和水分离。
5 多塔分离过程
油水分离的有机相进入粗馏塔,并加入阻聚剂防止苯乙烯聚合,还要进入乙苯塔、苯乙烯精馏塔、苯∕甲苯塔,将依次它们分离出来,把分离出来的乙苯送回脱氢反应器,使其循环。
2.3 原料、产品及半成品
2.3.1 产品
化学名称:苯乙烯 英文名称:styrol
规 格:含量≥99.8% 分 子 量:104.15
沸 点:145.2℃ 熔 点:-30.6℃
折 光 率:1.5439(25℃) 结 构 式: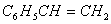
2.3.2 原料
化学名称:乙苯 结构式: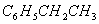
分 子 量:106.16 沸 点:136.2℃
折光指数:1.4959(25℃) 密 度:0.8671g/cm3
2.3.3 半成品
乙苯经脱氢反应器反应后,反应生成物送乙苯—苯乙烯塔分离成乙苯(苯和甲苯)及粗苯乙烯(带重组分及焦油)。
2.3.4 催化剂
催化剂以三氧化二铁为主,加上氧化铬、氧化铜、氧化钾等助催化剂涂于氧化铁或碳酸钾等载体上,使反应更好的发生,有利于苯乙烯的生成。
2.3.5 阻聚剂
在苯乙烯生产工艺中,阻聚剂主要在两个地方起重要作用:一是苯乙烯精馏系统,二是苯乙烯产品贮存系统。在精馏塔中,苯乙烯处于120℃的高温,阻聚剂主要用来防止单体的聚合;在苯乙烯贮存系统中,温度一般为20℃以下,聚合率较低,阻聚剂的主要用途之一是防止苯乙烯氧化。由于温度存在着很大的不同,阻聚剂发挥的主要作用不同,对阻聚剂的要求也不一样,所以,在蒸馏塔中使用无硫阻聚剂(2、4-二硝基-邻-二-丁基酚(DNBP)俗称NSI),在苯乙烯贮存系统中使用4-叔丁基邻苯二酚(TBC)。
2.4 生产方式的选取
全间歇与半间歇(统称间歇式操作)的优点是设备简单,改变生产品种容易;其缺点是原料消耗定额高,能量消耗大,劳动生产率低,产品质量不稳定。连续式操作,原料及能量消耗低,劳动生产率高,因此比较经济;但总投资较大,占地面积较大,一般单线生产能力为2~10万吨/年。半连续操作与连续操作相比设备费用较少,操作较简单,改变生产品种较容易,但产品质量不如连续操作稳定,与间歇操作相比,生产规模更大,劳动生产率也更高,用与较大规模的品种生产,一般为1~2万吨/年。由于苯乙烯用量很大,需连续化大生产。采用连续式操作比较有利。
苯乙烯生产能力根据设计任务规定为年产25万吨。取年工作日为300天,每日生产能力为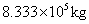 苯乙烯,每小时生产能力为
苯乙烯,每小时生产能力为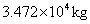 这样的规模采用连续操作是比较合理的。
这样的规模采用连续操作是比较合理的。
3 生产工艺计算
3.1 物料衡算
乙苯脱氢反应方程式为:
主反应C6H5C2H5→C6H5CH=CH2+H2 (式3-1)
副反应C6H5C2H5→C6H6+C2H4 (式3-2)
C6H5C2H5+H2→C6H5CH3+CH4 (式3-3)
物料衡算相关技术条件:
水蒸汽作稀释剂,水蒸汽和乙苯质量比为1.5:1反应压力为150KPa(绝),反应温度为580℃,反应器进口温度630℃,乙苯总转化率为80%,各反应选择性分别为:(4-1)96%、(4-2)1%、(4-3)3%。
原料组成:乙苯,99.6%( W% )。
水蒸汽为惰性组分,不发生水蒸汽转化反应,并且无结焦反应。
冷凝液经油水分离器分离成水和有机混合物,水中夹带芳烃量为500mg/L,夹带芳烃组成同有机混合物相同。有机混合物中水量很少可忽略。
阻聚剂加入量为有机混合物量的0.03(W%)。
精馏塔塔顶苯乙烯回收率大于95%。精馏塔真空操作,塔顶压力<50mmHg。
乙苯-苯乙烯塔真空操作,塔顶压力<200mmHg。塔顶苯乙烯含量<0.25%,塔釜乙苯<0.3%。
苯-甲苯塔塔顶压力<160mmHg,塔顶甲苯<0.5%,塔釜苯<0.2%。
乙苯回收塔,塔顶乙苯<0.1%,塔釜甲苯<0.4%。
3.1.1 生产能力的计算
根据设计任务,苯乙烯的年生产能力为25万吨/年。开工因子=生产装置开工时间/年自然时间。为了充分利用设备,开工因子应取的较大,接近1,但又不能等于1。因为还要考虑到设备的检修以及开停车等情况。开工因子一般取为0.7~0.8。全年365天,则年生产250~300天;因此除去季保养、月保养、修理、放假等总计65天,则年工作日为(365-65)天=300天。定昼夜生产为3班,每天连续生产。
可知每天的生产能力为(250000×103/300)Kg/天=833.3×103Kg/天。以此作为物料衡算的标准。
3.1.2 质量守恒定律
质量守恒定律是“进入一个系统的全部物料量,必须等于离开这个系统的全部物料量,再加上过程中损失量和在系统中累计量”。依据质量守恒定律,对研究系统做物料衡算,可用下式表示:
∑G进=∑G出+∑G损+∑G积
∑G进—输入物料量总和;
∑G出—离开物料量总和;
∑G损—总的损失量;
∑G积—系统中积累量。
(1)进出脱氢反应器的物料衡算
1)对连续生产可确定计算基准为Kg/天,则需计算每天产量及原料投料量
乙苯的脱氢反应
其中原料规格:乙苯(99.6%)水蒸气(95%)
原料乙苯含甲苯0.2%、含苯0.14%,含焦油0.06%。原料水蒸气含5%的杂质气体。
每天产苯乙烯:G8=8.333×105Kg(折算为100%)
每小时产苯乙烯:Gh=3.4721×104Kg
投料比:水蒸气/乙苯 =1.5/1(质量比)
乙苯总转化率:为80%
转化率:脱氢过程为96%
分离率:多塔分离过程为98%
每小时理论投料乙苯量:
G1=(3.472×104×106.15)/(104.15×80%×96%×99%×99%)=4.702×104Kg
每班理论投水蒸气量:
G2=1.5×4.702×104=7.053×104Kg
每小时原料实际投入量: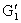
 =(4.702×104/0.996)Kg=4.721×104Kg
=(4.702×104/0.996)Kg=4.721×104Kg
G‘2 =(7.053×104/0.95)Kg=7.453×104Kg
=(7.053×104/0.95)Kg=7.453×104Kg
杂质:G3=(4.721-4.702)×104Kg+(7.081-7.053) ×104Kg=0.470×103Kg
催化剂的量:G4=(4.721+7.453) ×104×0.3%Kg=0.365×103Kg
2)脱氢过程计算
转化率为:80%
苯乙烯的产量G5=(G1×104.15×80%×96%)/106.16Kg=3.543×104Kg
氢气的产量:G6=G1×80%×(96%-3%)×2/106.15Kg=0.659×103Kg
氧气的加入量:G7=(0.5×32×0.659×103)/2=5.273×103 Kg
乙苯剩余量:G1×(1-80%)=9.404×103Kg
生成水G7=(0.659×103×18)/ 2Kg=5.931×103Kg
甲苯的量:生成量+带入量=(G1×92×80%×3%)/106.15+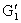 ×0.2%
×0.2%
=978.05+94.42=1072.47
苯的量:生成量+带入量=(G1×78×80%×1%)/106.15+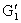 ×0.14%
×0.14%
=276.41+66.10=342.51
进出脱氢反应器的物料衡算见表3.1。
表3.1进出脱氢反应器的物料衡算表(Kg/批)
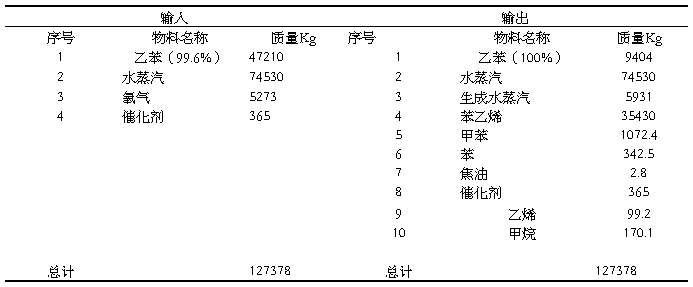
(2)冷凝油水分离阶段的物料衡算
脱氢结束后混合物温度很高,用冷凝器加以冷凝,除去水,温度必须控制在20℃左右,进出冷凝器的物料衡算见表3.2。
表3.2 进出冷凝油水分离器的物料衡算表(Kg/批)
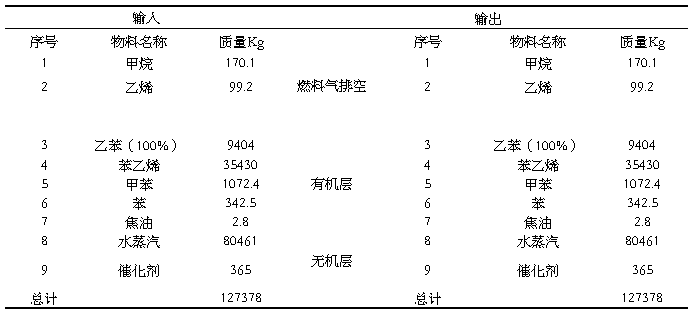
(3)粗馏塔的物料衡算
将有机相加入粗馏塔中进行分离,同时加入阻聚剂防止苯乙烯聚合。加入阻聚剂的量为:(9404+99.2+170.1+35430+1072.4+342.5+2.8)×0.3%=139.563Kg
表3.3粗馏塔的物料衡算表(Kg/批)

(4)乙苯塔的物料衡算表
将粗馏塔塔顶的物料加入到乙苯塔中,进行分离。
表3.4乙苯塔的物料衡算表

(5)苯乙烯精馏塔的物料衡算
将粗馏塔塔底的物料加到苯乙烯的精馏塔中进行分离,进一步浓缩苯乙烯的浓度。
表3.5苯乙烯精馏塔的物料衡算表

(6)苯∕甲苯的物料衡算
将乙苯塔塔顶的物料送到苯∕甲苯塔中,进行分离。
表3.6苯乙烯精馏塔的物料衡算表

3.1.4物料流程图
根据以上物料衡算,物料流程下图
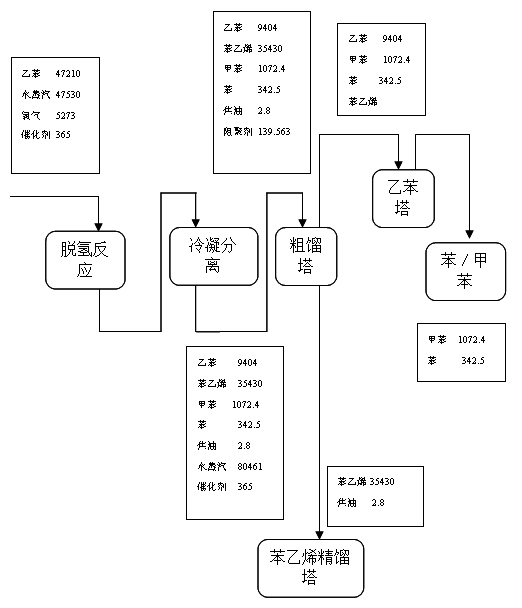
3.2 热量衡算
3.2.1 热量衡算[10-20]
按能量守恒定律“在无轴功条件下,进入系统的热量与离开热量应该平衡”,在实际中对传热设备的衡算可由下式表示
Q1+Q2+Q3=Q4+Q5+Q6 (式3—4)
式中: Q1—所处理的物料带入设备总的热量,KJ;
Q2—加热剂或冷却剂与设备和物料传递的热量(符号规定加热剂加入热量为“+”,冷却剂吸收热量为“-”),KJ;
Q3—过程的热效率,(符号规定过程放热为“+”;过程吸热为“-”)
Q4—反应终了时物料的焓(输出反应器的物料的焓)
Q5—设备部件所消耗的热量,KJ;
Q6—设备向四周散失的热量,又称热损失,KJ;
热量衡算的基准可与物料衡算相同,即对间歇生产可以以每日或每批处理物料基准。(计算传热面积的热负荷必须以每小时作为基准,而该时间必须是稳定传热时间)热量衡算温度基准,一般规定25℃。热量衡算式中各项计算
从 (式3—4)式中可得:
Q2 =Q 4+Q5+Q6-Q1-Q3 (式3—5)
式中各项可用以下计算方法
(1)Q1和Q4的计算
Q1和Q4均可以用下式计算:
Q=∑miciT1(T2)
式中: mi—反应物体系中组分I的质量,Kg;
ci—组分i在0—T℃时的平均比热容,KJ/(Kg*℃)或KJ/(Kmol·℃);
T1(T2)—反应物系反应前后的温度,℃
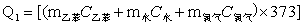
=[(47210×1.738)+(47530×4.2)+(5273×3.5)]×373
=(82050.98+199626+18455.5)×373KJ
=111949415KJ
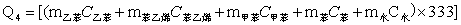
=[(9404×1.859)+(35430×1.555)+(978.05×1.834)+(276.41×3.5)+(47530×4.2)]×333 KJ
=91562633.95KJ
(2)Q3的计算
Q3作为过程的热效率分为化学反应热效应和物理过程热效应,在这次反应中由于物理过程热效应较低,相比化学反应热效应可忽略不计,故过程热效应可由下式表示:

式中Qr—化学反应热效应,KJ;
Qp—物理过程热效应,KJ;(可忽略不计)Qr可通过标准化学反应热qro计算:
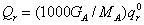
式中  —标准化学反应热,KJ/mol;
—标准化学反应热,KJ/mol;
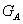 —参与化学反应的A物质质量,Kg;
—参与化学反应的A物质质量,Kg;
 —A物质分子量。
—A物质分子量。

反应体系中各物质标准焓为:
乙苯(40.219J/mol)
苯(33.871 KJ/mol)
甲苯(18.029KJ/mol)
qr0=(33.871+18.029-40.219×10-3)KJ/mol=51.86KJ/mol
Qr=Q3=(1000×35430/104.15)×51.86=17641860.78KJ
(3)Q5的计算
Q 5=∑Micpi (T2—T1)
Mi——设备上i部件质量,kg;
cpi——设备上i部件比热容,kJ/(kg?℃)
T1——设备各部件初温,℃;
T2——设备各部件终温,℃。
由于未连续反应,初温和终温将相同,所以Q5=0
(4)Q6的计算
设备向四周散失的热量Q6可用下式计算:
Q6=∑A×α(Tw-T)θ×10-3
式中 A—设备散热面积(㎡);
Tw—设备外表温度,℃;
T—环境介质温度,℃;
θ—操作过程持续时间(s);
α—对流传质系数,W/(㎡·℃)
当空气做自然对流,散热层表面温度为50~350℃时,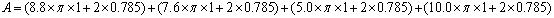
=104.926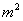
α=8+0.05Tw=(8+0.05×60)W/(㎡·℃)=11W/(㎡·℃)
Q6=104.926×11×(100-25)×3×3600×10-3=934890.66KJ
(5)热负荷Q2的计算
Q2=(Q4+Q5+Q6)-(Q1+Q3)=(91562633.95+0+934890.66)-(111949415+17641860.78) =-37093751.17
查手册得冷却水得cp为4.187KJ/(Kg·℃),则冷却水的用量
G=Q/[cp(t出-t进)]=37093751.17/[4.187×(60-25)]=253121.916kg
3.2.2热量衡算表
由能量守恒定律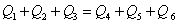 ,能量衡算结果见表3.7
,能量衡算结果见表3.7
表3.7热量衡算表

4 设备设计计算与选型
4.1 苯∕甲苯精馏塔的设计计算
4.1.1精馏塔的数据确定[10-15]
通过计算D=1.435kmol/h,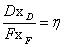 ,设
,设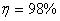 可知原料液的处理量为F=7.325kmol/h,由于每小时处理量很小,所以先储存在储罐里,等20小时后再精馏。故D=28.7
可知原料液的处理量为F=7.325kmol/h,由于每小时处理量很小,所以先储存在储罐里,等20小时后再精馏。故D=28.7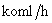 ,F=146.5kmol/h,组分为
,F=146.5kmol/h,组分为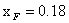 ,要求塔顶馏出液的组成为
,要求塔顶馏出液的组成为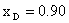 ,塔底釜液的组成为
,塔底釜液的组成为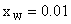 。设计条件如下:
。设计条件如下:
操作压力:4kPa(塔顶表压);进料热状况:自选;
回流比:自选;单板压降:≤0.7kPa;全塔压降: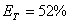 。
。
4.1.2精馏塔的物料衡算
1 原料液及塔顶、塔底产品的摩尔分率
苯的摩尔质量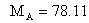 kg/kmol
kg/kmol
甲苯的摩尔质量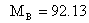 kg/kmol
kg/kmol
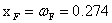 ,
,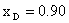 ,
,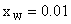
2 原料液及塔顶、塔底产品的平均摩尔质量
 0.274×78.11+(1-0.274)×92.13=87.367kg/kmol
0.274×78.11+(1-0.274)×92.13=87.367kg/kmol
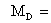 0.9×78.11+(1-0.9)×92.13=79.512kg/kmol
0.9×78.11+(1-0.9)×92.13=79.512kg/kmol
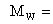 0.01×78.11+(1-0.01)×92.13=91.9898kg/kmol
0.01×78.11+(1-0.01)×92.13=91.9898kg/kmol
3 物料衡算
原料处理量F=88.182kmol/h
总物料衡算88.182=D+W
苯物料衡算88.182×0.274=0.9×D+0.01×W
联立解得D=26.157kmol/h,W=62.025kmol/h
4.1.3塔板数的确定
1.理论板数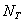 的求取
的求取
(1)相对挥发度的求取
苯的沸点为80.1℃,甲苯额沸点为110.63℃
① 当温度为80.1℃时,纯组分的饱和蒸汽压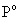 与温度的关系可表示为如下经验式:
与温度的关系可表示为如下经验式:
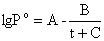
A、B、C为组分的安托因常数,由手册查得
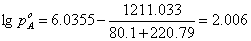
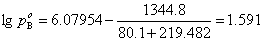
解得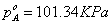 ,
,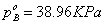 。
。
② 当温度为110.63℃时
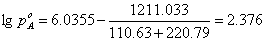
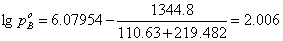
解得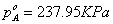 ,
,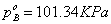 。
。
则有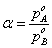 ,代入数据得:
,代入数据得:
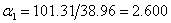
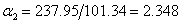
由于差别不是很大,则可取以下式计算
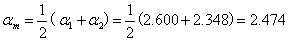
(2)最小回流比的求取
由于是饱和液体进料,有q=1,q线为一垂直线,故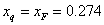 ,根据相平衡方程有
,根据相平衡方程有
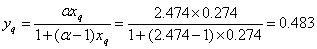
最小回流比为

由经验式知回流比为最小回流比的1.2~2倍,这次设计取1.5,所以
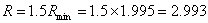
(3)精馏塔的气、液相负荷,在全凝器及泡点回流下
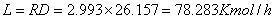



(4)操作线方程
精馏段操作线方程 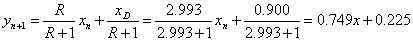
提馏段操作线方程
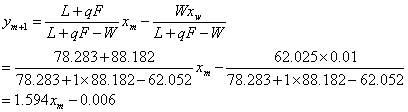
两操作线交点横坐标为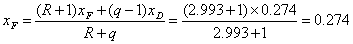
理论板计算过程如下:气液平衡方程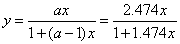
变形有
由y求的x,再将x带入平衡方程,以此类推
 总理论板数为15(包括蒸馏釜),精馏段理论板数为5,第6块板为进料板。
总理论板数为15(包括蒸馏釜),精馏段理论板数为5,第6块板为进料板。
2.实际板层数的求取
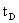 =82.1 ℃
=82.1 ℃  =110.5℃
=110.5℃
平均温度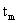 =(
=(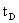 +
+ )/2=(82.1+110.5)/2=96.3℃
)/2=(82.1+110.5)/2=96.3℃
查手册,知
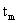 下的粘度为μA=0.27 μB=0.31
下的粘度为μA=0.27 μB=0.31
操作压力为106.7kPa,其中溶液含苯摩尔分数0.274
查表可得纯组分蒸汽压为:


假设一个泡点t,用所得安托因方程算出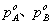 ,设t=100.8
,设t=100.8
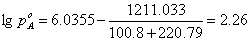
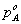 =181.9
=181.9
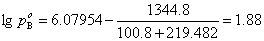
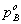 =76.2
=76.2
0.274=
由t-x-y图得 =0.365,
=0.365, =0.635,ya=0.581,yb=0.419
=0.635,ya=0.581,yb=0.419
μL=0.365×0.27+0.635×0.31=0.296
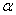 =(ya
=(ya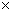 xb)/(yb
xb)/(yb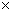 xa)=(0.581×0.635)/(0.419×0.365)=2.412
xa)=(0.581×0.635)/(0.419×0.365)=2.412
Et=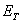 =0.49(
=0.49(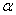
 )
)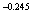 =0.49×(2.412×0.296)
=0.49×(2.412×0.296)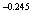 =0.53
=0.53
精馏段实际板层数
N精=5/0.53=9.4=10
N提=9/0.53=16.9=17
4.1.4 精馏塔的工艺条件及有关物性数据的计算
⑴ 操作压力的计算
塔顶操作压力 Pd=101.3+4=105.3( Kpa)
每层板压力:Pm=0.7(KPa)
进料板压力:PW=105.3+10×0.7=108.3(KPa)
精馏段平均压力: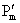 =(105.3+108.3/2=106.8(KPa)
=(105.3+108.3/2=106.8(KPa)
提馏段平均压力:P2m=(113.7+105.3+27×0.7)/2=118.95(KPa)
⑵ 操作温度的计算
塔顶温度tD=82.1℃
进料板温度tF=100.8℃
塔釜温度tW=103.2℃
精馏塔平均温度tm=(82.1+103.2)/2=89.65(℃)
⑶ 平均摩尔质量的计算
塔顶平均摩尔质量的计算
由理论板的计算过程可知,y1=0.9,x1=0.784
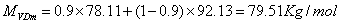
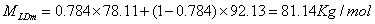
进料板平均摩尔质量的计算
由理论板的计算过程可知,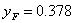 ,
,
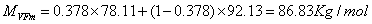
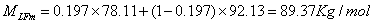
由理论板的计算过程可知,y15=0.013;x15=0.006
MVDm=0.013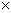 78.11+(1-0.013)
78.11+(1-0.013)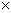 92.13=91.01Kg/mol
92.13=91.01Kg/mol
MLDm=0.006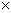 78.11+(1-0.006)
78.11+(1-0.006)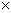 92.13=92.05Kg/mol
92.13=92.05Kg/mol
精馏段的平均摩尔质量为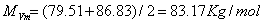

提馏段的平均摩尔质量为
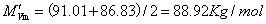
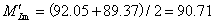
⑷ 平均密度的计算
精馏段平均密度的计算
Ⅰ气相由理想气体状态方程得
ρVm=PmMvw/RTm=(147×83.17)/[8.314×(273.15+89.65)]=4.05kg/m3
Ⅱ液相查不同温度下的密度,可得
tD=82.1.℃时,ρA=812.7kg/m3,ρB=807.9kg/m3
ρLDm=1/(0.9/812.7+0.1/807.9)=812.2kg/m3
tF=100.8℃时,ρA=793.0kg/m3,ρB=788.54kg/m3
tw=103℃时,ρA=790.0kg/m3,ρB=785.0kg/m3
ρLwm=1/(0.01/790.0+0.99/807.9)=807.7kg/m3
提馏段平均密度的计算
气相由理想气体状态方程得
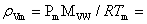 (147×88.92)/[8.31×(273.15+89.65)]
(147×88.92)/[8.31×(273.15+89.65)]
=4.33kg/m3
进料板液相的质量分率
αA=(0.197×78.11)/(0.197×78.11+0.803×92.13)=0.172
ρLFm=1/(0.172/793.0+0.827/788.54)=790.0kg/m3
精馏段液相平均密度为
ρLm=(ρLDm+ρLFm)/2=(812.2+790.0)/2=801.08kg/m3
提馏段液相平均密度
ρLm=(ρLwm+ρLFm)/2=(807.7+790.0)/2=798.9kg/m3
⑸ 平均粘度的计算
液相平均粘度依下式计算
lgμLm=∑(xi lgμi)
a.塔顶液相平均粘度的计算由tD=82.1℃查手册得
μA=0.302mPa.s,μB=0.306mPa.s
lgμLDm=0.900lg(0.302)+0.100lg(0.306)
解得
μLDm=0.302mPa.s
b.进料板平均粘度的计算 由tF=100.8℃查手册得
μA=0.25mPa.s,μB=0.30mPa.s
lgμLFm=0.197lg(0.25)+0.803lg(0.30)
解得
μLFm=0.289mPa.s
精馏段平均粘度
μLm=(0.302+0.289)/2=0.296mPa.s
c.塔底平均粘度的计算由tF=103℃查手册计算得
μLwm=0.26mPa.s
⑹ 液相平均表面张力的计算
液相平均表面张力依下式计算即
σLm=∑xiσi
a. 塔顶液相平均表面张力的计算,由tD=82.1℃查手册得
σA=21.24N/m,σB=21.42N/m
σLDm=0.90×21.24+0.1×21.42=21.258 N/m
b. 进料板液相平均表面张力的计算,由tF=100.8℃查手册得
σA=19.10N/m,σB=19.56N/m
σLFM=0.197×19.10+0.803×19.56=19.46 N/m
精馏段液相平均表面张力
σLm=(21.258+19.46)/2=20.36 N/m
4.1.5精馏塔的塔体工艺尺寸计算
1.塔径的计算
(1)精馏段的气、液相体积流率为
VS=VMVm/3600ρVm=(104.445×83.17)/(3600×4.05)=0.596m3/s
LS=LMLm/3600ρLm=(78.283×85.26)/(3600×801.08)=0.0023m3/s
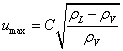 式中,负荷因子
式中,负荷因子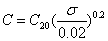 由史密斯关联图[15]查得C20再求的横坐标为Flv=L/V×(ρv/ρl)0.5=0.0532
由史密斯关联图[15]查得C20再求的横坐标为Flv=L/V×(ρv/ρl)0.5=0.0532
取板间距,HT=0.40m,板上清液层高度取hL=0.06m,则HT-hL=0.34 m
由史密斯关联图,得知C20=0.073
气体负荷因子C=C20×(σ/20)0.2=0.0732
Umax=1.027m/s
取安全系数为0.7,则空塔气速为U=0.7 Umax=0.7×1.027=0.719m/s
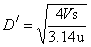 =1.02m
=1.02m
按标准塔径圆整后为D=1.1m
塔截面积为At=3.14×1.1×1.1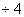 =0.95m2
=0.95m2
实际空塔气速为U实际=Vs/At=0.596/0.95=0.627m/s
U实际/ Umax=0.627/1.033=0.611(安全系数在充许的范围0.5~0.8内,符全设计要求)
⑵由上面可知提馏段
L=389.65kmol/h
V=189.61kmol/h
2.精馏塔有效高度的计算
精馏段有效高度为Z精=(N精-1)HT=(10-1)×0.40=3.6 m
提馏段有效高度为 Z提=(N提-1)HT=(17-1)×0.40=6.4 m
在进料板上方开一个人孔,其高度为0.8 m
故精馏塔有效高度为Z=Z精+Z提+0.8=3.6+6.4+0.8=10.8m
4.1.6塔板主要工艺尺寸的计算[11-16]
1.溢流堰装置计算
因塔径D=1.1m,所以可选取单溢流弓形降液管,采用凹形受液盘。( 此种溢流方式液体流径较长,塔板效率较高,塔板结构简单,加工方便,在直径小于2.2m的塔中被广泛使用。)各项计算如下:
1) 堰长lw
可取lw=0.65D=0.715m
2) 溢流堰高度hw
由hw=hL-how
选用平直堰,(溢流堰板的形状有平直形与齿形两种,设计中一般采用平直形溢流堰板。)堰上层液高度how由下列公式计算,
how=2.84/1000×E×(Lh/lw)(2/3)
lw-----堰长,m;
Lh-----液体体积流量,m3/h;
E-------校正系数
并由图液流收缩系数计算,则可取用E= 1.0 ,则
how=0.014m
取板上清液层高度hL=0.06 m
故 hw=0.046m
3) 弓形降液管的宽度Wd和截面积Af
由lw/D=0.65 m 查图可求得
Af/AT=0.071 1 Wd/D=0.122
Af=0.0711×0.95=0.0675m2
Wd=0.122×1.1=0.132m
并依据下式验算液体在降液管中的停留时间,即
θ=3600Af×HT/Lh= 3600×0.0452×0.40/(3600×0.0017)=10.64s>5s
其中HT即为板间距0.40m,Lh即为每小时的体积流量
验证结果为降液管设计符合要求。
4)降液管底隙高度ho
ho=Lh/(3600×lw×uo')
取uo'=0.09m/s
则ho=0.0017×3600/(3600×0.59×0.09)
=0.032m
Hw-ho=0.046-0.029=0.014m>0.006m
故降液管底隙高度设计合理
选用凹形受液盘,深度h'w=50mm。
2.塔板布置
1) 塔板的分块
因为D≥800mm,所以选择采用分块式,查表可得,塔板可分为3块。
2) 边缘区宽度确定
取Ws=W's=65mm,Wc=35mm
开孔区面积计算
开孔区面积Aa按下面式子计算,则有
Aa=2[x(r2-x2)0.5+∏r2/180×sin-1(x/r)]
其中x=D/2-(Wd+Ws)=1.1/2-(0.132+0.065)=0.353
r=D/2-Wc=1.1/2-0.035=0.515
并由Wd/D=0.122,推出Wd=0.134
由上面推出Aa=0.420m2
筛孔计算与排列
本实验研究的物系基本上没有腐蚀性,可选用δ=3mm碳钢板,取筛孔直径do=5mm
筛孔按正三角形排列,取孔中心距t为
t=3do=15mm
筛孔的数目n为
n=1.155Ao/t2=2156个
开孔率为φ=0.907(do/t)2=10.1%
气体通过阀孔的气速为
uo=Vs/Ao=0.596/(Aa×φ)=14.05m/s
4.1.7塔版流体力学验算
1) 塔板的压降
a 干板的阻力hc计算
干板的阻力hc计算由公式
hc=0.051(uo/co)2×(ρv/ρl)
并取do/δ=5/3=1.67,可查史密斯关联图得,co=0.772
所以hc=0.051(10.63/0.772)2×(4/801.2)=0.0483m液柱
b 气体通过液层的阻力hl的计算
气体通过液层的阻力hl由公式
hl=βhL
ua=Vs/(AT-Af)=0.596(0.95-0.0675)=0.526m/s
Fo=0.526 (4.00)1/2=1.05kg1/2/(s·m1/2)
可得,得β=0.59
所以hl=βhL=0.59×(0.046+0.014)=0.0354 m液柱
c 液体表面张力的阻力hσ计算
液体表面张力的阻力hσ由公式hσ=4σL/(ρl×g×do)计算,则有
hσ=(4×20.34×10-3)/(807.7×9.81×0.005)=0.0021 m液柱
气体通过每层塔板的液柱高度hP,可按下面公式计算
hP=hc+hl+hσ=0.0483+0.0354+0.0021=0.0858m液柱
气体通过每层塔板的压降为
Pp= hP×ρl×g=0.0858×807.7×9.81=680KPa<0.9KPa(设计允许值)
2) 液面落差
对于筛板塔,液面落差很小,由于塔径和液流量均不大,所以可忽略液面落差的影响。
3) 液沫夹带
液沫夹带量,采用公式
ev=5.7×106/σL×[ua/(HT-hf)]3.2
由hf=2.5hL=2.5×0.06=0.15m所以:
ev=(5.7×10-6/20.34×10-3) [0.763/(0.4-0.15)]
=0.010kg液/kg气<0.1kg液/kg气
可知液沫夹带量在设计范围之内。
4) 漏液
对于筛板塔,漏液点气速Uo,min可由公式
Uo,min=4.4Co[(0.0056+0.13 hL-hσ)/ρL/ρV]1/2=5.110m/s
实际孔速为Uo=10.63m/s>Uo,min
稳定系数为K=Uo/Uo,min=10.63/5.110=2.08>1.5
故在本设计中无明显漏液。
5) 液泛
为防止塔内发生液泛,降液管内液高度Hd应服从式子
Hd≤ψ(HT+hw)
甲醇与水属于一般物系,取ψ=0.5,则
ψ(HT+hw)=0.5(0.40+0.046)=0.223m
而Hd=hp+hL+hd
板上不设进口堰,则有
hd=0.153(uo’)2=0.153×(0.099)2=0.00151m液柱
Hd=hp+hL+hd=0.0858+0.06+0.00151=0.147m液柱
则有:Hd≤ψ(HT+hw)
于是可知本设计不会发生液泛
4.1.8塔板负荷性能图[12-15]
精馏段
a 漏液线
Uo,min=4.4Co[(0.0056+0.13 hL-hσ)/ρL /ρV]1/2
Uo,min=Vs, min/Ao
hL= h w +hOW
hOW =2.84/1000×E×(Lh/lw)(2/3)
Vs,min=4.4Co Ao{[0.0056+0.13( hW+2.84/1000×E×(Lh/lw)(2/3))- hσ]ρL /ρV }1/2 =2.039(0.00948+0.127Ls2/3) 1/2
在操作范围内,任取几个Ls值,依上式计算出Vs值计算结果列于下表

b 液沫夹带线
ev =0.1kg液/kg气为限,求Vs—Ls关系如下:
ev=5.7×10-6/σL×[ua/(HT-hf)]3.2
ua=Vs/(AT-Af)=1.693 Vs
hf=2.5hL=2.5(hw+how)
hw=0.046
how=2.84/1000×E×(Lh/lw)(2/3)
hf=2.5(0.046+ 0.98 Ls2/3)=0.115+2.5 Ls2/3
HT-hf=0.40-0.115-2.5Ls2/3=0.285-2.5 Ls2/3
ev=5.7×10-6/20.34×10-3 [1.693Vs/(0.285-2.5 Ls2/3)]3.2 =0.1
整理得Vs=1.06-9.27 Ls2/3
在操作范围内,任取几个Ls值,依上式计算出Vs值计算结果列于下表

c 液相负荷下限线
对于平流堰,取堰上液层高度how=0.005m作为最小液体负荷标准,由式
how=2.84/1000×E×(Lh/lw)(2/3) =0.006
Ls,min=0.00056m/s
据此可做出与气体流量无关的垂直液相负荷下限线3
d 液相负荷上限线
以θ=5s作为液体在降液管中停留时间的下限,由下式
θ=(Af×HT)/Ls=5
故Ls,max=(Af×HT)/5=(0.0452×0.40)/5=0.00362 m3/s
据此可以作出与气体流量无关的垂直液相负荷上限
e 液泛线
令Hd=ψ(HT+hw)
Hd=hp+hL+hd
hP=hc+hl+hσ
hl=βhL
hL=h w+hOW
联立得ψHT+(ψ-β-1)hw=(β+1)hOW+hc+hd+hσ
忽略hσ,将hOW与Ls、hd和Ls、hc与Vs的关系代入上式,得
a'V2s=b'-c' Ls2-d' Ls2/3 式中
a'=[0.051/(Aoco)2]×(ρv/ρl)
b'=ψHT+(ψ-β-1)hw
c'=0.153/(lwhO)2
d'=2.84×10-3×E×(1+β)(3600/lw)(2/3)
将有关数据代入,得
a'=[0.051/(0.101×0.42×0.772)2]×(4.00/801.2)=0.237
b'=0.5×0.4+(0.5-0.59-1)×0.046=0.150
c'=0.153/(0.59×0.029)2=522.63
d'=2.84×10-3×1×(1+0.59)(3600/0.59)(2/3)=1.552 故
V2s=0.63-2205.19 Ls2-6.55 L2/3s
在操作范围内,任取几个Ls值,依上式计算出Vs的值,计算结果如下表

在负荷性能图上,作出操作点A,连接OA,即作出操作线。由图4.2可看出,该筛板的操作上限为液泛控制,下限为漏控制。由图查得
Vs,max= 0.70m3/s,Vs,min=0.20 m3/s
故操作弹性为Vs,max/Vs,min=0.704/0.207=3.400

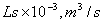
图4.2
(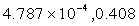 ) (
) (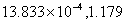 )
)
4.2冷凝器的设计[16-18]
冷凝器按其制冷介质和冷却方式 ,可以分为水冷式 ,空气冷却式和蒸发式三种类型。蒸发式冷凝器主要是利用冷却水蒸发时吸收潜热而使制冷剂蒸气凝结。根据能量守恒原理,假设热损失可忽略不计,则单位时间内热流体放出的热量等冷流体吸收的能量。热负荷Q为:

式中 KJ/(Kg·℃);
KJ/(Kg·℃);
t-冷流体的温度,℃。
Q=376146336.9kJ
管壳式换热器的对数平均温度按逆流计算,即
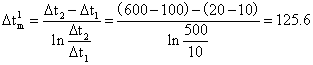 ℃
℃
查得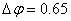 ,所以
,所以
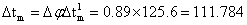 ℃
℃
故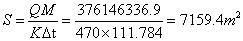
查化工原理上册得,选用TB∕4715-92,列管尺寸为直径19mm;管心距为25mm;管程数为1;管子总根数为1267个;中心排管数为39个;管程流通面积为0.2239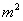 列管长度6000mm,换热面积446.2m2,所以需要16个这样的换热器。
列管长度6000mm,换热面积446.2m2,所以需要16个这样的换热器。
4.3 油水分离器
重力法脱除水中的油滴其基本原理是利用水与油的密度差,使含油污水中的油滴在设备中上浮而除去。
按照Stokes定律,油滴的脱除效率只与油滴粒径、油与水物性、处理量和浮升面积有关,而与浮升高度无关,这就是所谓的“浅池原理”。根据“浅池原理”即可以采用低浮升高度的多层板结构,以增大浮升面积,提高油滴脱除效率。而且由于多层板组当量直径的减小,可使液流在较大流量下保持层流状态,也有利于油滴的有效分离。但是,在一定的设备高度内,增加多层板层数、缩短板距,必然带来要固定多层板而需的结构上的复杂与困难。所以,一般多层板除油装置板距均较大,且不能十分保证水流分布均匀,其处理效率的提高及设备的紧凑化,就受到限制。另一种强化途径是,使含油污水中的细小油滴通过聚结床合并为大油滴,则能使脱油效率得到较大的提高,这就是油滴的聚结。但采用聚结技术,也有限制,即流速要在一定范围内,且不但需要另外的浮升分离空间,还需定期反洗,增加了投资和操作费用。
本高效油水分离器,正是将“浅池原理”和“聚结技术”结合起来,用特殊的内部分离构件和配置,保证了在一定设备容积内,可提供最大的油滴浮升面积,以及尽可能多的油滴聚结机会,并使得水中油滴在浮升中聚结,在聚结中浮升,且内部液流分布均匀,防止了液流的短路与沟流,故在较短的停留时间内,可获得较高的脱油效率。
高效油水分离器为一水平放置的卧式容器,主要由进水部分、出水部分、集油室和由斜通道波纹板构成的主体板组等构成,其结构特点为:
a.可以采用尽可能小的板距而无需固定支撑构件,从而在一定高度设备内,有更多的油滴浮升分离层,保证了在较短的停留时间内,可脱除较小的油滴,得到较高的脱油效率;
b.多层板组的当量直径较小,可在较大流速下,保持层流状态,避免了高处理量下湍流对油滴浮升所带来的不利影响;
c.由于斜通道波纹板一正一反迭放的特殊配置方式,整个板组内形成相互连接的“之”字形通道,水流在三维方向上不断改变方向,这就为油滴之间的碰撞聚结和油滴与构件之间的勃附聚结,提供 了更多的机会,在整个板组中,油滴在浮升中聚结,在聚结中浮升,更进一步促进了脱油效率的提高;
d.由于板组“之”字形通道,也使板组内液流分布比较均匀,避免由于液流不均对脱油带来的不利影响;
e.固体悬浮物也有一定的脱除作用;
f.内构件可采用较薄的碳钢、铝、不锈钢或塑料制造,成本较低,制造、安装和维护清洗都很方便;
g.整个设备可以做成密闭式,可保证安全和防止二次污染。
4.4过热蒸汽炉[16]
过热蒸汽炉的设计依据是按《蒸汽锅炉安全技术监察规程》和《工业锅炉通用技术条件》的规定,并以“安全可靠、节能经济、保护环境、配套齐全、好用好造”为原则设计的。选用HS201或HS219。
5 设备一览表及公用工程
5.1 设备[17-18]
年产50万吨苯乙烯需要的设备及其规格如表5.1所示:
表5.1 主要生产设备一览表

注:另需配套管道阀门若干;100~150吨风冷水塔2个,作为冷却水循环使用装置。
5.2 公用工程规格
5.2.1 电
对输入的动力电源的要求:采用单回路电压为380伏,频率为50赫兹,允许波动范围±3%。电器设备对电源的要求:
(1)对于电动机,使用380伏交流电。
(2)正常照明用220/380伏交流电,事故照明用220伏直流电。
(3)电器部分控制,信号及继电保护用220伏直流电。
(4)仪表电源用100伏和24伏。
5.2.2 冷却水
(1)温度:供水温度为常温,回水温度为进水温度+10℃
(2)压力:回水压力—对于循环冷却水要求回水能直接流到冷却塔顶,不另设接力泵,因此回水压力设为0.4MPa(G)。供水压力:考虑到回水压力加上热交换阻力和管道系阻力,因此取0.6MPa(G)。
(3)污垢系数:根据水质处理费用和热交换费用,决定污垢系数为0.000145(m2·h·℃)KJ。
5.2.3 加热蒸汽
根据生产需要决定蒸汽压力和温度,蒸汽压力取低压0.4MPa(G),进反应器
温度为600℃,出反应器温度为100℃。
6 车间布置设计
6.1 车间布置设计重要性
车间布置设计是从理论走向生产的重要一环,其中要进行各种管路和各种附加设备的布置,详细情况请见图纸。
车间布置的主要内容包括确定各工艺设备在车间的平面和立面位置以及设备的空间方位,确定车间内主要道路及通道的位置,确定各种管道、管线的位置和走向。一个好的设备布置方案应做到经济合理、操作方便、符合安全生产的要求、设备排列整齐美观。总体布局主要应该满足生产、安全、发展三个方面的要求
6.2 车间生产要求
总体布局首先要求保证直径和简捷的生产作业线,尽可能避免交叉和迂回,使各种物料的输送距离为最小。同时将水、电、汽耗量大的车间尽量集中,形成负荷中心,并使其与供应来源靠近,使水、电、汽输送距离为最小。
车间总体布局还应使人流和货流的交通路线径直和简捷,避免交叉和重叠。
6.3 车间安全要求
化工生产车间具有易燃、易爆、有毒的特点,车间应充分考虑安全布局、严格遵守防火、卫生等安全规范和标准的有关规定,重点是防止火灾和爆炸的发生。
6.4 车间发展要求
车间布置要求有较大的弹性,对于生产车间的发展变化有较大的适应性。也就是说,随着工厂不断的发展变化,车间的不断扩大,车间的生产布局和安全布局方面仍能保持合理的布置。
7 “三废”处理和安全事项
7.1 废水
化工废水是指化学工业生产中产生的废水,其中含有随水流失的化工原料,中间产物,产品以及生产过程中产生的污染物。本工艺生产过程中的工业废水主要来源式缩合反应中生成的水,经多次中和洗涤后的水,脱酮、脱苯时气体蒸汽的冷却水,废水中含有钠盐,苯等。治理办法首先从工艺上减少废水的排放量,用沉降法分离废水中的悬浮物质,苯为有毒物质可以考虑用活性分离或膜分离等处理方法将其分离,也可用连续萃取的方法将其做回收处理,经处理的废水达标后方可排放或做循环利用[18-19]。
7.2 废气
化学工业中大气污染物的特点是:有的是有毒物质,有的是对人类有威胁的致癌物质,有的是有强腐蚀性的,有的是易燃易爆气态物。本工艺生产过程中因含有一些低沸点组分而带臭味。一般采用填料式废气洗涤器用水洗涤后除去臭味排除[20]。
7.3 废渣
化学工业固体工业废弃物属工业固体废弃物的一种,主要指硫酸烧渣、铬渣、制碱废渣和磷肥工业废渣。本工艺生产中因山苍子油中含有少量重组分物质,可用燃烧的方法处理[19]。
7.4 副产品处理一览表
表7.1 副产品处理一览表

7.5 废物处理一览表
表7.2 废物处理一览表

7.6 安全事项
该项目生产属于甲级防火,注意跑、冒、漏、滴等现象发生,在生产区内动火要先做好安全防护工作,酸、碱乃强腐蚀物,操作时要有防护面具。苯是有毒物质,要注意作好贮存及其污染治理工作。
结论
1.苯乙烯是具有极好经济效益的精细化工产品,适用于各种有机化工原料,市场
前景极为广阔。
2.采用连续式生产工艺,设备简单,改变生产品种容易,工艺投资收益高,经济
效益很好。
3.本工艺采用乙苯和水蒸汽为原料,脱氢生产出苯乙烯;先后经过冷凝、压缩油
水分离、粗馏、精馏收集苯乙烯。生产技术成熟、可靠,工艺合理,原料成本相
对较低,产品质量、产率都很高。还有这个生产工艺流程,操作和设备都比较稳
定,收效快,适合大型企业选用。
4.本工艺因水洗彻底,而且重要设备采用了耐腐蚀的不锈钢材料,延长了设备的
使用寿命。生产中注重对“三废”的处理,适应绿色化工的步伐,在较大程度上
减少了对环境的污染。
综上所述本工艺设计是可行的,而且很有设计建设价值。
参 考 文 献
[1]夏清,陈常贵.化工原理.天津[M].天津大学出版社,20##年.
[2]Dong-Min Kim,E.Bruce Nauman. Anionic Polymerization of Styrene in a Tubular Reactor[J]. Ind.Eng.Chem.Res. 1999, 38: 1856-1862.
[3]William L. Luyben.Design and Control of the Styrene Process.Ind. Eng.Chem.Res.2011,50,1231–1246.
[4]贾绍义,柴诚敬.化工原理课程设计.天津[M]:天津大学出版社,20##年 .
[5]Taylor.R.;Krishna.1L Modelling reactive distillation[J].Chemical Engineering Science.2000,55,5183—5229.
[6]蔡丽娟.苯乙烯生产技术[J].化工进展,2001(3):74-78.
[7]饶兴鹤.苯乙烯生产现状及工艺技术进展[J].化工生产与技术,2002(5):33-35.
[8]金秋.苯乙烯的技术进展[J].精细化工原料及中间体,2008(4):19-23.
[9]左文明,李小军.苯乙烯生产工艺及国产化技术进展[J].炼油与化工,2007(3):55-56.
[10]左识之.精细化工反应器及车间工艺设计[M].上海:华东理工大学出版社,1998年
[11]汤善莆,朱思明.化工设备机械基础[M](第二版).上海:华东理工大学出版社,20##年
[12]顾芳珍,陈国桓.化工设备设计基础[M].天津:天津大学出版社,1994年
[13]邝生鲁.化学工程师全书[M].北京:化学工业出版社,20##年
[14]国家医药管理局上海医药设计院.化工工艺设计手册(上)[M].北京:化学工业出版社, 1992年
[15]化工设备机械基础编写组.化工设备机械基础[M].北京:化学工业出版社,1979年
[16]唐尔钧,詹长福.化工设备机械基础[M].北京:中央广播电视大学出版社,1985年
[17]汪家鼎等主编.化学工程手册[M].北京:化学工业出版社
[18]陈胜宗.化工过程开发与设计[M].北京:化学工业出版社,20##年
[19]娄爱娟,吴志泉,吴叙美.化工设计[M].上海:华东理工大学出版社,20##年
[20]刘光启,马连湘,刘杰.化学化工物性数据手册[M].北京:化学工业出版社,20##年
[21]王斌,李磊,张国华.中文版Auto CAD 2006实用培训教程[M]. 北京:清华大学出版社,2005 年
[22]魏崇光,郑晓梅.化工工程制图[M].北京:化学工业出版社,1994年
谢辞
本次化工设计我们继化工原理课程设计后对化工设计课程的又一次深刻的认识和实践,为我们以后从事化工行业的工作以及科学研究打下了坚实的基础。
本设计是在我的指导老师范文娟老师的亲切关怀指导下完成的,从课题的选定到工艺合成路线、设备以及附属设备的工艺尺寸和选型的确定,范老师都予以耐心的指导,给了我极大的关怀与帮助;同时范老师渊博的知识、严谨的治学态度和高度的敬业精神深深的感染了我,使我在设计过程中受益颇多,同时也认识到了搞工艺设计的艰辛,尤其是意识到查资料的重要性,在此请允许我对范老师表示崇高的敬意和真心的谢意!
在整个毕业设计过程中,我也得到了化学工程与工艺教研室其他老师以及同学的热心帮助,让我得以如期完成毕业设计,在此,一并向老师和同学致以由衷的感谢。
由于我自身的知识和认识水平有限,设计中难免有错误与不妥之处,恳请老师批评指正。
