综合实验3 海带中碘元素的提取和检验
实验目的
1.了解从海带中分离和检验碘元素的基本原理。
2.知道从海带中分离和检验碘元素的操作流程。
3.理解萃取的原理及萃取方法的适用范围。
4.掌握溶解、过滤、萃取、分液等基本操作的要点。
5.了解物质分离、提纯方法选择的基本原则及一般思路,初步形成用化学实验解决问题的能力。
实验原理
海带、紫菜等海藻中含有碘元素,将海带灼烧成灰,在灰分中加入水,碘元素便以I-的形式进入溶液,用适量的氧化剂(如氯水、过氧化氢溶液等)将I-氧化成I2。I2能与淀粉的水溶液作用显蓝色。有关的化学反应方程式为:2I-+Cl2=I2+2Cl- 2I-+H2O2+2H+==I2+2H2O
萃取是利用溶质在互不相溶的溶剂里溶解度的不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液里提取出来的方法。萃取后往往需要用分液漏斗将这两种不相溶的液体分开,这一操作称为分液。
碘单质易溶于四氯化碳、苯等有机溶剂。用与水不相溶的有机溶剂可以把碘单质从碘的水溶液中萃取出来。
实验用品
仪器:试管、烧杯(两只)、量筒、铁架台、漏斗、滤纸、玻璃棒、酒精灯、火柴、分液漏斗、石棉网
试剂:2 mol·L-1 H2SO4溶液、6%H2O2溶液、CCl4、淀粉溶液、蒸馏水,海带灰
实验步骤
1.检查分液漏斗是否漏水
向分液漏斗中加入少量水,检查旋塞处是否漏水。用右手食指按住分液漏斗上口玻璃塞,将漏斗倒转过来,检查玻璃塞是否漏水。若漏水,须在旋塞芯(或玻璃塞)上涂一层薄薄的凡士林(注意不堵塞上面的小孔),将旋塞芯塞进旋塞内(或将玻璃塞塞进上口),旋转数圈,使凡士林均匀分布。
确信分液漏斗不漏水后,将分液漏斗置于铁架台的铁圈上备用。
2.制取海带灰的浸取液
在小烧杯内取一药匙海带灰,再向其中加入30 mL 蒸馏水,煮沸1~2 min,过滤,得滤液(若滤液稍显浑浊,可重新过滤一次)。
3.碘离子(I-)的氧化
在滤液中加入1~2 mL 2 mol·L-1 H2SO4溶液,再加入3~5 mL 6%H2O2溶液
4.碘的检验
试管中取约1 mL上述反应后的液体(余下的液体备用),向其中滴加几滴淀粉溶液。
5.从碘的水溶液中提取碘
(1)向以上余下的备用液体中,加入约3 mL CCl4,再将混合液转移至分液漏斗中,塞上分液漏斗上口的玻璃塞。
(2)用右手压住分液漏斗的玻璃塞,左手握住旋塞,将分液漏斗倒转过来,用力振摇。开始时,振摇速度要慢,振摇几次后,将漏斗上口向下倾斜,下部支管口斜向上方,左手仍握住旋塞,用拇指和食指旋开旋塞放气,放气时支管口不能对着人,也不能对着火。经几次振摇并放气后,将分液漏斗置于铁架台的铁圈上,静置片刻。
(3)将分液漏斗口上的玻璃塞打开或使塞上的凹槽(或小孔)对准漏斗口上的小孔,使漏斗内外空气相通。
(4)打开旋塞,使下层液体慢慢流出(用小烧杯承接)。待下层液体完全流出后关闭旋塞,将上层液体从漏斗上口倒出。
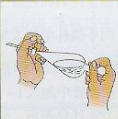

振 摇 分 液
实验现象和结论

实验评价与改进
1.还有哪些氧化剂可将溶液中的I-氧化成I2?本实验中选用过氧化氢作氧化剂有哪些优点?
2.从碘水中提取碘单质时,为什么要加入CCl4并振摇、静置?能否用酒精代替CCl4?为什么?
第二篇:从海带中提取碘实验版
从海带中提取碘
一、实验目的
1.掌握萃取、过滤的操作及有关原理。
2.了解从海带中提取碘的过程。
3.复习氧化还原反应的知识。
二、实验原理
把干海带燃烧后生成的灰烬,海带会中的碘元素以碘离子的形式存在。加入去离子水并煮沸,使碘离子溶于水中,过滤取滤液,调节滤液pH为中性(海带灰里含有碳酸钾,酸化使其层中性或弱酸性对下一步氧化析出碘有利。但硫酸加多了则易使碘化氢氧化出碘而损失)。蒸干滤液,将得到的白色固体与重铬酸钾混合均匀,研磨。在高筒烧杯中加热混合物,此时碘单质会升华出来,用注满冰水的圆底烧瓶盖在烧杯口处,碘就会凝华在烧瓶底部。刮下生成的碘,称量计算产率。

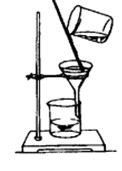 三、实验装置图
三、实验装置图


四、仪器与试剂
仪器:电子天平,天平,圆底烧瓶,高筒烧杯,烧杯(50ml、250mL),酒精灯,剪子,带盖坩埚,泥三角,坩埚钳,蒸发皿,脱脂棉,研钵,pH试纸,定量滤纸,吸滤瓶,导管,橡皮管,小刀。
试剂:干海带(50g),蒸馏水,自来水,H2SO4溶液,重铬酸钾(s)。
五、实验方法
1.取50g食用干海带,用刷子把干海带表面附着物刷净,不要用水洗。将海带剪碎,用酒精润湿放入瓷坩埚中,把坩埚置于泥三角上。
2.用酒精灯灼烧盛有海带的坩埚,至海带完全烧成炭黑色灰后,停止加热,自然冷却。
3.将海带灰倒在烧杯中,依次加入50ml、30ml、10ml蒸馏水熬煮,每次熬煮后,倾泻出上层清夜,抽滤。将滤液和三次浸取液合并在一起,总体积不宜超过40ml。 再加入15mL蒸馏水,不断搅拌,煮沸4min~5min,使可溶物溶解,10分钟后过滤。
4.向滤液里加H2SO4溶液酸化,调节pH值显中性。把酸化后的滤液倒入蒸发皿中,蒸发至干并尽量炒干,将固体转移至研钵中,加入2g重铬酸钾固体,研细。
5.将上述混合物放入干燥的高筒烧杯中,将自来水冷却的烧瓶放在烧杯口上,在烧杯的缺口部位用脱脂棉赛紧,加热烧杯使生成的碘遇热升华。碘蒸气在烧瓶底部遇冷凝华。当在无紫色碘蒸气产生时,停止加热。取下烧瓶,将烧瓶凝聚的固体碘刮到小称量瓶中,称重。计算海带中碘的百分含量。
6.取少量的产品溶于蒸馏水中,加入淀粉试剂,观察是否变蓝。其余的碘单质存放于棕色瓶中,
六、问题与解决
七、撰写论文
