1,2-二溴乙烷的合成
一、实验目的
1. 学习以醇为原料通过烯烃制备邻二卤代烃的实验原理和过程;
2. 进一步巩固蒸馏的基本操作和分液漏斗的使用方法。
二、实验原理
CH3CH2OH → CH2=CH2+H2O
CH2=CH2 + Br2 → BrCH2CH2Br
三、仪器与药品
100mL圆底烧瓶、直形冷凝管、接受弯头、温度计、蒸馏头、分液漏斗、锥形瓶;
乙醇(95%)、液溴、粗砂、浓硫酸(d=1.84)、10%氢氧化钠、无水氯化钙
四、实验装置

五、实验步骤
在250ml 三颈烧瓶A(乙烯发生器)一边侧口插上温度计(接近瓶底),中间装上恒压滴液漏斗,另一侧口通过乙烯出口管与安全瓶B(250ml抽滤瓶)相连,瓶内装有少量水,插入安全管。安全瓶B与洗瓶C(150ml三角瓶或用抽滤瓶)相连,洗瓶C内盛有10%氢氧化钠溶液以便吸收反应中产生的二氧化硫,洗瓶C与盛有3ml液溴的反应管D(具支试管)连接(管内盛有2-3ml水以减少溴的挥发),试管置于盛有冷水的烧杯中,反应管D同时连接盛有碱液的小三角瓶,以吸收溴的蒸气。装置要严密,各瓶塞必须用橡皮塞,切不可漏气。
为了避免反应物发生泡沫而影响反应进行,向三角烧瓶内加入7g粗砂。在冰浴冷却下,将30ml浓硫酸慢慢加入15ml95%乙醇中,摇匀,然后取出10ml混合液加入三颈烧瓶A中,剩余部分倒入恒压滴液漏斗,关好活塞。加热前,先将C与D连接处断开,在石棉网上加热,待温度升到约120℃时,此时体系内大部分空气已排除,然后连接C与D。当A内反应温度升至160-180℃,即有乙烯产生,调节火焰,使反应温度保持在180℃左右,使气泡迅速通过安全瓶B的液层,但并不汇集成连续的气泡流。然后从滴液漏斗中慢慢滴加乙醇-硫酸的混合液,保持乙烯气体均匀的通入反应管D中,产生的乙烯与溴作用,当反应管中溴液褪色或接近无色,反应即可结束,反应时间约0.5h。先拆下反应管D,然后停止加热。
将粗品移入分液漏斗,分别用水、10%氢氧化钠溶液各10ml洗涤至完全褪色,再用水洗涤二次,每次10ml,产品用无水氯化钙干燥。然后蒸馏收集129-133℃馏分,产量7-8g。
纯1,2-二溴乙烷为无色液体,bp为131.3℃,n20D1.5387。
六、注意事项
1、安全管不要贴底部。若安全管水柱突然上升,表示体系发生了堵塞,必须立即排除故障。
2、反应过程中,硫酸既是脱水剂,又是氧化剂,因此反应过程中,伴有乙醇被硫酸氧化的副产物二氧化硫和二氧化碳产生,二氧化硫与溴发生反应:Br2+2H2O→2HBr+H2SO4 故生成的乙烯先要经过氢氧化钠溶液洗涤,以除去这些酸性气体杂质。
3、液溴相对密度为3.119,通常用水覆盖。液溴对皮肤有强烈的腐蚀性,蒸气有毒,故取溴时需在通风橱内小心进行。
4、溴和乙烯发生反应时放热,如不冷却,会导致溴大量逸出,影响产量。
5、仪器装置不得漏气!这是本实验成败的重要因素。
6、粗砂需经水洗,酸洗(用HCl),然后烘干备用。
7、若不褪色,可加数毫升饱和亚硫酸氢钠溶液洗涤。
七、思考题
1、影响1,2-二溴乙烷产率的因素有哪些?试从装置和操作两方面加以说明。
2、本实验装置的恒压漏斗、安全管、洗气瓶和吸收瓶各有什么用处?
3、若无恒压漏斗,可用平衡管。如何安装?
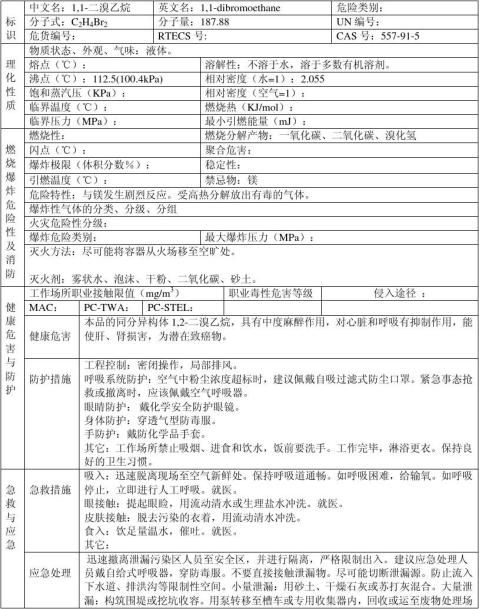
第二篇:1,1-二溴乙烷